
【题目】下列保存物质或试剂的方法不正确的是
A.实验室保存溴时,常在保存液溴的试剂瓶中加入少量水来防止溴挥发
B.盛放溴水的试剂瓶不能用橡胶塞
C.新制氯水应密封保存在棕色试剂瓶中
D.取碘水于试管中,加入CCl4,振荡后静置,溶液分层,上层呈紫红色
科目:高中化学 来源: 题型:
【题目】三种短周期元素在周期表中的位置关系如图所示,下列说法正确的是( )
X | ||
Y | ||
Z |
A.无法确定X,Y,Z是何种元素
B.Z元素没有负价
C.均是非金属元素
D.均能形成双原子分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M
①氧化剂是H3AsO3;②还原性:Cl->As;
③每生成7.5gAs,还原剂失去的电子为0.3 mol;
④M为OH-;⑤ SnCl62-是氧化产物。
关于该反应的说法中正确的组合是( )
A.①③⑤
B.①③
C.①②④⑤
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物在生产、生活中有着重要的应用价值。请按要求回答下列问题。
(1)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理.

通过计算,可知系统(Ⅰ)和系统(Ⅱ) 制氢的热化学方程式分别为_________;_________;制得等量H2所需能量较少的是系統_________。
(2)H2S 与CO2在高温下发生反应: H2S(g)+CO2(g) ![]() COS(g)+H2O(g)。在340℃时,将0.10molCO2与0.10molH2S充入2.5 L的空钢瓶中。
COS(g)+H2O(g)。在340℃时,将0.10molCO2与0.10molH2S充入2.5 L的空钢瓶中。
①该反应平衡后H2O(g)的物质的量分数为0.3,H2S的平衡转化率α1=____,反应平衡常数K=____。
②在350℃重复试验,平衡后H2O(g)的物质的量分数为0.4,H2S的转化率α2_____α1,(填“>”“<”或“=”)该反应的△H____0。
③测定钢铁中硫含量: 将钢铁中的硫转化为H2SO3,然后用一定浓度的I2溶液进行滴定,所用指示剂为____,滴定反应的离子方程式为__________。
已知25 ℃时,H2SO3的电离常数K.a1=1×10-2,Ka2=5×10-8,则该温度下NaHSO3的水解平衡常数Kb=_____。若向NaHSO3溶液中加入少量的I2,则溶液中c(H2SO3)/c(HSO3-)将_______(填“增大”、“减小”或“不变" ).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项表述中,正确的是( )
A.CCl4分子的球棍模型: ![]()
B.![]() 所有碳原子可能在同一平面上
所有碳原子可能在同一平面上
C.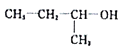 命名为2-甲基-1-丙醇
命名为2-甲基-1-丙醇
D.乙醛、氯乙烯和乙二醇均可作为合成聚合物的单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为: ![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.苹果酸能被氧化成三元羧酸
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.含1 mol苹果酸的稀溶液与足量金属Na反应生成1.5molH2
D.2分子苹果酸相互反应,可形成结构为六元环、七元环或八元环的酯类物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氢有(1H,2H,3H)三种同位素,氯有(35Cl,37Cl)两种同位素.用“精确的天平”分别称量1000个HCl分子,所得数据可能有( )
A.1种
B.5种
C.6种
D.1000种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com