
����Ŀ����15�֣�������H��һ�����ںϳɦé����ڵ��ڼ���ҩ���м��壬��ϳ�·������ͼ����: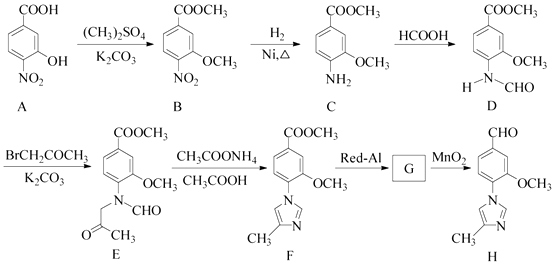
��1��C�еĺ�������������Ϊ�� ��
��2��D��E �ķ�Ӧ����Ϊ ��
��3��д��ͬʱ��������������C��һ��ͬ���칹��Ľṹ��ʽ�� ��
�ٺ��б������ҷ�������һ������̼ԭ�ӣ����ܷ���ˮ�ⷴӦ��ˮ�����֮һ�Ǧ��������ᣬ��һˮ����������ֻ��2�ֲ�ͬ��ѧ�������⣮
��4��G �ķ���ʽΪC12H14N2O2 �� �������õ�H��д��G�Ľṹ��ʽ�� ��
��5����֪�� 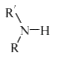
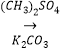
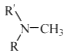 ��R����������R'����������H�� �����
��R����������R'����������H�� ��д���� 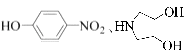 �ͣ�CH3��2SO4Ϊԭ���Ʊ�
�ͣ�CH3��2SO4Ϊԭ���Ʊ� ![]() �ĺϳ�·������ͼ�����Լ����ã��ϳ�·������ͼʾ����������ɣ���
�ĺϳ�·������ͼ�����Լ����ã��ϳ�·������ͼʾ����������ɣ���
���𰸡�
��1���Ѽ�������
��2��ȡ����Ӧ
��3��![]()
��4��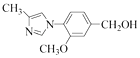
��5��

����������:��1���ɽṹ��֪C�еĺ�������������Ϊ�Ѽ������������Դ��ǣ��Ѽ�����������2��D��EΪ������H��ȡ������Ӧ����Ϊȡ����Ӧ�����Դ��ǣ�ȡ����Ӧ����3��C��һ��ͬ���칹�壬����ٺ��б������ҷ�������һ������̼ԭ�ӣ����ܷ���ˮ�ⷴӦ��ˮ�����֮һ�Ǧ��������ᣬ��һˮ����������ֻ��2�ֲ�ͬ��ѧ�������⣬��ˮ�����Ϊ�Ա����ӣ��Һ��������백��������CΪ����̼����֪���������Ľṹ��ʽΪ ![]() ��
��
���Դ��ǣ� ![]() ����4��G �ķ���ʽΪC12H14N2O2 �� �������õ�H����֪F��G��ת����COOCH3ת��Ϊ��CH2OH�������ṹ���䣬��G�Ľṹ��ʽΪ
����4��G �ķ���ʽΪC12H14N2O2 �� �������õ�H����֪F��G��ת����COOCH3ת��Ϊ��CH2OH�������ṹ���䣬��G�Ľṹ��ʽΪ 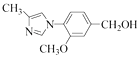 �����Դ��ǣ�
�����Դ��ǣ� 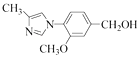 ����5����
����5���� 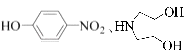 �ͣ�CH3��2SO4Ϊԭ���Ʊ�
�ͣ�CH3��2SO4Ϊԭ���Ʊ� ![]() ����������ϳ����̿�֪����OHת��Ϊ��Br���ө�OHת��Ϊ�Ѽ�������ת��Ϊ�������������Ϣ�еķ�Ӧ����ϳ�����Ϊ ��
����������ϳ����̿�֪����OHת��Ϊ��Br���ө�OHת��Ϊ�Ѽ�������ת��Ϊ�������������Ϣ�еķ�Ӧ����ϳ�����Ϊ ��
���Դ��ǣ�  ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʾ�Ϊ�������ʻ����ǵ���Һ������AΪ����ɫ������C��X��Ϊ��ɫ������ZΪdz��ɫ��Һ��DΪһ�ֳ�����ǿ����
��������֮���ת����ϵ����ͼ�����û�ѧ����ش����⣺�����ֲ�����ʡ�ԣ�

��1��д���������ʵĻ�ѧʽ��A_____________ B ___________ D _____________
��2��A��SO3(g)�ķ�Ӧ������A��X�ķ�Ӧ����д��A��SO3(g)��Ӧ�Ļ�ѧ����ʽΪ��______________________________________________________________________________��
��3����Z��Һ��ͨ��һ������Cl2��д������Z���������Ƿ�Ӧ��ȫ�����Լ���__________��
��4������Eת��Ϊ����F������Ϊ____________________________________________________����ѧ����ʽΪ��_______________________________________________________________________��
��5����10g D����Һ��ͨ��һ������X������D��ȫ��Ӧ���ڵ��������������ᾧ�����յõ�14.8g���塣�ټ��������ᾧ�ڵ��������½��е����ɣ�_________________________________��
�����ù����к��е�����Ϊ__________________ �����ǵ����ʵ���֮��Ϊ__________________����������Ϊ��һ���ʣ�����˿գ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ù���������������һ�����ʵ���Ũ����Һʱ�����в����ܵ�����ҺŨ��ƫ�ߵ��ǣ� ��
A.���ձ����ܽ�ʱ��������Һ�彦��B.��Ʒ�л���̼���ƹ���
C.����ƿʹ��ǰδ������D.����ʱ��������ƿ�̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.6molW�����0.5molX��������2L�ܱ������У�ʹ���Ƿ������·�Ӧ��4W(g)+3X(g) ![]() 2Y(g)+nZ(g)��2minĩ������0.2mol Y������֪��Z��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.0025mol/(L��s)���Լ���
2Y(g)+nZ(g)��2minĩ������0.2mol Y������֪��Z��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.0025mol/(L��s)���Լ���
��1��ǰ2min����W��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ_______________��
��2��2minĩʱX��Ũ��Ϊ_____________________________��
��3����ѧ��Ӧ����ʽ��n=_____________________________��
��4��2minĩ���ָ�����Ӧǰ�¶ȣ���ϵ��ѹǿ�Ƿ�Ӧǰѹǿ��__________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ��CaC2O4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ���ǣ� �� 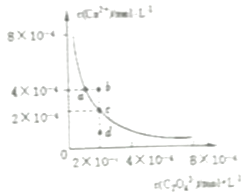
A.��CaC2O4������Һ�м������Na2C2O4������a��䵽b��
B.ͨ������������d��䵽c��
C.d����CaC2O4��������
D.a���Ӧ��Ksp����c���Ӧ��Ksp
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���绯ѧ���������������ڼ�����NH3�ĺ������乤��ԭ��ʾ��ͼ��ͼ������˵������ȷ���ǣ� �� 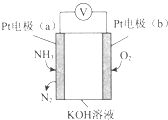
A.��Һ��OH����缫a�ƶ�
B.O2�ڵ缫b�Ϸ�����ԭ��Ӧ
C.��Ӧ���ĵ�NH3��O2�����ʵ���֮��Ϊ4��5
D.�缫a�ķ�ӦʽΪ2NH3��6e��+6OH���TN2+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH3ClΪ��ɫ���Դ���ζ�����壬�ܶ�Ϊ2.25g/L���۵�Ϊ��24.2�棬��������ˮ���������Ҵ��ͱ������л��ܼ��� ��ʵ������ȡCH3Cl��ԭ����CH3OH+HCl��Ũ�� ![]() CH3Cl+H2O�����岽�����£�
CH3Cl+H2O�����岽�����£�
�ٸ���ZnCl2���壻
�ڳ�ȡ24g��ϸ����ˮZnCl2����ȡ20mLŨ�������Բ����ƿ��ͬʱ��ȡһ�����ļ״������Һ©���У�
�۽���Һ©����ļ״���ε�����ƿ�в����ȣ���ZnCl2��ȫ�ܽ����CH3Cl�����ݳ���������ˮ���ռ���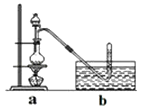
��ش�
��1��ʵ���Ҹ���ZnCl2�����Ƶ���ˮZnCl2�ķ�����
��2����Ӧ�����е�����ƿ�м״�������������٣��״���Ũ��������ʵ���Ũ�Ƚӽ����������� ��
��3��ʵ����Ϊ������ˮ���ռ�CH3Cl��
��4����ij���ϼ��أ�CH4�����е�һ��Hԭ�ӱ�Clԭ��ȡ�������ȶ����ܵ�Ӱ�죬�ɱ�ǿ���������Ը������������������ֻϴ��ƿ���ֱ�ʢ�������Լ��� A.1.5%KMnO4��H+����Һ�� B������ˮ��C.5%Na2SO3��Һ�� D.98%H2SO4
Ϊ֤ʵ��һ���۵Ŀɿ��ԣ��������ѡ����ǡ����ϴ��ƿ����aװ�����ɵ���������ͨ��ϴ��ƿ����ϴ��ƿ��ţ�������۲쵽��֤ʵ�������ϵ���ȷ�ԣ�
��5��д��ϴ��ƿ�з�����Ӧ�����ӷ���ʽ��CԪ�ص���������ΪCO2����
��6�����CH3Cl�Ǵ�������Ⱦ�����ϴ��ƿ֮��Ӧ��һֻʢ��ϴ��ƿ��
��7��ijС��ͬѧȡVmL��CH3Cl��Ⱦ��ˮ������ƿ�У���0.10molL��1����KMnO4��Һ���еζ���ʵ���������������ʾ��
����� | 1 | 2 | 3 | 4 |
����KMnO4��Һ���/mL | 20.90 | 20.02 | 20.00 | 19.98 |
��һ��ʵ�����ݳ����쳣����������쳣��ԭ�������������ĸ���ţ���
a����ƿϴ����δ���� b����ʽ�ζ���������ˮϴ����δ�ñ�Һ��ϴ
c���ζ�����������ƿʱ��Һ�彦�� d���ζ��յ�ʱ���Ӷ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��IUPAC����117��Ԫ��ΪTs���������� ![]() ����ti��n����Ts��ԭ�Ӻ���������������7������˵������ȷ���ǣ�������
����ti��n����Ts��ԭ�Ӻ���������������7������˵������ȷ���ǣ�������
A.Ts�ǵ������ڵڢ�A��Ԫ��
B.Ts��ͬλ��ԭ�Ӿ�����ͬ�ĵ�����
C.Ts��ͬ��Ԫ���зǽ���������
D.������Ϊ176��TS���ط����� ![]() Ts
Ts
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com