
����Ŀ���������ʾ�Ϊ�������ʻ����ǵ���Һ������AΪ����ɫ������C��X��Ϊ��ɫ������ZΪdz��ɫ��Һ��DΪһ�ֳ�����ǿ����
��������֮���ת����ϵ����ͼ�����û�ѧ����ش����⣺�����ֲ�����ʡ�ԣ�

��1��д���������ʵĻ�ѧʽ��A_____________ B ___________ D _____________
��2��A��SO3(g)�ķ�Ӧ������A��X�ķ�Ӧ����д��A��SO3(g)��Ӧ�Ļ�ѧ����ʽΪ��______________________________________________________________________________��
��3����Z��Һ��ͨ��һ������Cl2��д������Z���������Ƿ�Ӧ��ȫ�����Լ���__________��
��4������Eת��Ϊ����F������Ϊ____________________________________________________����ѧ����ʽΪ��_______________________________________________________________________��
��5����10g D����Һ��ͨ��һ������X������D��ȫ��Ӧ���ڵ��������������ᾧ�����յõ�14.8g���塣�ټ��������ᾧ�ڵ��������½��е����ɣ�_________________________________��
�����ù����к��е�����Ϊ__________________ �����ǵ����ʵ���֮��Ϊ__________________����������Ϊ��һ���ʣ�����˿գ�
���𰸡� Na2O2 Na2CO3 NaOH 2Na2O2��2SO3=== 2Na2SO4��O2 ���Ը��������Һ����K3Fe(CN)6�� ��ɫ����Ѹ��ת��Ϊ����ɫ����������ת��Ϊ���ɫ���� 4 Fe(OH)2��2H2O��O2 ===4 Fe(OH)3 ����̼���������¶ȹ���ʱ�ֽ� Na2CO3��NaHCO3 n(Na2CO3): n(NaHCO3)=2:1
�������������������������Ϣ��֪�� AΪ����ɫ���壬��A����Ϊ�������ƣ�C��X��Ϊ��ɫ���壬ZΪdz��ɫ��Һ����Z���������ӣ�DΪһ�ֳ�����ǿ���������֮���ת����ϵ�����ƶϣ�AΪ�������ơ�BΪ̼���ơ�CΪ������DΪ�������ơ�EΪ����������FΪ����������XΪ������̼��ZΪ��������Һ��
��1��A ΪNa2O2 ��B ΪNa2CO3�� DΪ NaOH��
��2��A��SO3(g)�ķ�Ӧ������A��X�ķ�Ӧ����ˣ� A��SO3(g)��Ӧ�Ļ�ѧ����ʽΪ2Na2O2��2SO3=== 2Na2SO4��O2��
��3��Fe2+����ʹ���Ը��������Һ��ɫ��Ҳ������K3Fe(CN)6������ɫ���������ԣ�����Z��Fe2+�Ƿ�Ӧ��ȫ�����Լ�Ϊ���Ը��������Һ����K3Fe(CN)6����
��4������Eת��Ϊ����F������Ϊ����ɫ����Ѹ��ת��Ϊ����ɫ����������ת��Ϊ���ɫ��������ѧ����ʽΪ4 Fe(OH)2��2H2O��O2 ===4 Fe(OH)3��
��5����10g NaOH����Һ��ͨ��һ�����Ķ�����̼������NaOH��ȫ��Ӧ���ڵ��������������ᾧ�����յõ�14.8g���塣�������ᾧ�ڵ��������½��е�������������̼���������¶ȹ���ʱ�ֽ�����10g NaOH�����ʵ���Ϊ0.25mol��������ȫת��Ϊ̼���ƣ��������0.125mol̼���ƣ���13.25g̼���ƣ�������ȫת��Ϊ̼�����ƣ��������0.25mol̼�����ƣ�������Ϊ21g����Ϊ13.25��14.8��21�����������ù����к��е�����ΪNa2CO3��NaHCO3���ɹ���������Ϊ14.8g��֪��106g/mol![]() n(Na2CO3)+ 84g/mol
n(Na2CO3)+ 84g/mol![]() n(NaHCO3)= 14.8g�����������غ��֪��2n(Na2CO3)+n(NaHCO3)=0.25mol������ʽ������������⣬n(Na2CO3)==0.1mol��n(NaHCO3)=0.05mol�����ǵ����ʵ���֮��Ϊn(Na2CO3): n(NaHCO3)=2:1��
n(NaHCO3)= 14.8g�����������غ��֪��2n(Na2CO3)+n(NaHCO3)=0.25mol������ʽ������������⣬n(Na2CO3)==0.1mol��n(NaHCO3)=0.05mol�����ǵ����ʵ���֮��Ϊn(Na2CO3): n(NaHCO3)=2:1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������Ҫ����Al2O3��Al��OH��3��AlO��OH����������Fe2O3�����ʣ����ðݶ���������������������ͼ��ʾ��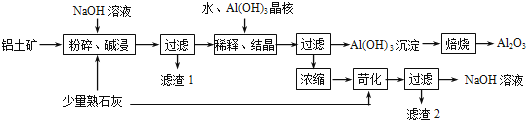
��1����������������ʱӦ�ڸ����½��У���Ŀ���� ��
��2��AlO��OH����NaOH��Ӧ�Ļ�ѧ����ʽΪ�� ��
��3����ϡ�͡��ᾧ�����У�ϡ�͵�Ŀ���� ����Al��OH��3���˵�Ŀ���Ǵٽ�Al��OH��3��������������ϡ�͡��ᾧ�����գ�Ҳ����ͨ�������� ����ķ��������森
��4��Ũ�����õ�NaOH��Һ���������˿����е�CO2���������ʣ������ʿ�ͨ��������Ӧ��ȥ��д��������Ӧ�Ļ�ѧ����ʽ���� ��
��5��������������ʵ�� ���ѧʽ����ѭ�����ã�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������Na2S2O3������Ϊ���ȼ�����֪25.0 mL 0.100 mol��L-1 Na2S2O3��Һǡ�ð�224 mL Cl2����״��������ȫת��ΪCl������S2O32����ת��Ϊ�� ��
A. SO42�� B. S C. SO32�� D. S2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ����ͼ��ʾװ����ȡ�������������Իش��������⣺ 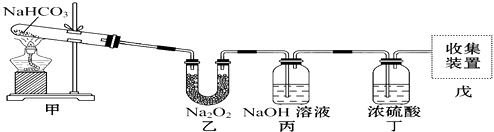
��1�����з����ķ�Ӧ�Ļ�ѧ����ʽΪ��������Na2O2���ܷ����ķ�Ӧ�У�д��ѧ����ʽ��
��2������NaOH��Һ�������� �� ����Ũ����������� ��
��3������ԭװ������˳���Ϊ�ס����������ҡ��죬����װ�������ܷ��ռ�������������ܡ����ܡ�����ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƺ��������Ļ����Һ�У�Al3�������ʵ���Ũ��Ϊ0.2mol��L��1��SO42-Ϊ0.4mol��L��1����Һ��Na�������ʵ���Ũ��Ϊ�� ��
A. 0.1 mol��L��1B. 0.2mol��L��1C. 0.3mol��L��1D. 0.4mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�ӦCO��g��+2H2��g��CH3OH��g�������������仯��ͼ��ʾ��д���÷�Ӧ���Ȼ�ѧ����ʽ�� 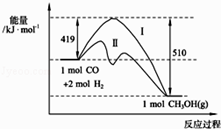
��֪�÷�Ӧ����صĻ�ѧ�������������£�
��ѧ�� | H��H | C��O | H��O | C��H |
E/��kJmol��1�� | 436 | 343 | 465 | 413 |
��C��O�еļ���ΪKJmol��1��ͼ�����ߢ��ʾ���Ӧ�������������仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���йػ�ѧ��Ӧ�������仯��˵����ȷ����( )

A. ͼa��ʾ�������ȷ�Ӧ�������仯
B. ͼaһ����Ҫ���Ȳ��ܷ�����ͼb������Ҳ�ܷ���
C. ͼb�з�Ӧ����������ȶ�
D. ͼb���Ա�ʾ�Ȼ�粒����������������巴Ӧ�������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ǵ�ͳ�в�ҩ���˵���Ч�ɷ�֮һ��������ϸ����ɱ���ж������ã������йغ������ص�������ȷ���ǣ�������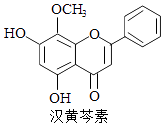
A.�������صķ���ʽΪC16H13O5
B.��������FeCl3��Һ��ɫ
C.1 mol����������ˮ��Ӧ���������1mol Br2
D.������H2�����ӳɷ�Ӧ�÷����й����ŵ��������1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15�֣�������H��һ�����ںϳɦé����ڵ��ڼ���ҩ���м��壬��ϳ�·������ͼ����: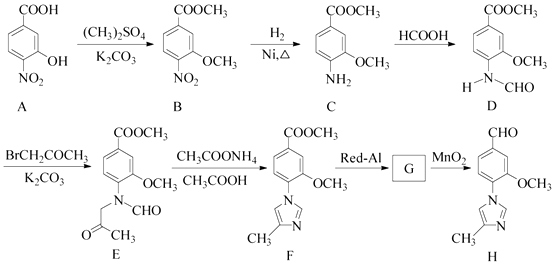
��1��C�еĺ�������������Ϊ�� ��
��2��D��E �ķ�Ӧ����Ϊ ��
��3��д��ͬʱ��������������C��һ��ͬ���칹��Ľṹ��ʽ�� ��
�ٺ��б������ҷ�������һ������̼ԭ�ӣ����ܷ���ˮ�ⷴӦ��ˮ�����֮һ�Ǧ��������ᣬ��һˮ����������ֻ��2�ֲ�ͬ��ѧ�������⣮
��4��G �ķ���ʽΪC12H14N2O2 �� �������õ�H��д��G�Ľṹ��ʽ�� ��
��5����֪�� 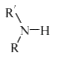
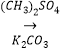
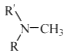 ��R����������R'����������H�� �����
��R����������R'����������H�� ��д���� 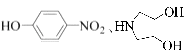 �ͣ�CH3��2SO4Ϊԭ���Ʊ�
�ͣ�CH3��2SO4Ϊԭ���Ʊ� ![]() �ĺϳ�·������ͼ�����Լ����ã��ϳ�·������ͼʾ����������ɣ���
�ĺϳ�·������ͼ�����Լ����ã��ϳ�·������ͼʾ����������ɣ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com