
【题目】X、Y、Z 是短周期元素,在周期表中的位置关系如图所示,下列说法不正确的是
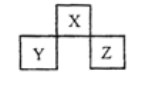
A.X、Z的原子序数之和与Y 的原子序数之比可能为5:3
B.X最简单的气态氢化物的稳定性一定高于Y的气态氢化物
C.Z单质的熔点一定高于Y单质
D.若Z的最高价氧化物为Z2O7,则Y的气态氢化物为YH3
【答案】C
【解析】
根据这三种元素在周期表中的位置结合X、Y、Z是短周期元素判断,X属于第二周期元素,Y和Z是第三周期元素;
A.根据XYZ始终元素的位置关系计算X的原子序数,注意X的原子序数不大于10,且是整数;
B.同一周期元素,非金属元素氢化物的稳定性随着原子序数的增大而增大;同一主族元素,非金属元素氢化物的稳定性随着原子序数的增大而减小;
C.根据元素可能为金属或非金属判断,若是金属,金属单质的熔点增大;若是非金属,非金属单质的熔点减小;
D.根据Z的最高价氧化物判断Z的族序数,从而确定Y的族序数,根据Y的族序数确定其氢化物的化学式;
A.设X的原子序数为a,a必须是正整数且不小于10.则Y的原子序数是a+7,Z的原子序数是a+8
(a+a+9): (a+7)=5:3,a=8,是氧元素,A项正确;
B.由图知,X的非金属性大于其同主族的第三周期元素的非金属性,Y的非金属性小于同一周期的其右边紧相邻主族元素的非金属性,所以X的非金属性大于Y的非金属性,导致X的气态氢化物的稳定性一定高于Y的气态氢化物,B项正确;
C.根据这三种元素在周期表中的位置知,Z和Y可能是金属单质,也可能是非金属单质,如果是金属单质,Z的熔点大于Y,如果是非金属单质,则Y的熔点大于Z,C项错误.
D.若Z的最高价氧化物为Z2O7,Z的化合价是+7价,所以Z是第ⅤⅡA族元素,则Y是第ⅤA族元素,Y的最高化合价是+5价,最低化合价是-3价,所以其气态氢化物的化学式为YH3,D项正确;
答案选C。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.28g乙烯与丙烯组成的混合物中含碳碳双键的数目为NA
B.2mol冰醋酸与4mol乙醇一定条件下充分反应,生成乙酸乙酯个数为2NA
C.室温时,1.0LpH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA
D.标准状况下11.2LCl2溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,体积均为0.5L的两个恒容密闭容器中发生可逆反应:2A(g)+B(g) ![]() 2C(g)△H=-QkJ/mol(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如下表:
2C(g)△H=-QkJ/mol(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如下表:
容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
A | B | C | ||
① | 2 | 1 | 0 | 放热 0.75QkJ |
② | 0.4 | 0.2 | 1.6 | |
下列叙述中正确的是( )
A. 容器①、②中反应的平衡常数均为4
B. 容器②中达到平衡时放出的热量为0.05QkJ
C. 向容器①中通入氦气,平衡时A的转化率不变
D. 其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于2/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中的原因或结论与现象不对应的是
选项 | 现象 | 原因或结论 |
A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
B | 在密闭容器中有反应:A+xB(g) | A非气体、x=1 |
C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 2NO2(g) |
D | 向5mL 0.005mol·L-1 FeCl3溶液中加入5mL 0.015mol·L-1 KSCN溶液,溶液呈红色,再滴加几滴1 mol·L-1 KSCN溶液,溶液颜色加深 | 增大反应物浓度,平衡向正反应方向移动 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。25℃时,向浓度均为0.01mol/L的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成____________沉淀(填化学式),生成该沉淀的离子方程式为______________,当两种沉淀共存时,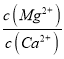 __________(保留两位有效数字)。
__________(保留两位有效数字)。
(2)25℃时,向0.01mol/L的MgCl2溶液中,逐滴加入浓NaOH溶液,刚好出现沉淀时,溶液的pH为____________;当溶液中的离子浓度小于1×10-5mol/L时,认为该离子沉淀完全,当Mg2+完成沉淀时,溶液的pH为___________ (忽略溶液体积的变化,已知:![]() 。
。
(3)该温度下,反应Cu(OH)2+2H+![]() Cu2++2H2O的平衡常数K=_____________。
Cu2++2H2O的平衡常数K=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸(CH3COOOH)是常用的消毒剂,易溶于水、易挥发、见光或受热易分解。制备原理为:H2O2+CH3COOH![]() CH3COOOH+H2O △H<0,制得的过氧乙酸(含少量H2O2)含量测定流程如下,下列说法不正确的是( )
CH3COOOH+H2O △H<0,制得的过氧乙酸(含少量H2O2)含量测定流程如下,下列说法不正确的是( )
![]()
A.应在密闭、低温、避光条件下保存过氧乙酸
B.在常压条件下采用蒸馏操作将过氧乙酸分离出来
C.溶液由无色变为浅红色且30s内不变色,说明H2O2已除尽
D.加过量硫酸亚铁溶液目的是还原CH3COOOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察如图,回答问题:

(1)该装置叫__装置,可以将__能转化为__能。
(2)负极是__,电极反应式为__。
(3)正极是__,电极反应式为__。
(4)电池总反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用粗制ZnO粉末(含杂质Fe、Ni等)制备高纯ZnO的流程如下:
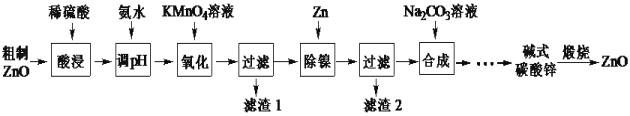
已知:本实验条件下,Ni2+不能被氧化,高锰酸钾还原产物为MnO2;过滤出滤渣1达到除铁目的。
(1)加快酸浸速率可采取的措施_____________________________。(任写一条)
(2)写出“除镍”步骤发生的主要反应离子方程式____________________________。
(3)“滤渣2”的成分是______。
(4)流程中“![]() ”涉及的操作有______、洗涤、______。
”涉及的操作有______、洗涤、______。
(5)获得的碱式碳酸锌需要用水洗涤,检验沉淀是否洗涤干净的方法是_____。
(6)若碱式碳酸锌的成分是ZnCO3· xZn(OH)2。取干燥后的碱式碳酸锌11.2g,煅烧后可得到产品8.1g,则x等于______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题:
(1)以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池中:
①H+向___________极移动(填“正”或“负”)。
②电子流动方向由____________极流向____________极(填:“正”、“负”)。
③若有1mol e- 流过导线,则理论上负极质量减少____________g。
④若将稀硫酸换成硫酸铜溶液,电极质量增加的是___________(填“锌极”或“铜极”),原因是_____________(用电极方程式表示)。
(2)一定温度下,在容积为2 L的密闭容器中进行反应:aN(g) ![]() bM(g) +cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g) +cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a∶b∶c=_________。
②1 min到3 min这段时刻,以M的浓度变化表示的平均反应速率为:________________________。
③下列叙述中能说明上述反应达到平衡状态的是____________________________。
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗a mol N,同时消耗b mol M
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com