
| A. | Na2C2O4水解:C2O42-+2H2O═H2C2O4+2OH- | |
| B. | NH4HSO3溶液与少量NaOH溶液混合:HSO3-+OH-═SO32-+H2O | |
| C. | 将FeS溶液加入过量稀硝酸中:FeS+2H+═Fe2++H2S↑ | |
| D. | 向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═CO32-+2HClO |
分析 A.草酸根离子的水解分步进行,且应该用可逆号;
B.氢氧化钠少量,亚硫酸氢根离子优先反应;
C.稀硝酸具有强氧化性,二者发生氧化还原反应;
D.次氯酸的酸性大于碳酸氢根离子,二者反应生成碳酸时期内和次氯酸.
解答 解:A.Na2C2O4水解主要以第一步为主,其水解的离子方程式为:C2O42-+H2O?HC2O4-++OH-,故A错误;
B.NH4HSO3溶液与少量NaOH溶液混合,反应生成亚硫酸铵、亚硫酸钠和水,反应的离子方程式为:HSO3-+OH-═SO32-+H2O,故B正确;
C.用稀HNO3溶解FeS固体的离子反应为:NO3-+FeS+4H+═Fe3++S↓+NO↑+2H2O,故C错误;
D.NaClO溶液中通入少量CO2,反应生成碳酸氢钠和次氯酸,正确的离子方程式为:ClO-+CO2+H2O═HCO3-+HClO,故D错误;
故选B.
点评 本题考查离子反应方程式书写,为高频考点,题目难度中等,明确发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,试题培养了学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Ba2+、NO3-、NH4+、Cl- | B. | Mg2+、NH4+、SO42-、K+ | ||
| C. | K+、Ba2+、Cl-、HSO3- | D. | Ca2+、HCO3-、NH4+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某有机物的结构简式如图,取足量的H2、NaOH溶液和溴水分别和等物质的量的该物质在一定条件下反应(必要时可以加热),完全反应后消耗的H2、NaOH和Br2三种物质的物质的量之比是( )
某有机物的结构简式如图,取足量的H2、NaOH溶液和溴水分别和等物质的量的该物质在一定条件下反应(必要时可以加热),完全反应后消耗的H2、NaOH和Br2三种物质的物质的量之比是( )| A. | 3:4:1 | B. | 5:4:1 | C. | 3:5:1 | D. | 3:5:0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由非金属元素形成的某些共价化合物的熔点高于某些金属单质的熔点 | |
| B. | 只有在原子中,质子数才与核外电子数相等 | |
| C. | 目前使用的元素周期表中,最长的周期含有18种元素 | |
| D. | 由短周期非金属元素形成的纯净物中,相邻原子之间最多只能共用2对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
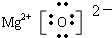 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “三聚氰胺”奶粉事件是化学问题,不是商家的道德问题 | |
| B. | 爆炸一定是化学变化 | |
| C. | 某国产化妆品的生产不使用任何化学原理和方法 | |
| D. | 我们学习化学学科,应该做到:准确理解、辩证看待以及正面传播它 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9gD2O和9gH2O中含有的质子数均为5NA | |
| B. | 2L0.5mol/LH2SO3溶液中含有的H+数小于2NA | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
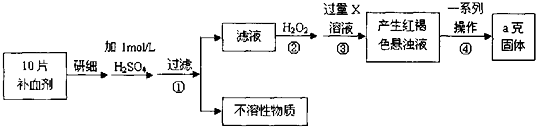
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com