
【题目】红矾钠(重铬酸钠:![]() )是重要的基本化工原料,应用十分广泛。工业制备红矾钠的流程如下:
)是重要的基本化工原料,应用十分广泛。工业制备红矾钠的流程如下:
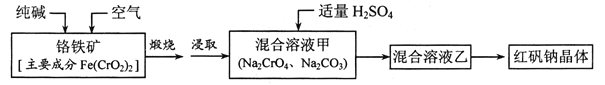
请回答下列问题:
(1)![]() 的基态电子排布式为____________。
的基态电子排布式为____________。
(2)锻烧铬铁矿发生反应:____________Fe(CrO2)2+Na2CO3+O2![]() Fe2O3+Na2CrO4+CO2 配平上述化学反应方程式。
Fe2O3+Na2CrO4+CO2 配平上述化学反应方程式。
(3)溶液甲中加入H2SO4时,可以观察到溶液由黄色变为橙色,并放出无色气体,有关反应的离子方程式为____________。
(4)制备红矾钠的废水必须进行处理。首先酸化废水,将含+6价铬的酸性废液放入电解槽内,用铁作阳极进行电解,阴极析出H2,阳极产物被![]() 氧化然后转化为Cr(OH)3、 Fe(0H)3 沉淀。
氧化然后转化为Cr(OH)3、 Fe(0H)3 沉淀。
①阳极的电极反应式为(不考虑后续反应):____________。
②溶液中金属离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因:______。
③已知某含![]() 的酸性废水中Cr元素的含量是52.5mg/L,处理后Cr元素最高允许 排量为0.5 mg/L。要处理100 m3废水达到排放标准,至少消耗铁_____kg。
的酸性废水中Cr元素的含量是52.5mg/L,处理后Cr元素最高允许 排量为0.5 mg/L。要处理100 m3废水达到排放标准,至少消耗铁_____kg。
【答案】1s22s22p63s23p63d3或[Ar] 3d3 4Fe(CrO2)2+8Na2CO3+7O2![]() 2Fe2O3+8Na2CrO4+8CO2 2 CrO42-+2H+
2Fe2O3+8Na2CrO4+8CO2 2 CrO42-+2H+![]() Cr2O72-+H2O、CO32-+2H+==CO2↑+H2O Fe-2e-==Fe2+ 阴极区水电离出的H+得电子产生H2,促进水的电离平衡正向移动,使溶液OH-浓度增大 16.8
Cr2O72-+H2O、CO32-+2H+==CO2↑+H2O Fe-2e-==Fe2+ 阴极区水电离出的H+得电子产生H2,促进水的电离平衡正向移动,使溶液OH-浓度增大 16.8
【解析】
(1)Cr为24号元素,位于周期表中第四周期VIB族;
(2)利用化合价升降法配平;
(3)加入硫酸时,碳酸钠与硫酸反应生成硫酸钠、二氧化碳和水,铬酸根在酸性环境下可以变成重铬酸根,黄色溶液逐渐变成橙色;
(4)①铁作阳极时,铁失电子生成亚铁离子;
②阴极为水得电子生成氢气和氢氧根离子,破坏水的电离平衡;
③根据6Fe2++Cr2O72-+14H+=6Fe3++ 2Cr3++7H2O计算。
(1)Cr为24号元素,位于周期表中第四周期VIB族,基态电子排布式为1s22s22p63s23p63d3或[Ar]3d3;
(2)反应中,Fe化合价由+2变为+3价,Cr由+3价变为+6价,1molFe(CrO2)2失去7mol电子,O2化合价由0价变为-2价,1molO2得到4mol电子,最小公倍数为28,则方程式为4Fe(CrO2)2+8Na2CO3+7O2![]() 2Fe2O3+8Na2CrO4+8CO2;
2Fe2O3+8Na2CrO4+8CO2;
(3)加入硫酸时,碳酸钠与硫酸反应生成硫酸钠、二氧化碳和水,铬酸根在酸性环境下可以变成重铬酸根,黄色溶液逐渐变成橙色,则反应的离子方程式为2 CrO42-+2H+![]() Cr2O72-+H2O、CO32-+2H+==CO2↑+H2O;
Cr2O72-+H2O、CO32-+2H+==CO2↑+H2O;
(4)①铁作阳极时,铁失电子生成亚铁离子,电极反应式为Fe-2e-==Fe2+;
②阴极为水得电子生成氢气和氢氧根离子,反应式为2H2O-2e-=H2↑+2OH-,破坏水的电离平衡,溶液中氢离子浓度减小,OH-浓度增大;
③阳极产生的亚铁离子与Cr2O72-反应生成铁离子、铬离子,n(Fe2+):n(Cr2O72-)=6:1,溶液中减少m(Cr3+)=100×103L×(52.5mg/L-0.5mg/L)10-3g/mg =5200g,减少Cr元素的质量=5200g/52g/mol=100mol,则n(Fe2+)=300mol,消耗铁的质量为300mol![]() 56g/mol=16800g=1.68kg。
56g/mol=16800g=1.68kg。


科目:高中化学 来源: 题型:
【题目】下列关于金属腐蚀与防护的说法不正确的是
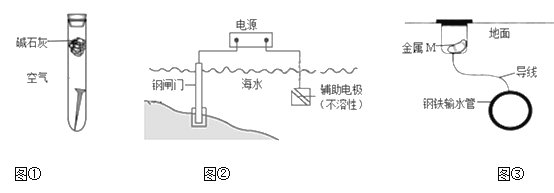
A. 图①,放置于干燥空气中的铁钉不易生锈
B. 图②,若将钢闸门与电源的正极相连,可防止钢闸门腐蚀
C. 图②,若断开电源,钢闸门将发生吸氧腐蚀
D. 图③,若金属M比Fe活泼,可防止输水管腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)铅蓄电池是典型的二次电池,电池总反应式为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________________________。当外电路通过1 mol电子时,理论上负极板的质量增加______g。
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________________________。当外电路通过1 mol电子时,理论上负极板的质量增加______g。
(二)某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若用HNO3(浓)作电解质溶液,电极为铜片和铝片,正极上发生的电极反应式为________________;
(2)若电解质溶液为0.5mol/LNaOH溶液,电极为镁片和铝片,则负极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中各组物质不能实现如图所示转化的是
![]()
选项 | 甲 | 乙 | 丙 |
A | CO2 | NaHCO3 | Na2CO3 |
B | AlCl3 | Al2O3 | NaAlO2 |
C | AlCl3 | Al | Al(OH)3 |
D | AlCl3 | Al(OH)3 | NaAlO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表中的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | E | F | H | J | ||||
3 | B | C | D | G | I |
根据A~J在周期表中的位置,用元素符号或化学式回答下列问题:
(1)化学性质最不活泼的元素是________,氧化性最强的单质是________,还原性最强的单质是________。
(2)最高价氧化物对应的水化物中,碱性最强的是________,酸性最强的是________,呈两性的是________。
(3)A分别与E、F、G、H、I形成的简单气态化合物中,最稳定的是________。
(4)在B、C、D、G、I中,原子半径最大的是________。
(5)元素C与I形成的化合物的电子式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X(仅含三种短周期元素)是一种储氢材料,X中某种元素的单质常用来制造信号弹和烟火,某研究小组为了探究X的组成和性质,设计并完成了如下实验。(金属互化物——全部由金属元素组成的化合物)
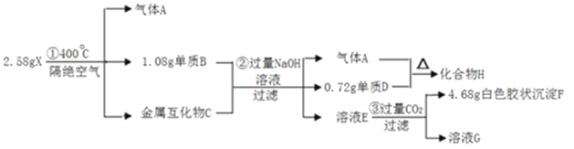
(1)写出H的电子式:________。
(2)X在400℃下分解的化学方程式:________。
(3)下列说法中正确的有:________。
A.化合物H可以与水反应生成氢气 B.单质D可以在干冰中燃烧 C.往溶液E中逐滴加入稀盐酸,将立刻产生白色沉淀 D.溶液G的成分可用于泡沫灭火器
(4)金属化合物C分别与足量盐酸和足量氢氧化钠溶液反应产生的气体物质的量之比为:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g) ![]() 2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
A. 平衡常数K值越大,X的转化率越大
B. 达到平衡时,反应速率v正(X)=2v逆(Z)
C. 达到平衡后降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
D. 达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷厄姆和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。![]() 、
、![]() 常用作锂离子电池的正极材料,请回答下列问题:
常用作锂离子电池的正极材料,请回答下列问题:
(1)基态锂原子的最高能级的电子云形状是________;基态磷原子有________个未成对电子;基态铁原子核外电子排布式为________。
(2)![]() 中
中![]() 的配位数为4,配体中N的杂化方式为________,该配离子中各元素的第一电离能由小到大的顺序为________(用元素符号表示)。
的配位数为4,配体中N的杂化方式为________,该配离子中各元素的第一电离能由小到大的顺序为________(用元素符号表示)。
(3)![]() 在水中易被还原成
在水中易被还原成![]() ,而在氨水中可稳定存在,其原因为________。
,而在氨水中可稳定存在,其原因为________。
(4)![]() 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:

这类磷酸根离子的化学式可用通式表示为________(用n代表P原子数)。
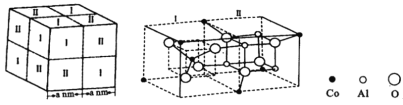
(5)钴蓝晶体结构如下图,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成。晶体中![]() 占据
占据![]() 形成的________(填“四面体空隙”或“八面体空隙”);钴蓝晶体的密度为___________
形成的________(填“四面体空隙”或“八面体空隙”);钴蓝晶体的密度为___________![]() (列出计算式,用
(列出计算式,用![]() 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组欲制备三草酸合铁(Ⅲ)酸钾并用离子交换法测定其配离子的电荷,实验过程如下:
Ⅰ.三草酸合铁(Ⅲ)酸钾的制备
①称取![]() ,加数滴
,加数滴![]() ,另称取
,另称取![]() ,分别以蒸馏水溶解,将两溶液缓慢混合并加热至沸,搅拌并维持微沸约
,分别以蒸馏水溶解,将两溶液缓慢混合并加热至沸,搅拌并维持微沸约![]() 后停止加热,此时有
后停止加热,此时有![]() 晶体产生,待充分沉降后过滤,以热蒸馏水洗涤沉淀。
晶体产生,待充分沉降后过滤,以热蒸馏水洗涤沉淀。
②称取![]() ,加
,加![]() 蒸馏水,微热使其溶解,将该溶液加至已洗净的
蒸馏水,微热使其溶解,将该溶液加至已洗净的![]() 中,将盛该混合物的容器置于40℃热水中,以滴管缓慢加入约
中,将盛该混合物的容器置于40℃热水中,以滴管缓慢加入约![]() ,边加边搅拌,加完后,需检验
,边加边搅拌,加完后,需检验![]() 是否氧化彻底。
是否氧化彻底。
③在生成![]() 的同时也有
的同时也有![]() 生成,需在微沸情况下补加
生成,需在微沸情况下补加![]() 溶液,将其进一步转化为
溶液,将其进一步转化为![]() 。向所得绿色溶液中加入
。向所得绿色溶液中加入![]() 乙醇,将一小段棉线悬挂在溶液中,一端固定好,盖好烧杯,暗处放置数小时,即有
乙醇,将一小段棉线悬挂在溶液中,一端固定好,盖好烧杯,暗处放置数小时,即有![]() 析出,抽滤,向晶体上滴加少许乙醇,继续抽干,转移至表面皿上,低温干燥
析出,抽滤,向晶体上滴加少许乙醇,继续抽干,转移至表面皿上,低温干燥![]() ,称重,计算产率。
,称重,计算产率。
回答下列问题:
(1)步骤①中加硫酸的作用是___________,如何证明沉淀已洗净________________________。
(2)步骤②中,检验![]() 所用的试剂是______________,不能用酸性
所用的试剂是______________,不能用酸性![]() 溶液检验的理由是_____________________。
溶液检验的理由是_____________________。
(3)写出步骤③中![]() 转化为
转化为![]() 的化学反应方程式_____________。
的化学反应方程式_____________。
Ⅱ.离子交换法测定三草酸合铁(Ⅲ)酸钾中配离子的电荷
原理:利用离子交换树脂对某些离子具有特别的亲和力,当含有这些离子的溶液流过交换树脂时,会吸附在树脂上,树脂上原有的另一类同种电性离子会被溶液带出,从而实现离子的完全交换。
实验步骤:将准确质量的样品溶于水后,使其完全通过![]() 型离子交换树脂,样品中配离子即与氯离子实现交换。
型离子交换树脂,样品中配离子即与氯离子实现交换。
(4)若流出的交换液中![]() ,被交换配离子n(配离子)
,被交换配离子n(配离子)![]() ,则该配离子的负电荷数为___________________。
,则该配离子的负电荷数为___________________。
(5)以沉淀滴定法测定![]() :将流出液稀释至
:将流出液稀释至![]() ,取
,取![]() ,以
,以![]() 为指示剂,用
为指示剂,用![]() 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液![]() 。
。
①溶解度![]() ________
________![]() (填“大于”或“小于”)。
(填“大于”或“小于”)。
②若离子交换步骤称取的样品物质的量为![]() ,该样品中配离子所带的负电荷数为______________。
,该样品中配离子所带的负电荷数为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com