
¡¾̀âÄ¿¡¿2019Äêŵ±´¶û»¯Ñ§½±ÊÚÓèÔ¼º²¡¤¹ÅµẨÁÄÉ·̣¡¢Ë¹̀¹Àû¡¤»ƯÍ¢¶̣Ä·ºÍ¼ª̉°ƠĂÈưλ¿Æѧ¼̉£¬̉Ô±íƠĂËûĂÇÔÚ﮵ç³ØÁ́Ọ́Ëù×ö³öµÄ¾̃´ó¹±Ïס£![]() ¡¢
¡¢![]() ³£ÓĂ×÷ï®Àë×Óµç³ØµÄƠư¼«²ÄÁÏ£¬Çë»Ø´đÏÂÁĐÎỀ⣺
³£ÓĂ×÷ï®Àë×Óµç³ØµÄƠư¼«²ÄÁÏ£¬Çë»Ø´đÏÂÁĐÎỀ⣺
(1)»ù̀¬ï®Ô×ÓµÄ×î¸ßÄܼ¶µÄµç×ÓÔÆĐÎ×´ÊÇ________£»»ù̀¬Á×Ô×ÓÓĐ________¸öδ³É¶Ôµç×Ó£»»ù̀¬̀úÔ×ÓºËÍâµç×ÓÅŲ¼Ê½Îª________¡£
(2)![]() ÖĐ
ÖĐ![]() µÄÅäλÊưΪ4£¬Åä̀åÖĐNµÄÔÓ»¯·½Ê½Îª________£¬¸ĂÅäÀë×ÓÖи÷ÔªËصĵÚ̉»µçÀëÄÜÓÉĐ¡µ½´óµÄ˳Đ̣Ϊ________(ÓĂÔªËØ·ûºÅ±íʾ)¡£
µÄÅäλÊưΪ4£¬Åä̀åÖĐNµÄÔÓ»¯·½Ê½Îª________£¬¸ĂÅäÀë×ÓÖи÷ÔªËصĵÚ̉»µçÀëÄÜÓÉĐ¡µ½´óµÄ˳Đ̣Ϊ________(ÓĂÔªËØ·ûºÅ±íʾ)¡£
(3)![]() ÔÚË®ÖĐ̉×±»»¹Ô³É
ÔÚË®ÖĐ̉×±»»¹Ô³É![]() £¬¶øÔÚ°±Ë®ÖĐ¿ÉÎȶ¨´æÔÚ£¬ÆäỘ̉Ϊ________¡£
£¬¶øÔÚ°±Ë®ÖĐ¿ÉÎȶ¨´æÔÚ£¬ÆäỘ̉Ϊ________¡£
(4)![]() ÊôÓÚ¼̣µ¥Á×ËáÑΣ¬¶øÖ±Á´µÄ¶àÁ×ËáÑÎỘÊÇ̉»ÖÖ¸´ÔÓÁ×ËáÑΣ¬È磺½¹Á×ËáÄÆ¡¢ÈưÁ×ËáÄƵȡ£½¹Á×Ëá¸ùÀë×Ó¡¢ÈưÁ×Ëá¸ùÀë×ÓÈçÏÂͼËùʾ£º
ÊôÓÚ¼̣µ¥Á×ËáÑΣ¬¶øÖ±Á´µÄ¶àÁ×ËáÑÎỘÊÇ̉»ÖÖ¸´ÔÓÁ×ËáÑΣ¬È磺½¹Á×ËáÄÆ¡¢ÈưÁ×ËáÄƵȡ£½¹Á×Ëá¸ùÀë×Ó¡¢ÈưÁ×Ëá¸ùÀë×ÓÈçÏÂͼËùʾ£º

ƠâÀàÁ×Ëá¸ùÀë×ӵĻ¯Ñ§Ê½¿ÉÓĂͨʽ±íʾΪ________(ÓĂn´ú±íPÔ×ÓÊư)¡£
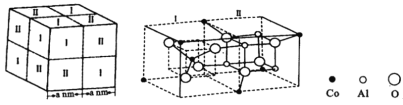
(5)îÜÀ¶¾§̀å½á¹¹ÈçÏÂͼ£¬¸ĂÁ¢·½¾§°ûÓÉ4¸ö¢ñĐͺÍ4¸ö¢̣ĐÍĐ¡Á¢·½̀å¹¹³É¡£¾§̀åÖĐ![]() Ơ¼¾Ư
Ơ¼¾Ư![]() ĐγɵÄ________(̀î¡°ËÄĂæ̀å¿Ơ϶¡±»̣¡°°ËĂæ̀å¿Ơ϶¡±)£»îÜÀ¶¾§̀åµÄĂܶÈΪ___________
ĐγɵÄ________(̀î¡°ËÄĂæ̀å¿Ơ϶¡±»̣¡°°ËĂæ̀å¿Ơ϶¡±)£»îÜÀ¶¾§̀åµÄĂܶÈΪ___________![]() (ÁĐ³ö¼ÆËăʽ£¬ÓĂ
(ÁĐ³ö¼ÆËăʽ£¬ÓĂ![]() ±íʾ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ)¡£
±íʾ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ)¡£
¡¾´đ°¸¡¿Ç̣ĐÎ 3 ![]() £¨»̣
£¨»̣![]() £©
£© ![]()
![]()
![]() ¿ÉÓë
¿ÉÓë![]() ĐγɽÏÎȶ¨µÄÅäºÏÎï
ĐγɽÏÎȶ¨µÄÅäºÏÎï ![]() °ËĂæ̀å¿Ơ϶
°ËĂæ̀å¿Ơ϶ 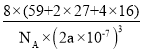
¡¾½âÎö¡¿
(1)ï®ÊÇ3ºÅÔªËØ£¬ºËÍâµç×ÓÅŲ¼Îª1s22s1£¬×î¸ßÄܼ¶ÊÇ2s£¬Æäµç×ÓÔÆĐÎ×´ÊÇÇ̣ĐΣ»Á×ÊÇ15ºÅÔªËØ£¬ºËÍâµç×ÓÅŲ¼Ê½Îª1s22s22p63s23p3£¬Æäδ³É¶Ôµç×ÓÊưÊÇ3pÄܼ¶ÉϵÄ3¸öµç×Ó£»̀úÊÇ26ºÅÔªËØ£¬C¸ù¾ƯºËÍâµç×ÓÅŲ¼¹æÂɿɵĂÆä»ù̀¬̀úÔ×ÓºËÍâµç×ÓÅŲ¼Ê½1s22s22p63s23p63d64s2»̣[Ar]3d64s2£»
¹Ê´đ°¸Îª£ºÇ̣ĐΣ»3£»1s22s22p63s23p63d64s2»̣[Ar]3d64s2£»
(2)NO3£ÖĐ¼Û²ăµç×Ó¶ÔÊưΪ5+0+12=3£¬¹ÊΪsp2ÔÓ»¯£»̉»°ăÇé¿öÏ·ǽđÊôĐÔԽǿµÚ̉»µçÀëÄÜÔ½´ó£¬µ«ÓÉÓÚNÔ×ÓÖĐ×îÍâ²ăΪ°ë³äÂú×´̀¬£¬±È½ÏÎȶ¨£¬¹ÊµÚ̉»µçÀëÄÜ´óÓÚO£¬Ëù̉ÔµÚ̉»µçÀëÄÜÓÉĐ¡µ½´óµÄ˳Đ̣Ϊ![]() £»
£»
¹Ê´đ°¸Îª£ºsp2£»![]() £»
£»
(3)![]() ¿ÉÓë
¿ÉÓë![]() ĐγɽÏÎȶ¨µÄÅäºÏÎ¹Ê
ĐγɽÏÎȶ¨µÄÅäºÏÎ¹Ê![]() ÔÚË®ÖĐ̉×±»»¹Ô³É
ÔÚË®ÖĐ̉×±»»¹Ô³É![]() £¬¶øÔÚ°±Ë®ÖĐ¿ÉÎȶ¨´æÔÚ£»
£¬¶øÔÚ°±Ë®ÖĐ¿ÉÎȶ¨´æÔÚ£»
(4)¿É̉Ô¸ù¾ƯÁ×Ëá¸ù¡¢½¹Á×Ëá¸ù¡¢ÈưÁ×Ëá¸ùµÄ»¯Ñ§Ê½ÍƵ¼£ºPO43-¡¢P2O74-¡¢P3O105-Á×Ô×ӵı仯¹æÂÉΪ£º1¡¢2¡¢3¡¢4£¬nÑơÔ×ӵı仯¹æÂÉΪ£º4¡¢7¡¢10¡¢3n+1Ëá¸ùËù´øµçºÉÊưµÄ±ä»¯¹æÂÉΪ£º3¡¢4¡¢5¡¢n+2£¬ƠâÀàÁ×Ëá¸ùÀë×ӵĻ¯Ñ§Ê½¿ÉÓĂͨʽ![]() À´±íʾ£»
À´±íʾ£»
(5£©¸ù¾ƯîÜÀ¶¾§̀徧°û½á¹¹¹Û²́£¬¾§̀åÖĐAl3+Ơ¼¾ƯO2-ĐγɵİËĂæ̀å¿Ơ϶£»¸Ă¾§°ûµÄ̀å»ưΪ(2a¡Á10-7)3£¬¸Ă¾§°ûµÄÖÊÁ¿Îª32¡Á16+16¡Á27+8¡Á59NA=8(59+2¡Á27+4¡Á16)NA£¬Ëù̉ÔĂܶÈΪ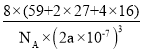 £»
£»
¹Ê´đ°¸Îª£º°ËĂæ̀å¿Ơ϶£»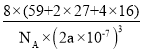 ¡£
¡£



| Ä꼶 | ¸ßÖĐ¿Î³̀ | Ä꼶 | ³ơÖĐ¿Î³̀ |
| ¸ß̉» | ¸ß̉»Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ở» | ³ở»Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ß¶₫ | ¸ß¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ơ¶₫ | ³ơ¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ßÈư | ¸ßÈưĂâ·Ñ¿Î³̀ÍƼö£¡ | ³ơÈư | ³ơÈưĂâ·Ñ¿Î³̀ÍƼö£¡ |
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿2014Äê5ÔÂ7ÈƠ£¬̀́½̣ij¹¤³̀¼́²â¹«Ë¾ÔÚ½øĐĐ̀½ÉË×÷̉µÆڼ䣬̉»Ă¶»Æ¶¹Á£´óĐ¡µÄ·ÅÉäÔ´̉¿-192¶ªÊ§£¬Ố³ÉÁËÑÏÖصݲȫʹʣ¬Í¼Ê¾ÊÇ̉¿ÔÚÔªËØÖÜÆÚ±íÖеÄĐÅÏ¢£¬ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ£¨ £©
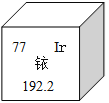
A. ̉¿µÄÏà¶ÔÔ×ÓÖÊÁ¿Îª192.2¿Ë
B. ̉¿Ô×ÓºËÄÚµÄÖĐ×ÓÊưΪ77
C. K2IrO3ÖĐIrµÄ»¯ºÏ¼ÛΪ+4
D. Éú»îÖĐ³£ÓõÄ̉¿½đ±ÊΪ´¿¾»µÄ̉¿µ¥ÖÊ
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿º́·¯ÄÆ£¨ÖظơËáÄÆ£º![]() £©ÊÇÖØ̉ªµÄ»ù±¾»¯¹¤ÔÁÏ£¬Ó¦ÓĂÊ®·Ö¹ă·º¡£¹¤̉µÖƱ¸º́·¯ÄƵÄÁ÷³̀ÈçÏ£º
£©ÊÇÖØ̉ªµÄ»ù±¾»¯¹¤ÔÁÏ£¬Ó¦ÓĂÊ®·Ö¹ă·º¡£¹¤̉µÖƱ¸º́·¯ÄƵÄÁ÷³̀ÈçÏ£º
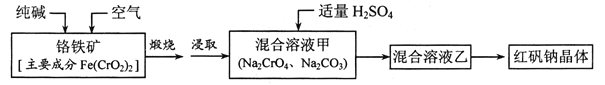
Çë»Ø´đÏÂÁĐÎỀ⣺
(1)![]() µÄ»ù̀¬µç×ÓÅŲ¼Ê½Îª____________¡£
µÄ»ù̀¬µç×ÓÅŲ¼Ê½Îª____________¡£
(2)¶ÍÉƠ¸ờú¿ó·¢Éú·´Ó¦£º____________Fe(CrO2)2+Na2CO3+O2![]() Fe2O3+Na2CrO4+CO2 ÅäƽÉÏÊö»¯Ñ§·´Ó¦·½³̀ʽ¡£
Fe2O3+Na2CrO4+CO2 ÅäƽÉÏÊö»¯Ñ§·´Ó¦·½³̀ʽ¡£
(3)ÈÜ̉º¼×ÖĐ¼ÓÈëH2SO4ʱ£¬¿É̉Ô¹Û²́µ½ÈÜ̉ºÓÉ»ÆÉ«±äΪ³ÈÉ«£¬²¢·Å³öÎ̃É«Æø̀壬ÓĐ¹Ø·´Ó¦µÄÀë×Ó·½³̀ʽΪ____________¡£
(4)ÖƱ¸º́·¯ÄƵķÏË®±ØĐë½øĐĐ´¦Àí¡£Ê×ÏÈËữ·ÏË®£¬½«º¬+6¼Û¸ơµÄËáĐÔ·Ï̉º·ÅÈëµç½â²ÛÄÚ£¬ÓẰú×÷Ñô¼«½øĐеç½â£¬̉ơ¼«Îö³öH2,Ñô¼«²úÎï±»![]() Ñơ»¯È»ºóת»¯ÎªCr(OH)3¡¢ Fe(0H)3 ³Áµí¡£
Ñơ»¯È»ºóת»¯ÎªCr(OH)3¡¢ Fe(0H)3 ³Áµí¡£
¢ÙÑô¼«µÄµç¼«·´Ó¦Ê½Îª£¨²»¿¼ÂǺóĐø·´Ó¦)£º____________¡£
¢ÚÈÜ̉ºÖĐ½đÊôÀë×ÓÔÚ̉ơ¼«Çø¿É³ÁµíÍêÈ«£¬´ÓË®µÄµçÀëƽºâ½Ç¶È½âÊÍÆäỘ̉£º______¡£
¢Û̉Ñ֪ijº¬![]() µÄËáĐÔ·ÏË®ÖĐCrÔªËصĺ¬Á¿ÊÇ52.5mg/L,´¦ÀíºóCrÔªËØ×î¸ßÔÊĐí ÅÅÁ¿Îª0.5 mg/L¡£̉ª´¦Àí100 m3·ÏË®´ïµ½Åŷűê×¼£¬ÖÁÉÙÏûºÄ̀ú_____kg¡£
µÄËáĐÔ·ÏË®ÖĐCrÔªËصĺ¬Á¿ÊÇ52.5mg/L,´¦ÀíºóCrÔªËØ×î¸ßÔÊĐí ÅÅÁ¿Îª0.5 mg/L¡£̉ª´¦Àí100 m3·ÏË®´ïµ½Åŷűê×¼£¬ÖÁÉÙÏûºÄ̀ú_____kg¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Éè![]() Ϊ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ( )¡£
Ϊ°¢·ü¼ÓµÂẪ³£ÊưµÄÖµ¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ( )¡£
A.![]() Óë
Óë![]() µÄ»́ºÏÎº¬Àë×Ó×ÜÊưΪ
µÄ»́ºÏÎº¬Àë×Ó×ÜÊưΪ![]()
B.̉ÑÖª![]() ÖиơÔªËصĻ¯ºÏ¼ÛΪ
ÖиơÔªËصĻ¯ºÏ¼ÛΪ![]() ¼Û£¬Ộ
¼Û£¬Ộ![]() ·Ö×ÓÖĐ´æÔڵĹưÑơ¼üÊưĿΪ
·Ö×ÓÖĐ´æÔڵĹưÑơ¼üÊưĿΪ![]()
C.![]() ÈÜ̉ºÍêÈ«·´Ó¦£¬×ª̉Ƶç×ÓÊưÄ¿̉»¶¨Îª
ÈÜ̉ºÍêÈ«·´Ó¦£¬×ª̉Ƶç×ÓÊưÄ¿̉»¶¨Îª![]()
D.³£ÎÂʱ£¬![]() µÄÑÎËáÖĐË®µçÀëµÄ
µÄÑÎËáÖĐË®µçÀëµÄ![]() ÊưĿΪ
ÊưĿΪ![]()
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Ạ́ËáẰ¾§̀å(![]() )ÊÇÖØ̉ªµÄ΢Á¿ÔªËØ·ÊÁÏÖ®̉»¡£Ä³ĐËÈ¤Đ¡×éÔÚʵÑéỂÖĐ̀½¾¿ÓĂÈíẰ¿ó(Ö÷̉ª³É·ÖΪ
)ÊÇÖØ̉ªµÄ΢Á¿ÔªËØ·ÊÁÏÖ®̉»¡£Ä³ĐËÈ¤Đ¡×éÔÚʵÑéỂÖĐ̀½¾¿ÓĂÈíẰ¿ó(Ö÷̉ª³É·ÖΪ![]() £¬º¬ÓĐÉÙÁ¿
£¬º¬ÓĐÉÙÁ¿![]() ¡¢
¡¢![]() ¡¢
¡¢![]() µÈÔÓÖÊÖÆÈ¡Ạ́ËáẰ¾§̀壬Æä¾ß̀åÁ÷³̀ÈçÏ£º
µÈÔÓÖÊÖÆÈ¡Ạ́ËáẰ¾§̀壬Æä¾ß̀åÁ÷³̀ÈçÏ£º
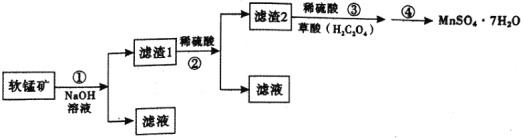
̉ÑÖª£º¢Ù·´Ó¦ÔÀíΪ£º![]() £»
£»
¢Ú![]() ÄÑÈÜÓÚË®¡£
ÄÑÈÜÓÚË®¡£
(1)ÂËÔü2Ö÷̉ª³É·ÖÊÇ![]() £¬²½Öè¢ÚÖеÄÏ¡Ạ́ËáµÄ×÷ÓĂÊÇ________¡£
£¬²½Öè¢ÚÖеÄÏ¡Ạ́ËáµÄ×÷ÓĂÊÇ________¡£
(2)²½Öè¢ÛÖĐ²ÉÓĂ![]() Ạ́ËáºÍ²ƯËᾧ̀åÈܽâ
Ạ́ËáºÍ²ƯËᾧ̀åÈܽâ![]() £¬²ƯËᾧ̀åµÄ×÷ÓĂÊÇ________£»ÅäÖÆ
£¬²ƯËᾧ̀åµÄ×÷ÓĂÊÇ________£»ÅäÖÆ![]() Ạ́Ëáʱ£¬Đè̉ªµÄ̉ÇÆ÷³ưÁ¿Í²¡¢ÉƠ±¡¢²£Á§°ôÍ⣬»¹Đè̉ª________¡£½«ÂËÔü2ÖĂÓÚÉƠ±ÖĐ£¬ÏȼÓÈëÏ¡Ạ́Ëᣬ½«ÈÜ̉ºÉÔ¼ÓÈȺó£¬ÔÚ½Á°èÏ»ºÂư·ÖÅú¼ÓÈë²ƯËᾧ̀壬ֱÖÁÉƠ±ÖĐµÄ¹̀̀åÈ«²¿Èܽ⡣ÔÚ½Á°èÏ»ºÂư·ÖÅú¼ÓÈë²ƯËᾧ̀åµÄÀíÓÉÊÇ________¡£
Ạ́Ëáʱ£¬Đè̉ªµÄ̉ÇÆ÷³ưÁ¿Í²¡¢ÉƠ±¡¢²£Á§°ôÍ⣬»¹Đè̉ª________¡£½«ÂËÔü2ÖĂÓÚÉƠ±ÖĐ£¬ÏȼÓÈëÏ¡Ạ́Ëᣬ½«ÈÜ̉ºÉÔ¼ÓÈȺó£¬ÔÚ½Á°èÏ»ºÂư·ÖÅú¼ÓÈë²ƯËᾧ̀壬ֱÖÁÉƠ±ÖĐµÄ¹̀̀åÈ«²¿Èܽ⡣ÔÚ½Á°èÏ»ºÂư·ÖÅú¼ÓÈë²ƯËᾧ̀åµÄÀíÓÉÊÇ________¡£
(3)²½Öè¢ÜµÄ¾ß̀åʵÑé²Ù×÷ÓĐ________£¬¾Ï´µÓºó¸ÉÔïµĂµ½![]() ¾§̀å¡£
¾§̀å¡£
(4)ĐËÈ¤Đ¡×éͬѧÄâ¼̀ĐøÑĐ¾¿Ạ́ËáẰµÄ¸ßηֽâµÄ¹̀̀å²úÎ¾²é×ÊÁÏ¿ÉÖª£ºẠ́ËáẰ¾§̀å¸ßÎÂÏ·ֽâ²úÎïΪ![]() ¡¢
¡¢![]() ¡¢
¡¢![]() £¬¼°Ë®ƠôÆø¡£ÎªÁËÈ·¶¨
£¬¼°Ë®ƠôÆø¡£ÎªÁËÈ·¶¨![]() µÄ»¯Ñ§Ê½£¬²ÉÓĂÏÂĂæ×°ÖĂ½øĐĐ²â¶¨(̉ÑÖª£º
µÄ»¯Ñ§Ê½£¬²ÉÓĂÏÂĂæ×°ÖĂ½øĐĐ²â¶¨(̉ÑÖª£º![]() µÄÈÛµăΪ16.8¡æ£¬·ĐµăΪ44.8¡æ)¡£
µÄÈÛµăΪ16.8¡æ£¬·ĐµăΪ44.8¡æ)¡£
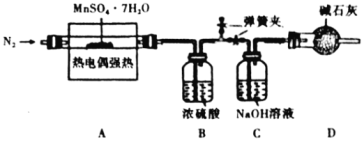
¢Ù![]() ×°ÖĂÖĐÎüÊƠµÄÆø̀åΪ________¡£
×°ÖĂÖĐÎüÊƠµÄÆø̀åΪ________¡£
¢ÚʵÑé×ÔʼÖÁÖƠ¾ùĐèͨÈë![]() £¬ÆäÄ¿µÄÊÇ________¡£
£¬ÆäÄ¿µÄÊÇ________¡£
¢ÛÈôÆđʼʱ£¬ÔÚ×°ÖĂAÖĐ¼ÓÈë![]() £¬³ä·Ö·´Ó¦ºó£¬²âµĂ×°ÖĂCÔöÖØ6.4g£¬Ộ
£¬³ä·Ö·´Ó¦ºó£¬²âµĂ×°ÖĂCÔöÖØ6.4g£¬Ộ![]() µÄ»¯Ñ§Ê½Îª________¡£
µÄ»¯Ñ§Ê½Îª________¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ĐÂĐÍĂ¾ÂÁºÏ½đ£¨Mg17Al12£©ÓĐ´¢ÇâĐÔÄÜ£¬Ëü̉»¶῭ơ¼₫ÏÂÍêÈ«ÎüÇâµÄ·´Ó¦ÎªMg17Al12+17H2¨T17MgH2+12Al£¬µĂµ½µÄ»́ºÏÎïY£¨17MgH2+12Al£©ÄÜÓëËá·´Ó¦Êͷųö´óÁ¿ÇâÆø£®ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A. ¸ĂºÏ½đÓ¦ÔÚµªÆø±£»¤Ï£¬½«̉»¶¨±ÈÀưµÄMg¡¢Alµ¥ÖÊÈÛÁ¶¶ø³É
B. ºÏ½đÔÚÎüÇâ¹ư³̀Öб»H2»¹Ô
C. ̉»¶¨Á¿µÄĂ¾ÂÁºÏ½đ¼È¿É̉ÔÍêÈ«ÈÜÓÚ×ăÁ¿ÑÎËáÖĐ£¬̉²¿É̉ÔÍêÈ«ÈÜÓÚ×ăÁ¿µÄNaOHÈÜ̉ºÖĐ
D. µÈÖÊÁ¿µÄĂ¾¡¢ÂÁ¡¢ºÍĂ¾ÂÁºÏ½đ·Ö±đÓë×ăÁ¿µÄÑÎËá·´Ó¦Éú³ÉH2µÄ̀å»ư£¨Í¬ÎÂͬѹÏ£©ÓÉ´óµ½Đ¡µÄ˳Đ̣Ϊ£ºV(Mg)£¾ V(ºÏ½đ)£¾V(ÂÁ)
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ÊµÑéỂĐè̉ª95 mL l.0 mol/LÏ¡Ạ́ËᣬÏÖÓĂ98%µÄŨẠ́Ëá(ÆäĂܶÈΪ1.84 g.mL-l)À´ÅäÖÆ¡£
(1)ʵÑéĐè̉ªµÄ²£Á§̉ÇÆ÷ÓĐ50 mLÉƠ±¡¢²£Á§°ô¡¢½ºÍ·µÎ¹Ü¡¢____¡¢____¡£
(2)²£Á§°ôµÄ×÷ÓĂΪ____£¬½ºÍ·µÎ¹ÜµÄ×÷ÓĂΪ________£¬
(3)ÅäÖƹư³̀ÖĐ£¬ÏÂÁĐÇé¿ö»áʹÅäÖƽá¹ûÆ«µÍµÄÊÇ(̀îĐ̣ºÅ)____¡£
A.½«Ï¡Ê͵ÄẠ́Ëá̉º×ª̉ÆÖÁÈƯÁ¿Æ¿ºó£¬Ï´µÓÉƠ±ºÍ²£Á§°ô2-3´Î¡£
B.½«ÉƠ±ÄÚµÄÏ¡Ạ́ËáỊ̈ÈƯÁ¿Æ¿ÖĐת̉Æʱ£¬̣̉²Ù×÷²»µ±Ê¹²¿·ÖÏ¡Ạ́Ëὦ³öÆ¿Íâ¡£
C.ÈƯÁ¿Æ¿Ê¹ÓĂʱδ¸ÉÔï¡£
D.ÓĂ½ºÍ·µÎ¹Ü¼Óˮʱ£¬ÑöÊÓ¹Û²́ÈÜ̉º°¼̉ºĂæÓëÈƯÁ¿Æ¿¿̀¶ÈÏàÇĐ¡£
E.δÀäÈ´ÖÁỂξͶ¨ÈƯ¡£
F.¶¨ÈƯºó¾Ơñµ´¡¢̉¡ÔÈ¡¢¾²ÖĂ£¬·¢ÏÖ̉ºĂæµÍÓÚ¿̀¶ÈÏߣ¬ÔÙ¼ÓƠôÁóË®²¹ÖÁ¿̀¶ÈÏß¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿¸ß¯Á¶̀úÊÇÏÖ´ú¸Ö̀úÉú²úµÄÖØ̉ª»·½Ú£¬´Ë·¨¹¤̉Ơ¼̣µ¥£¬²úÁ¿´ó£¬Äܺĵͣ¬ÈÔÊÇÏÖ´úÁ¶̀úµÄÖ÷̉ª·½·¨£¬»Ø´đÏÂÁĐÎỀ⣺
(1)̉ÑÖªÁ¶̀ú¹ư³̀µÄÖ÷̉ª·´Ó¦ÎªFe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ¡÷H1
»¹»á·¢Éú3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ¡÷H2=a kJ/mol£»
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ¡÷H3=b kJ/mol£»
FeO(s)+CO(g)=Fe(s)+ CO2(g) ¡÷H4=c kJ/mol£»
Ộ¡÷H1=________kJ/mol£¨ÓĂº¬a¡¢b¡¢cµÄ´úÊưʽ±íʾ£©¡£
(2)¸ß¯Á¶̀ú²úÉúµÄ·ÏÆø(CO¡¢CO2)ÓжàÖÖ´¦Àí·½·¨£¬·´Ó¦ÔÀíÈçÏ£º
¢ÙÉú³É¼×´¼£ºCO(g)+2H2(g)![]() CH3OH(l)¡£̉»¶¨Î¶ÈÏÂÔÚºăÈƯĂܱƠÈƯÆ÷ÖĐÄ£Äâ´Ë·´Ó¦£¬ÏÂÁĐ»¯Ñ§·´Ó¦ËÙÂÊ×î¿́µÄÊÇ_______________
CH3OH(l)¡£̉»¶¨Î¶ÈÏÂÔÚºăÈƯĂܱƠÈƯÆ÷ÖĐÄ£Äâ´Ë·´Ó¦£¬ÏÂÁĐ»¯Ñ§·´Ó¦ËÙÂÊ×î¿́µÄÊÇ_______________
A£®¦Ô(CO)=1.2 mol/(L¡¤min) B£®¦Ô(H2)=0.025 mol/(L¡¤s) C£®¦Ô(CH3OH)=1 mol/(L¡¤min)
¢ÚÉú³É̉̉Ï©£º2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g)¡£ÔÚÁ½¸öÈƯ»ưÏàͬµÄĂܱƠÈƯÆ÷ÖĐ̉Ô²»Í¬µÄÇầ¼±È[n(H2)£ºn(CO2)]³äÈëÔÁÏÆø£¬CO2ƽºâת»¯ÂʦÁ(CO2)ÓëζȵĹØϵÈçͼËùʾ
C2H4(g)+4H2O(g)¡£ÔÚÁ½¸öÈƯ»ưÏàͬµÄĂܱƠÈƯÆ÷ÖĐ̉Ô²»Í¬µÄÇầ¼±È[n(H2)£ºn(CO2)]³äÈëÔÁÏÆø£¬CO2ƽºâת»¯ÂʦÁ(CO2)ÓëζȵĹØϵÈçͼËùʾ
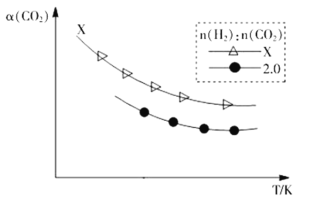
Çầ¼±ÈX_____2.0£῭¡¢£¼»̣£½£¬ÏÂͬ£©£¬ÀíÓÉÊÇ___________________¡£
(3)·´Ó¦CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)£¬Æ仯ѧƽºâ³£ÊưKÓëζÈT¹ØϵÈç±í£º
CH3OH(g)+H2O(g)£¬Æ仯ѧƽºâ³£ÊưKÓëζÈT¹ØϵÈç±í£º
T/¡æ | 700 | 800 | 1000 | 1200 |
K | 0.6 | 1.0 | 2.3 | 3.6 |
¢Ù¸Ă·´Ó¦ÊÇ___________·´Ó¦(̀î¡°ÎüÈÈ¡±»̣¡°·ÅÈÈ¡±)¡£
¢ÚÈôijºă¶¨Î¶ÈÏ£¬Ị̈ÈƯ»ưΪ1 LµÄºăÈƯĂܱƠÈƯÆ÷ÖĐ³äÈë2 mol CO2¡¢3 mol H2£¬10 minºó·´Ó¦´ïµ½Æ½ºâ×´̀¬£¬²âµĂ¦Ô (CH3OH)=0.075 mol/(L¡¤min)£¬Ộ´Ë·´Ó¦̀ơ¼₫ÏÂζÈ______800¡æ£῭¡¢£¼»̣£½£©¡£
¢ÛÈô·´Ó¦ÔÚ1200¡æ½øĐĐÊÔÑ飬ijʱ¿̀²âµĂ·´Ó¦ÈƯÆ÷Öи÷ÎïÖÊŨ¶ÈÂú×ă¹Øϵʽ2c(CO2)¡¤c3(H2)=3c(CH3OH)¡¤c(H2O)£¬´Ëʱ·´Ó¦ÔÚ________Ị̈½øĐĐ£῭î¡°Ơư¡±»̣¡°Ä桱£©¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Èôº¬ÓĐ1 mol̀úÀë×ÓºÍ1 molÂÁÀë×ӵĻ́ºÏÈÜ̉º£¬ÏÖ°´ÏÂͼºá×ø±ểÀ´Î¼ÓÈë8 mol ÇâÑơ»¯ÄÆÈÜ̉º¡¢1 molÑÎËᣬͨÈë1 mol ¶₫Ñơ»¯̀¼Æø̀壬×Ư×ø±êΪ»́ºÏ³ÁµíµÄÎïÖʵÄÁ¿¡£

(1)Ç뻳ö³ÁµíµÄÁ¿Ëæ·´Ó¦µÄ±ä»¯ÇúÏß______________¡£
(2)²¢Đ´³ö¼ÓÈëÇâÑơ»¯ÄÆ6 mol¼°Æäºó·¢ÉúµÄ¸÷²½·´Ó¦µÄÀë×Ó·½³̀ʽ______________¡£
²é¿´´đ°¸ºÍ½âÎö>>
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com