
T ℃时,将6 mol CO2和8 mol H2充入2 L密闭容器中,发生反应CO2(g)+3H2(g)  CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
A.反应开始至a点时v(H2)=1 mol·L-1·min-1
B.若曲线Ⅰ对应的条件改变是升温,
则该反应H>0
C.曲线Ⅱ对应的条件改变是降低压强
D.T ℃时,该反应的化学平衡常数为0.125
【知识点】化学平衡移动、影响因素、平衡常数的计算
【答案解析】A
解析:A、a点时t=1min,n(H2)=6mol,则△n(H2)=8-6=2mol, △C(H2)=1mol/L,v(H2)= △C(H2)/t=1 mol·L-1·min-1 ;B、升高温度,平衡时氢气的量增大,说明是逆向移动,则该反应H<0,故B错误;C、曲线Ⅱ达平衡时所需时间少,平衡时氢气的量减小,改变的条件应该是增大二氧化碳的浓度或增大压强,故C错误;D、根据反应结合图像:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
C(始) 3 4 0 0
△C 1 3 1 1
C(平) 2 1 1 1
K=C(CH3OH)C(H2O)/C(CO2)C3(H2)=0.5 故D错误;
故答案选A
【思路点拨】本题考查化学反应速率计算、化学平衡的影响因素,运用勒夏特列原理分析平衡移动,图像遵循“先拐先平,条件高”原则分析条件的变化。


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案科目:高中化学 来源: 题型:
在一固定体积的密闭容器中,可逆反应,nA(g)+mB (g)  pC(g)已经达到平衡状态。已知n+m>p,正反应为放热反应。下列分析结论中正确的是
pC(g)已经达到平衡状态。已知n+m>p,正反应为放热反应。下列分析结论中正确的是
①升温,c(B)/c(C)的值变小;②降温,平衡体系内混合气体的平均相对分子质量变小;
③增加B的物质的量,A的转化率增大;④使用催化剂,气体总的物质的量不变;
⑤加压使密闭容器的容积变小,A或B的浓度则变大;
⑥若A的反应速率为v(A),则v(B)= n /m [v(A)]
A.①② B.②③④ C.③④⑤ D.③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后得到密度为1.17 g·cm-3的溶液。请计算:
①混合后的溶液中NaCl的质量分数是多少?
②混合后的溶液的物质的量浓度为多少?
(2)在标准状况下,1 L水溶解了一定体积的NH3,所得溶液的密度为ρ g·cm-3,物质的量浓度为a mol·L-,则所溶解的NH3的体积为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A、高温下FeSO4发生如下反应:2FeSO4高温Fe2O3+SO2↑+SO3↑,将生成的气体通入氯化钡溶液中,得到的沉淀物是BaSO3和BaSO4
B、浅绿色的Fe(NO3)2溶液中存在着如下的平衡:Fe2++2H2O Fe(OH)2+2H+
Fe(OH)2+2H+
若在此溶液中加入盐酸,则Fe2+浓度增大
C、在铁和铜的混合物中,加入不足量的稀硝酸,反应后剩余金属m1g;再向其中加入一定量的稀硫酸,充分振荡后 ,剩余金属m2g,则m1大于等于m2
D、实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取的Na2CO3质量分别为1000mL , 212.0g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关有机物的说法正确的是( )
A.甲烷、乙烯和苯在工业上都可通过石油分馏得到。
B.米酒变酸的过程涉及了氧化反应。
C.乙烯和聚丙烯都能与氢气在一定条件下发生加成反应。
D.淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【[化学—有机化学基础】没食子酸丙酯简称PG,结构简式为 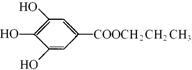 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
⑴PG的分子式为 ,请写出PG分子中所含官能团的名称 ,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是 。
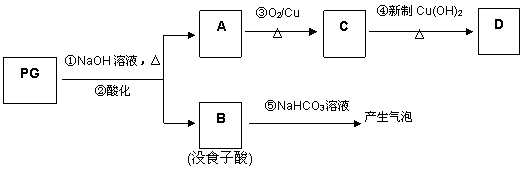 PG可发生如下转化:
PG可发生如下转化:
⑵A的结构简式为 ,1mol没食子酸最多可与 mol H2 加成。
⑶上图的有关变化中,属于氧化反应的有(填序号) 。
⑷从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号) 。
a.含有苯环 b.含有羧基 c.含有酚羟基 d. 微溶于食用油
⑸反应④的化学方程式为:
⑹B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式:
i.含有苯环,且苯环上的一溴代物只有一种;ii.既能发生银镜反应,又能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属的冶炼,叙述错误的是( )
|
| A. | 活泼金属钠用电解法冶炼 | B. | 用火法或湿法均可制备铜 |
|
| C. | 金属镁只能用热还原法制备 | D. | 铁的冶炼可以用铝热法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
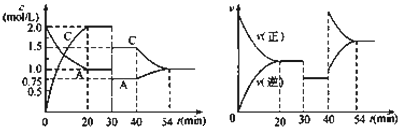
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)⇌2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如图所示.下列说法中正确是( )
|
| A. | 30 min~40 min间该反应使用了催化剂 |
|
| B. | 反应方程式中的x=1,正反应为吸热反应 |
|
| C. | 30~40min改变的条件是将容器的体积扩大至原来的2倍 |
|
| D. | 在25min、35min、55min时化学平衡常数分别为K1、K2、K3,则K1=K2>K3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
NaCl是一种化工原料,可以制备一系列物质(见下图)。下列说法正确的是( )
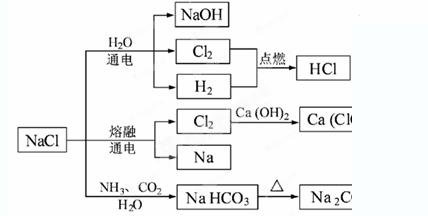
A.25℃,NaHCO3在水中的溶解度比Na2CO3的大
B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂
C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D.图4所示转化反应都是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com