
【题目】德国化学家凯库勒认为:苯分子是由6个碳原子以单双键相互交替结合而成的环状结构为了验证凯库勒有关苯环的观点,甲同学设计了如图实验方案.

①按如图所示的装置图连接好各仪器;②检验装置的气密性;③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压預先装有水的胶头滴管的胶头,观察实验现象.
请回答下列问题.
(1)A中所发生反应的反应方程式为_____,能证明凯库勒观点错误的实验现象是______.
(2)装置B的作用是______.
(3)C中烧瓶的容积为500mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对氢气的相对密度为35.3,则实验结束时,进入烧瓶中的水的体积为______mL 空气的平均相对分子质量为29.
(4)已知乳酸的结构简式为![]() 试回答:
试回答:
①乳酸分子中含有______和______两种官能团写名称.
②乳酸跟氢氧化钠溶液反应的化学方程式:______.
【答案】.![]() ; 烧瓶中产生“喷泉”现象 除去未反应的苯蒸气和溴蒸气 400 羟基 羧基 CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O
; 烧瓶中产生“喷泉”现象 除去未反应的苯蒸气和溴蒸气 400 羟基 羧基 CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O
【解析】
(1)苯与溴在溴化铁做催化剂的条件下生成溴苯和溴化氢,苯分子里的氢原子被溴原子所代替,
方程式为:![]() ,该反应为取代反应,不是加成反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象;
,该反应为取代反应,不是加成反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象;
(2)因为反应放热,苯和液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳除去溴化氢气体中的溴蒸气和苯,以防干扰检验HBr;
(3)烧瓶中混合气体对氢气的相对密度为35.3,故烧瓶中混合气体的平均分子量为35.3×2=70.6,
设HBr的体积为x,空气的体积为y,则:81×x/500+29×y/500=70.6;x+y=500,计算得出:x=400mL,y=100mL,所以进入烧瓶中的水的体积为400mL;
(4)①乳酸分子中含羟基(-OH)和羧基(-COOH);
②羧基与氢氧根发生中和反应,反应方程式为:CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O。


科目:高中化学 来源: 题型:
【题目】一种有效治疗关节炎、脊椎炎等一些疾病的常用药物-菲诺洛芬钙,它的一种合成路线如下(具体反应条件和部分试剂略)

已知:①SOCl2可与醇发生反应,醇的羟基被氯原子取代而生成氯化烃
②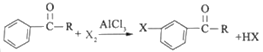 (X表示卤素原子)
(X表示卤素原子)
③R-X+NaCN![]() RCN+NaX
RCN+NaX
回答下列问题:
(1)B→C的反应类型是___________;写出D的结构简式:___________。
(2)F中所含的官能团名称是______________________。
(3)写出F和C在浓硫酸条件下反应的化学方程式______________________。
(4)A的同分异构体中符合以下条件的有___________种(不考虑立体异构)
①属于苯的二取代物; ②与FeCl3溶液发生显色反应。
其中核磁共振氢谱图中共有4个吸收峰的分子的结构简式为___________。
(5)结合上述推断及所学知识,参照上述合成路线任选无机试剂设计合理的方案,以苯甲醇(![]() )为原料合成苯乙酸苯甲酯(
)为原料合成苯乙酸苯甲酯(![]() )写出合成路线______________________,并注明反应条件。
)写出合成路线______________________,并注明反应条件。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)下列说法正确是( )
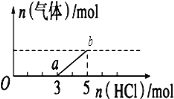
A.oa段反应的离子方程式为:H++OH-=H2O
B.O点溶液中所含溶质的化学式为NaHCO3、Na2CO3
C.标准状况下,通入CO2的体积为4.48L
D.原NaOH溶液的物质的量浓度为2.5molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将8.00gCuO和Fe2O3的混合物分成两等份,其中一份在高温下用足量CO还原后,剩余固体质量为2.88g;另一份固体用200mL某浓度的盐酸恰好溶解,则:
(1)混合物中CuO和Fe2O3的物质的量之比为:________________________
(2)所用盐酸的物质的量浓度为_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的热现象说法不正确的是( )
①放热反应发生时不必加热 ②化学反应一定有能量变化
③吸热反应需要加热后才能发生
④化学反应吸收或放出热量的多少与参加反应的物质多少有关
A.①②B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个1L的密闭容器中加2molA和1molB发生反应: 2A(g)+B(g)![]() 3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是
3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是
A. 6mol C+2mol D B. 4mol A+2mol B
C. 1mol A+0.5mol B+1.5mol C D. 3mol C+5mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,含有以下离子中的若干种:Na+、NH4+、Clˉ、Ba2+、CO32ˉ、SO42ˉ,现取两份 100 m L的该溶液进行如下实验:
(1)第1份加足量NaOH溶液,加热,收集到标准状况下的气体448mL;
(2)第2份加足量Ba(OH)2溶液,得沉淀4.30 g,再用足量盐酸洗涤、干燥,得沉淀2.33 g。
根据上述实验,下列推测正确的是( )
A.Ba2+一定存在B.100 mL该溶液中含0.01 molCO32ˉ
C.Na+不一定存在D.Clˉ不确定,可向原溶液中加入AgNO3溶液进行检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在科学研究和化工生产等领域都有着广泛的应用。请回答下列问题:
(1)与氮元素同族的第四周期元素的基态原子价层电子轨道表达式为___________。
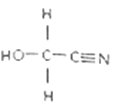
(2)HOCH2CN的结构简式如图,该分子中σ键与π键数目之比为___________,其分子中碳原子的杂化方式为___________,该物质中除氢以外的元素的第一电离能由大到小的顺序为______________________。
(3)[Cu(NH3)4]SO4是一种重要的配合物。与SO42-互为等电子体的分子的化学式为___________(任写一种)。NH3的 VSEPR模型为___________。[Cu(NH3)4]2+的结构可用示意图表示为______________________。
(4)①已知:2UO2+5NH4HF2![]() 2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为___________(填选项字母)。
2UF4·NH4F+3NH3↑+4H2O↑,NH4HF2中不含有的作用力为___________(填选项字母)。
A.共价键 B.配位键 C.金属键 D.离子键 E.氢键
②NH3和H2O的键角由大到小的顺序为______________________(用分子式表示),原因是_______________________________________________________。
(5)Cu3N的晶胞结构如图所示,N3-的配位数为___________,Cu+半径为apm,N3-的半径为bpm,Cu3N晶胞的密度为___________g/cm3(列出计算式即可,阿伏加德罗常数的值用NA表示)。
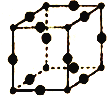
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com