
【题目】钼![]() 是一种重要的过渡金属元素,工业上由钼精矿
是一种重要的过渡金属元素,工业上由钼精矿![]() 主要成分是
主要成分是![]() 制备单质钼和钼酸钠晶体
制备单质钼和钼酸钠晶体![]() 的流程如下:
的流程如下:

![]() 中Mo元素的化合价为______;钼精矿焙烧的主要反应中,氧化剂和还原剂物质的量之比为______。
中Mo元素的化合价为______;钼精矿焙烧的主要反应中,氧化剂和还原剂物质的量之比为______。
![]() 流程中由
流程中由![]() 溶液获得晶体的操作是______、过滤、洗涤、干燥。加入
溶液获得晶体的操作是______、过滤、洗涤、干燥。加入![]() 溶浸时发生的主要反应的离子方程式为______。
溶浸时发生的主要反应的离子方程式为______。
![]() 操作1中,所得
操作1中,所得![]() 溶液中含
溶液中含![]() 杂质,其中
杂质,其中![]() ,
,![]() ,在结晶前需加入
,在结晶前需加入![]() 固体以除去溶液中的。当
固体以除去溶液中的。当![]() 开始沉淀时,
开始沉淀时,![]() 的去除率是______。
的去除率是______。![]() 、
、![]()
![]() ,溶液体积变化可忽略
,溶液体积变化可忽略![]()
![]() 工业上钼精矿在酸性条件下,加入
工业上钼精矿在酸性条件下,加入![]() 溶液,也可以制备钼酸钠,该法的优点是______。
溶液,也可以制备钼酸钠,该法的优点是______。
![]() 高纯Mo可用于制造电池级
高纯Mo可用于制造电池级![]() ,
,![]() 电池是一种性能优异的二次电池,其电池反应为:
电池是一种性能优异的二次电池,其电池反应为:![]()
![]()
![]() 该电池放电时正极反应为______;充电时
该电池放电时正极反应为______;充电时![]() 移动方向为______
移动方向为______![]() 填“由阳极移向阴极”或“由阴极移向阳极”
填“由阳极移向阴极”或“由阴极移向阳极”![]() 。
。
【答案】![]() 7:2 蒸发浓缩、冷却结晶
7:2 蒸发浓缩、冷却结晶 ![]()
![]() 工艺简单
工艺简单![]() 或能耗低,节约能源
或能耗低,节约能源![]()
![]() 由阳极移向阴极
由阳极移向阴极
【解析】
灼烧钼精矿,![]() 燃烧,反应方程式为
燃烧,反应方程式为![]() ,碱性条件下,
,碱性条件下,![]() 和
和![]() 溶液反应,反应方程式为
溶液反应,反应方程式为![]() ,溶液中的溶质为
,溶液中的溶质为![]() ,将溶液蒸发浓缩、冷却结晶,然后重结晶得到
,将溶液蒸发浓缩、冷却结晶,然后重结晶得到![]() ,
,![]() 与足量盐酸反应生成钼酸,高温灼烧钼酸生成
与足量盐酸反应生成钼酸,高温灼烧钼酸生成![]() ,氢气还原
,氢气还原![]() 得到Mo,以此来解答。
得到Mo,以此来解答。
![]() 中Mo元素的化合价为
中Mo元素的化合价为![]() ;钼精矿焙烧发生
;钼精矿焙烧发生![]() ,氧化剂
,氧化剂![]() 和还原剂(
和还原剂(![]() )物质的量之比为7:2,
)物质的量之比为7:2,
故答案为:![]() ;7:2;
;7:2;
![]() 流程中由
流程中由![]() 溶液获得晶体的操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥。加入
溶液获得晶体的操作是蒸发浓缩、冷却结晶、过滤、洗涤、干燥。加入![]() 溶浸时发生的主要反应的离子方程式为
溶浸时发生的主要反应的离子方程式为![]() ,
,
故答案为:蒸发浓缩、冷却结晶;![]() ;
;
![]() ,
,![]() ,当
,当![]() 开始沉淀时,
开始沉淀时,![]() ,此时
,此时![]() ,
,![]() 的去除率
的去除率![]() ,
,
故答案为:![]() ;
;
![]() 工业上钼精矿在酸性条件下,加入
工业上钼精矿在酸性条件下,加入![]() 溶液,也可以制备钼酸钠,该法的优点是工艺简单
溶液,也可以制备钼酸钠,该法的优点是工艺简单![]() 或能耗低,节约能源
或能耗低,节约能源![]() ,
,
故答案为:工艺简单![]() 或能耗低,节约能源
或能耗低,节约能源![]() ;
;
![]() 高纯Mo可用于制造电池级
高纯Mo可用于制造电池级![]() ,
,![]() 电池是一种性能优异的二次电池,其电池反应为:
电池是一种性能优异的二次电池,其电池反应为:![]()
![]()
![]() 。该电池放电时正极反应为
。该电池放电时正极反应为![]() ;充电时
;充电时![]() 移动方向为由阳极移向阴极,
移动方向为由阳极移向阴极,
故答案为:![]() ;由阳极移向阴极。
;由阳极移向阴极。


科目:高中化学 来源: 题型:
【题目】硼镁矿属于硼酸盐,可用来制备硼酸(H3BO3)和MgO,方法如下:硼镁矿粉与(NH4)2SO4溶液混合后加热,反应生成H3BO3晶体和MgSO4溶液,同时放出NH3;再向MgSO4溶液中通入NH3与CO2,得到MgCO3沉淀和滤液,沉淀经洗涤、煅烧后得MgO,滤液则循环使用。回答下列问题:
(1)与硅酸盐类似,硼酸盐结构也比较复杂,如硬硼钙石化学式为Ca2B6O11·5H2O,将其改写为氧化物的形式_____________________________。
(2)上述制备过程中,检验沉淀洗涤是否完全的方法是_______________________。
(3)写出MgSO4溶液中通入NH3与CO2反应的化学方程式_______________________。
(4)若准确称取1.68 g硼镁矿,完全反应后得H3BO3晶体1.24 g,MgO 0.8 g,计算该硼酸盐的组成。(写出计算过程)___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的化学元素,图1是某化工厂从海水中提取![]() 、
、![]() (海水中以
(海水中以![]() 形式存在)、
形式存在)、![]() (海水中以
(海水中以![]() 形式存在)等物质的生产流程简图:
形式存在)等物质的生产流程简图:
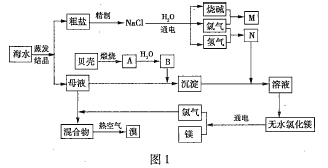
(1)![]() 中加入盐酸后,要获得
中加入盐酸后,要获得![]() 晶体,需要进行的实验操作依次为________(填序号)。
晶体,需要进行的实验操作依次为________(填序号)。
A 蒸馏 B 灼烧 C 过滤 D 蒸发 E 冷却结晶
(2)利用![]() 可制得无水氯化镁,应采取的措施是__________。
可制得无水氯化镁,应采取的措施是__________。
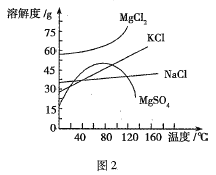
(3)母液中常含有![]() 、
、![]() 、
、![]() 、
、![]() (各物质的溶解度曲线如图2所示)等,进一步加工可制得一些重要的产品。若将母液加热到60℃以上,随着水分的蒸发,会逐渐析出晶体,该晶体的主要成分有________、________;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的________晶体。
(各物质的溶解度曲线如图2所示)等,进一步加工可制得一些重要的产品。若将母液加热到60℃以上,随着水分的蒸发,会逐渐析出晶体,该晶体的主要成分有________、________;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的________晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色) ![]() 2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
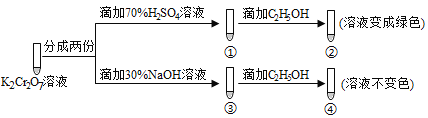
A. ①中溶液橙色加深,③中溶液变黄 B. ②中Cr2O72-被C2H5OH还原
C. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 D. 对比②和④可知K2Cr2O7酸性溶液氧化性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知![]() ,下列有关叙述错误的是( )
,下列有关叙述错误的是( )

A.HA、HB两种酸中,HB的酸性弱于HA
B.b点时,![]()
C.同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.实验室将少量Na保存在乙醇中
B.可用激光笔鉴别FeCl3溶液和Fe(OH)3胶体
C.32 g O3中含有的氧原子数约是3×6.02×1023
D.常温下,可以用铝制容器来储运浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 0.18 mol·L-1 D. 0.24 mol·L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式见下图,取足量的Na、NaOH溶液和NaHCO3溶液分别和等物质的量的该物质在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和NaHCO3三物质的物质的量之比

A.3∶4∶2B.3∶5∶2
C.3∶5∶1D.3∶4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于σ键和π键的理解不正确的是( )
A.σ键可以绕键轴旋转,π键不能绕键轴旋转
B.H2分子中的σ键是s-s σ键,HClO分子中的σ键都是p-pσ键
C.C2H4分子和N2H4中都是含有5个σ键
D.σ键以“头碰头”方式重叠,π键以“肩并肩”方式重叠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com