
����Ŀ���ҹ��Ǹ�ũҵ�����ũҵ������֮����������ũҩ�ķ�չ��ũҵ���ž���ƶ����á���ش��������⣺
(1)ũ�������������в���ȱ�ٵ���Ԫ����![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() �ȣ����ǻ���ø����ɳɷ֣��������ø�Ļ��ԣ���ũ��������Ӫ�������γɺ��³´�л����ȱ�ٵ�Ԫ�ء�����ͭ���ǵ��������μ�أ�����
�ȣ����ǻ���ø����ɳɷ֣��������ø�Ļ��ԣ���ũ��������Ӫ�������γɺ��³´�л����ȱ�ٵ�Ԫ�ء�����ͭ���ǵ��������μ�أ�����![]() ��ʩ�õ���ʱ�˽���Һ_____________�������ҶƬ�ϡ�����ˮ���������С�����ԭ����_______________________��
��ʩ�õ���ʱ�˽���Һ_____________�������ҶƬ�ϡ�����ˮ���������С�����ԭ����_______________________��
(2)ũҩ������Һ��һ�ֳ��õ�ɱ�����������䷽Ϊ����ͭ����ʯ�ҡ�ˮ�����߰�һ�������Ȼ�ϣ���������β��溦��ԭ��________________��
���𰸡�����ҶƬ�� ![]() �ڼ������������ɲ����ũ��������������� ������Һ������������ͷų�
�ڼ������������ɲ����ũ��������������� ������Һ������������ͷų�![]() ��
��![]() ��ʹ���嵰���ʱ���
��ʹ���嵰���ʱ���
��������
��1���ڼ��������У�����Cu2������������ʽ�����ɲ��ױ�ũ�������յIJ���������˽�������![]() ����Һ��ʩ��ũ����ҶƬ�ϣ��ʴ�Ϊ������ҶƬ�ϣ�Cu2���ڼ������������ɲ����ũ��������������գ�
����Һ��ʩ��ũ����ҶƬ�ϣ��ʴ�Ϊ������ҶƬ�ϣ�Cu2���ڼ������������ɲ����ũ��������������գ�
��2��������Һ��ũ������������������ͷų�Cu2����Cu2��Ϊ�ؽ������ӣ�����ʹϸ���ĵ����ʱ��ԣ����ﵽɱ��Ч�����ʴ�Ϊ��������Һ������������ͷų�Cu2����Cu2����ʹ���嵰���ʱ��ԡ�


 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ�ݻ�Ϊ2L�ĺ����ܱ������г���2molA��3molB����һ�������·�Ӧ��A��g��+B��g��C��g������H >0���ﵽƽ���������ѹǿ�ǿ�ʼʱ��84����������ij�ִ�����Ӧ�������仯��ͼ��ʾ������˵����ȷ���ǣ� ��

A.��ͼ��֪���������֮��ԭ��Ӧ�ֳ�����������һ����Ӧ����
B.��40s��ﵽƽ�⣬����A��ʾ�÷�Ӧ������Ϊ0.01molL-1min-1
C.������c(B)/c(A)���ٸı�ʱ������˵���÷�Ӧ�ﵽ��ƽ��״̬
D.�ﵽƽ��ʱ��C���������ԼΪ25��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������(Na2S2O3)����Ҫ�Ļ���ԭ�ϡ����н�ǿ�Ļ�ԭ�ԣ���������֯��Ư������ȼ������������еĻ�ԭ����������ˮ���������Ҵ���Na2S2O35H2O��40��45���ۻ���48��ֽ⡣ʵ�����г����������ƺ�����Ʊ�Na2S2O35H2O���Ʊ�ԭ��Ϊ��Na2SO3+S+5H2O�TNa2S2O35H2O��ij��ѧ��ȤС����ʵ�����Ʊ���������ƾ��岢̽���仯ѧ���ʡ�
��.ʵ������ȡNa2S2O35H2O����IJ������£�
�ٳ�ȡ12.6 g Na2SO3���ձ��У�����80.0 mLˮ��
����ȡ4.0 g��ۣ��������Ҵ���ʪ�ӵ�������Һ�С�
��ˮԡ����(��ͼ1��ʾ������װ����ȥ)���У���ӦԼ1Сʱ����ˡ�
����Һ�ھ�������Ũ������ȴ�ᾧ������Na2S2O35H2O���塣
�ݽ��м�ѹ����(��ͼ2��ʾ)���Ҵ�ϴ�Ӳ������ش�
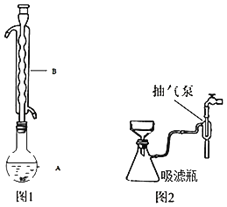
(1)����B��������_____��
(2)�������Ũ�������в����������ȣ���ԭ����_____�����������ֹͣ���ˣ�Ӧ�Ƚ�����ƿ֧���ϵ���Ƥ�ܰ��£��ٹس����ã���ԭ����_____��
(3)ϴ��ʱΪ�����ܱ����Ʒ��ʧӦѡ�õ��Լ���_____��
A.ˮ B.�Ҵ� C.����������Һ D.ϡ����
��.�������ʵ������̽��Na2S2O3��ijЩ��ѧ����
![]()
(4)ʵ���Na2S2O3��ҺpH��8��ԭ����_____(�����ӷ���ʽ��ʾ)��
(5)д��ʵ����з��������ӷ�Ӧ����ʽ_____��
��.��Na2S2O3����Һ�ⶨ��Һ��ClO2�����ʵ���Ũ�ȣ��ɽ�������ʵ�顣
����1��ȷ��ȡClO2��Һ10.00mL��ϡ�ͳ�100mL������
����2����ȡV1 ML�������뵽��ƿ�У�����������pH��2.0������������KI���壬ҡ�ȣ��ڰ�������30����(��֪��ClO2+I��+H+��I2+Cl��+H2O δ��ƽ)��
����3���Ե�����Һ��ָʾ������c mol/L Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2 mL(��֪��I2+2S2O32��=2I��+S4O62��)��
(6)�ζ��յ�������_____������������������ԭClO2��Һ�����ʵ���Ũ��Ϊ_____ mol/L(�ú���ĸ�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���ij�ܱ������м���һ������N2��H2�������淴Ӧ��N2(g)+3H2(g) ![]() 2NH3(g) ��H = -92.2kJmol��1�����0��10���ڣ�c(H2)��С��0.75molL��1������˵����ȷ����
2NH3(g) ��H = -92.2kJmol��1�����0��10���ڣ�c(H2)��С��0.75molL��1������˵����ȷ����
A��10��15����c(NH3) ����������0.25mol L��1
B����ѧ��Ӧ���ʹ�ϵ�ǣ�3������H2��= 2������NH3��
C����ƽ����������NH3��V�� ����
D���÷�Ӧ���淴Ӧ�Ļ�ܲ�С��92.2kJmol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ��(ƽ���ƶ�ԭ��)���͵���
����ˮ�д��ڻ�ѧƽ�⣺Br2��H2O ![]() HBr��HBrO��������AgNO3��Һ����Һ��ɫ��dz
HBr��HBrO��������AgNO3��Һ����Һ��ɫ��dz
�����ڳ�ʪ�Ŀ�����������
�۶���������������������ƽ����ϵ������ѹǿ����ɫ����
�ܺϳɰ���Ӧ��Ϊ��߰��IJ��ʣ�������Ӧ��ȡ�����¶ȵĴ�ʩ
�������Ȼ��ع����Ʊ��أ�Na(l)��KCl(l) ![]() K(g)��NaCl(l)
K(g)��NaCl(l)
��ӦCO(g)��NO2(g) ![]() CO2(g)��NO(g)(����ӦΪ���ȷ�Ӧ)���ﵽ��ѧƽ��������¶���ϵ����ɫ����
CO2(g)��NO(g)(����ӦΪ���ȷ�Ӧ)���ﵽ��ѧƽ��������¶���ϵ����ɫ����
A. �٢� B. �ڢ� C. �ڢ� D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���������������ϴ�������Ҫ�ɷ�ΪAl2O3,����Pd)����Al2(SO4)3��Pd ������ͼ��
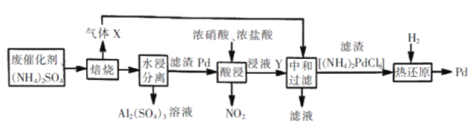
˵�������������б����¶Ȳ��˹��ߣ�����ᵼ������粒���ķֽ⡣
��1������ʱ��������X�ĽṹʽΪ________��
��2��ˮ�������У�����Pd�Ŀ����Ƚϴ�һ����Բ��õķ��뷽����_________ (����ĸ��
A.���� B.���� C.���� D.����
��3��д�����ʱ������Ӧ�����ӷ�ʽ______(��֪������Ϊ����)
��4��ijͬѧ��ʵ����������ͼ��ʾװ�����Pd���Ȼ�ԭʵ�飬������������ (NH4)2PdCl6�İٷֺ����������е����ʲ������Ȼ�ԭ��Ӧ����
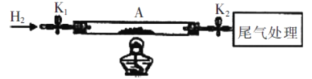
��д���Ȼ�ԭ�������з�����Ӧ�Ļ�ѧ����ʽ________��
��i.��ʯӢ�������У������أ�K1��K2)(��Ϊװ��A )���أ���Ϊmi g�������� [(NH4)2PdCl6]װ��ʯӢ�������У��ٴν�װ��A���أ���Ϊm2 g��
ii.���Ӻ�װ�ú�d�� �� ��b�� ��e(����)˳�����ʵ�顣_______
a.�ر�K1��K2 b.Ϩ��ƾ��� c.��ȼ�ƾ��ƣ�����
d.��K1��K2 e.����A f.����ͨ��H2 g.��ȴ������
iii.�ظ������������裬ֱ��A���أ���Ϊm3g��
�۸���ʵ���¼�����������У�NH4)2PdCl6�İٷֺ���__________[��ʽ��ʾ������(NH4)2PdCl6��Է�������Ϊ355]��
��ʵ�����ʱ������Ӳ���Թ��Ҷ���������ɫ���壬������____(�ѧʽ��,�����������ʵ����_________(����ƫ��������ƫ����������Ӱ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӫ�������������ڷ����ı仯������˵�����������������������ȷ����
A.����![]() ������
������![]() CO2��H2O(�ͷ�����ά�������)
CO2��H2O(�ͷ�����ά�������)
B.����![]() ������
������![]() CO2��H2O(�ͷ�����ά�������)
CO2��H2O(�ͷ�����ά�������)
C.��֬![]() ���ͺ�֬����
���ͺ�֬����![]() CO2��H2O(�ͷ�����ά�������)
CO2��H2O(�ͷ�����ά�������)
D.������![]() ������
������![]() ��������ĵ�����(������������)
��������ĵ�����(������������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ͷ����������γ�����ʱ������еİ��йأ���ͼ�������������������

A. �������ķ�ɢ����ͬ B. �����к�������狀������
C. NH3���γ���������Ĵ��� D. �������γ������ʩ�õ��ʡ�ȼ��ȼ�� �й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NOCl���۵���-64.5 �棬�е���0.5 �棬�ж�)��������һ�ֻ�ɫ��������ˮ��ˮ�⡣�����ںϳ���������ý�����м���ȡ�ʵ���ҿ���������һ�������ڳ��³�ѹ�ºϳɣ�����Һ̬������

��1�������ͬѧ���Ʊ�ԭ����NO��Cl2����������ͼ�Ʊ�װ��:
��д��NOCl��NԪ�ػ��ϼۣ�_______
��Ϊ�Ʊ�����������������±���ȱ�ٵ�ҩƷ�ǣ���д�ں����ϣ�:
ʵ����Ŀ | װ���� | װ���� | |
�Ʊ������� | ��ƿ�� | ��Һ©���� | |
a .�Ʊ����������Cl2 | MnO2 | _______ | _______ |
b .�Ʊ����������NO | Cu | _______ | _______ |
��2������ͬѧ���ü����Ƶõ�NO��Cl2�Ʊ�NOCl��װ����ͼ��ʾ:
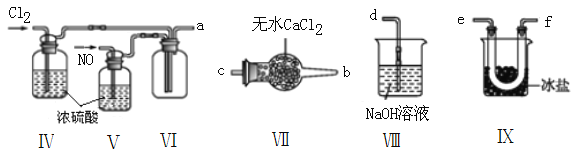
��װ������˳��Ϊa��____________________________(�������������ҷ�������Сд��ĸ��ʾ)��
��װ�����������ɽ�һ������NO��Cl2������һ��������______________________________��
��װ�â���ʵ����������װ��ǰ��Ӧ�������Ĵ�����_________________________��
��װ����������β��ʱ��NOCl�����ķ�������ԭ��Ӧ�Ļ�ѧ����ʽΪ___________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com