
【题目】工业上利用氧化铝基废催化剂(主要成份为Al2O3,少量Pd)回收Al2(SO4)3及Pd 流程如图:
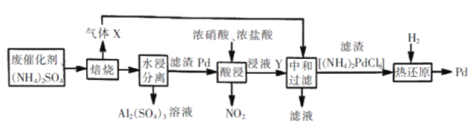
说明:上述流程中焙烧温度不宜过高,否则会导致硫酸铵固体的分解。
(1)焙烧时产生气体X的结构式为________。
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是_________ (填字母)
A.过滤 B.抽滤 C.倾析 D.渗析
(3)写出酸浸时发生反应的离子方式______(已知氯钯酸为弱酸)
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中 (NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应)。
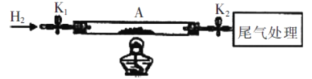
①写出热还原法过程中发生反应的化学方程式________。
②i.将石英玻璃管中(带开关;K1和K2)(设为装置A )称重,记为mi g。将滤渣 [(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→ → →b→ →e(填标号)顺序进行实验。_______
a.关闭K1和K2 b.熄灭酒精灯 c.点燃酒精灯,加热
d.打开K1和K2 e.称量A f.缓缓通入H2 g.冷却至室温
iii.重复上述操作步骤,直至A恒重,记为m3g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量__________[列式表示,其中(NH4)2PdCl6相对分子质量为355]。
④实验结束时,发现硬质试管右端有少量白色固体,可能是____(填化学式),这种情况导致实验结果_________(填“偏高”、“偏低”、“无影响”)
【答案】![]() C Pd+4NO3-+6Cl-+10H+=H2PdCl6+4NO2↑+4H2O
C Pd+4NO3-+6Cl-+10H+=H2PdCl6+4NO2↑+4H2O ![]() f;c;g;a
f;c;g;a ![]() NH4Cl 偏低
NH4Cl 偏低
【解析】
废催化剂(主要成分为Al2O3,少量Pd),废催化剂硫酸铵焙烧得到气体X为氨气,产物水浸过滤得到硫酸铝溶液,滤渣Pd加入浓硝酸和浓盐酸酸浸生成二氧化氮,浸液Y是Pd溶于王水发生Pd+6HCl+4HNO3=H2PdCl6+4NO2↑+4H2O,Y为H2PdCl6,通入氨气中和过滤得到滤渣(NH4)2PdCl6,被氢气还原得到Pd,发生(NH4)2PdCl6+2H2=Pd+2 NH3+6HCl,以此解答该题。
(1)焙烧得到气体是铵盐分解生成的氨气,结构式为![]() ,
,
故答案为:![]() ;
;
(2)水浸分离中,滤渣Pd的颗粒比较大,可用倾析的方法分离,故答案为:C;
(3)酸浸时发生反应的离子方程式为Pd+4NO3-+6Cl-+10H+=H2PdCl6+4NO2↑+4H2O,故答案为:Pd+4NO3-+6Cl-+10H+=H2PdCl6+4NO2↑+4H2O;
(4)①通入氢气,反应的方程式为![]() ,
,
故答案为:![]() ;
;
②实验时,应先通入氮气,冷却时注意关闭开关,防止氧气进入,冷却至室温再称量固体质量的变化,则正确的顺序为dfcbgae,
故答案为: f;c;g;a;
③样品的质量为(m2-m1)g,反应后减少的质量为(m2-m3)g,应为(NH4)2PdCl6、Pd质量之差,可知生成Pd的物质的量为![]() mol,可知(NH4)2PdCl6的质量为
mol,可知(NH4)2PdCl6的质量为![]() g,含量为
g,含量为![]() ,故答案为:
,故答案为:![]() ;
;
④实验结束时,若发现硬质试管右端有少量白色固体,可能是氯化铵,为氨气和氯化氢在温度较低时生成,这种情况会造成较大实验误差,可导致实验结果偏低,
故答案为:NH4Cl; 偏低。


科目:高中化学 来源: 题型:
【题目】下列各组关于强电解质、弱电解质、非电解质、混合物的归类,完全正确的是( )
A | B | C | D | |
强电解质 | Fe | NaCl |
|
|
弱电解质 |
|
|
|
|
非电解质 | 蔗糖 |
| 苯 |
|
混合物 | 碱石灰 | 胆矾 | 碘酒 | 液氯 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或离子方程式中,正确的是( )
A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) ΔH = -890.3 kJ·mol-1
B.500C、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) ΔH = -38.6 kJ·mol-1
2NH3(g) ΔH = -38.6 kJ·mol-1
C.向明矾溶液中加入过量的氢氧化钡溶液:Al3+ + 2SO42-+ 2Ba2+ + 4OH- = 2BaSO4↓+ 2H2O + AlO2-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4- + 5H2O2 + 6H+ = 2Mn2+ + 5 O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中,除稀有气体外几乎所有元素都能与氢形成氢化物。
(1)氨气属于共价型氢化物,工业常用氨气和醋酸二氨合铜[Cu(NH3)2]Ac的混合液来吸收CO(醋酸根离子简写为Ac-)。反应方程式为:[Cu(NH3)2]Ac+CO+NH3=[Cu(NH3)3CO]Ac
①氨水溶液中各元素原子的第一电离能从大到小排列顺序为___________。
②醋酸分子(CH3COOH)中的两个碳原子的杂化方式分别是_________________。
③生成物[Cu(NH3)3CO]Ac中所含化学键类型有_________(填序号)。
A.离子键b.金属键c.共价键d.配位键
(2)某离子化合物XY2,晶胞结构如图所示,其中6个Y原子用数字1~6标注。
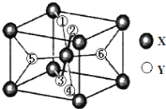
已知1、2、3、4号Y原子在晶胞上、下面上,则5、6号Y原子均在晶胞_________(填“侧面”或“内部”)。
②根据以上信息可以推知,XY2晶体的熔沸点______(填“>”、“=”或“<”)固态氨的熔沸点。
③若该晶胞的边长为anm,密度为ρg/cm3,XY2的摩尔质量为Mg/mol,则阿伏加德罗常数为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是个农业大国,农业是立国之本,化肥与农药的发展对农业起着巨大的推动作用。请回答下列问题:
(1)农作物生长过程中不可缺少的微量元素有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等,它们或是酶的组成成分,或能提高酶的活性,是农作物体内营养物质形成和新陈代谢不可缺少的元素。常用铜肥是胆矾,在盐碱地(土壤
等,它们或是酶的组成成分,或能提高酶的活性,是农作物体内营养物质形成和新陈代谢不可缺少的元素。常用铜肥是胆矾,在盐碱地(土壤![]() )施用胆矾时宜将溶液_____________(填“喷在叶片上”或“随水灌人土壤中”),原因是_______________________。
)施用胆矾时宜将溶液_____________(填“喷在叶片上”或“随水灌人土壤中”),原因是_______________________。
(2)农药波尔多液是一种常用的杀菌剂,常用配方为硫酸铜、熟石灰、水,三者按一定质量比混合,分析其防治病虫害的原因________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辛烷(C8H18)是汽油的重要成分,其与O2反应的能量变化如图所示。下列判断正确的是
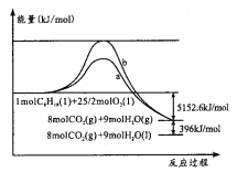
A. 曲线b代表加入催化剂时的能量变化
B. 反应物的总能量小于生成物的总能量
C. 表示辛烷燃烧热的热化学方程式:C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g) ΔH=-5152.6kJ/mol
D. 反应a、b的活化能不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() (X)、
(X)、![]() (Y)、
(Y)、![]() (Z)的分子式均为C5H6。下列说法正确的是( )
(Z)的分子式均为C5H6。下列说法正确的是( )
A.X、Y、Z均能使酸性高锰酸钾溶液褪色
B.Z的同分异构体只有X和Y两种
C.Z的二氯代物只有两种(不考虑立体异构)
D.Y分子中所有碳原子均处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,H2CO3 的 Kal=4.2×10-7,Ka2=5.6×10-11。室温下向10mL 0.1 mo1·L-1 Na2CO3 中逐滴加入 0.1 mo1·L-1 HCl。右图是溶液中含 C微粒物质的量分数随 pH降低而变化的
图像(CO2 因有逸出未画出)。下列说法错误的是
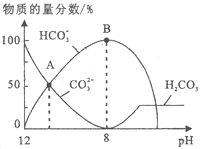
A. A点溶液的pH<11
B. B点溶液:c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2 CO3)
C. A→B 的过程中,离子反应方程式为:CO32-+H+=H CO3-
D. 分步加入酚酞和甲基橙,用中和滴定法可测定Na2CO3与NaHCO3混合物组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物瑞德西韦(Remdesivir)对新冠病毒有明显抑制作用,化合物M是合成瑞德西韦的中间体,下列关于M的说法错误的是( )
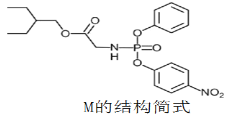
A.核磁共振氢谱共有10个吸收峰
B.分子中含有3种含氧官能团
C.分子中N原子一个是sp2杂化,一个是sp3杂化
D.1mol该物质与足量NaOH溶液反应时可以得到4种有机化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com