
����Ŀ���������ж�����Ԫ�ص�����(��֪Be��ԭ�Ӱ뾶Ϊ0.089nm)��
�� | �� | �� | �� | �� | �� | �� | �� | |
ԭ�Ӱ뾶(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
��������ϼ� | ��2 | ��1 | ��5 | ��7 | ��1 | ��5 | ��3 | |
������ϼ� | ��2 | ��3 | ��1 | ��3 |
��1�����Ԫ�������ڱ��е�λ����____������Ԫ�ش���ͬһ�������____��(��Ԫ�ط��ű�ʾ)
��2span>��Ԫ�آٺ͢����γ����ֻ����д�����н��ȶ��Ļ�������ˮ��Ӧ�����ӷ���ʽ��____��
��3����﮲���������й㷺Ӧ�ã�����ִ������(Li2NH��)����Яʽ��Դ����(LiCoO2��)����������Ҫ��ش����⣺
��![]() Li��
Li��![]() Li���˷�Ӧ����������壬
Li���˷�Ӧ����������壬![]() LiH��
LiH��![]() LiD�������¶Ѽ��ټ�������˵����ȷ����____��
LiD�������¶Ѽ��ټ�������˵����ȷ����____��
A.![]() Li��
Li��![]() Li��Ϊͬλ�� B.
Li��Ϊͬλ�� B.![]() Li��
Li��![]() Li����ͬ�ֺ���
Li����ͬ�ֺ���
C.![]() LiH��
LiH��![]() LiD�Ļ�ѧ���ʲ�ͬ D.
LiD�Ļ�ѧ���ʲ�ͬ D.![]() LiH��
LiH��![]() LiD��ͬ������
LiD��ͬ������
������˵������ȷ����____��
A.���ԣ�Be(OH)2<LiOH<NaOH<KOH
B.�뾶��K>Na>Li>Li+
C.�����ԣ�Li+<Na+<K+<Rb+<Cs+
D.�����ԣ�Cs>Rb>K>Na>Li>Be
���𰸡��ڶ����ڣ��ڢ�A�壻 Li��Na��N��P�� ![]() �� AD�� C��
�� AD�� C��
��������
Ԫ�������ɣ�ͬ���ڴ����ң�ԭ�Ӱ뾶��С��ͬ������ϵ��£�ԭ�Ӱ뾶���ͨ������ԭ�Ӱ뾶��Be��ԭ�Ӱ뾶Ϊ0.089nm��Ԫ�آ١��ߡ����ԭ�Ӱ뾶��BeС���ƶ�Ԫ�آ١��ߡ���Ϊ�ڶ�����Ԫ�أ�������������ϼۣ��Ƴ��١��ߡ���ֱ�ΪO��N��B���ۺ͢���������ϼ�Ϊ+1���Ңİ뾶�Ȣ۴��ƶϢۺֱ͢�ΪLi��NaԪ�أ��ڵ�ԭ�Ӱ뾶�Ȣ�С������������ϼ�Ϊ+2�����ΪMg���ܺ͢ߵ���������ϼ۶�Ϊ+5���Ңܵ�ԭ�Ӱ뾶�Ȣߴ����Ԣܺ͢߷ֱ���P��NԪ�أ��ݵ���������ϼ�Ϊ+7��������ϼ�Ϊ-1�����ΪClԪ�ء���Ԫ������ΪO��Mg��Li��P��Cl��Na��N��B��
Ԫ�������ɣ�ͬ���ڴ����ң�ԭ�Ӱ뾶��С��ͬ������ϵ��£�ԭ�Ӱ뾶���ͨ������ԭ�Ӱ뾶��Be��ԭ�Ӱ뾶Ϊ0.089nm��Ԫ�آ١��ߡ����ԭ�Ӱ뾶��BeС���ƶ�Ԫ�آ١��ߡ���Ϊ�ڶ�����Ԫ�أ�������������ϼۣ��Ƴ��١��ߡ���ֱ�ΪO��N��B���ۺ͢���������ϼ�Ϊ+1���Ңİ뾶�Ȣ۴��ƶϢۺֱ͢�ΪLi��NaԪ�أ��ڵ�ԭ�Ӱ뾶�Ȣ�С������������ϼ�Ϊ+2�����ΪMg���ܺ͢ߵ���������ϼ۶�Ϊ+5���Ңܵ�ԭ�Ӱ뾶�Ȣߴ����Ԣܺ͢߷ֱ���P��NԪ�أ��ݵ���������ϼ�Ϊ+7��������ϼ�Ϊ-1�����ΪClԪ�ء���Ԫ������ΪO��Mg��Li��P��Cl��Na��N��B��
��1�����Ԫ��ΪB���������ڱ��е�λ���ǵڶ����ڣ�����A�壻����Ԫ�ش���ͬһ�������Li��Na��N��P��
��2��Ԫ�آٺ͢����γɽ��ȶ��Ļ�������Na2O,����ˮ��Ӧ�����ӷ���ʽΪ![]() ��
��
��3��A.![]() Li��
Li��![]() Li��������ͬ����������ͬ��Ϊͬλ�أ�A��ȷ�� B.
Li��������ͬ����������ͬ��Ϊͬλ�أ�A��ȷ�� B. ![]() Li��
Li��![]() Li����ͬλ�أ�Ϊ��ͬ�ĺ��أ�B����
Li����ͬλ�أ�Ϊ��ͬ�ĺ��أ�B����
C. ![]() LiH��
LiH��![]() LiD����ͬ��Ԫ�ع��ɵĻ������ѧ���ʻ�����ͬ��C����
LiD����ͬ��Ԫ�ع��ɵĻ������ѧ���ʻ�����ͬ��C����
D. ![]() LiH��
LiH��![]() LiD��ͬ��Ԫ�ع��ɵĻ������ͬ�����ʣ�D��ȷ��
LiD��ͬ��Ԫ�ع��ɵĻ������ͬ�����ʣ�D��ȷ��
������ȷ��ΪAD��
�� A. ͬ���ڴ����ң������Լ������ǽ����Ա�ǿ������������Ӧˮ�����������ǿ�����Լ�����ͬ����Ԫ�ش��ϵ��£�����������Ӧˮ��������Լ��������Լ��ԣ�Be(OH)2 < LiOH < NaOH < KOH��A����ȷ��
B. ͬ����Ԫ�أ����ϵ��£�ԭ�Ӱ뾶���Li+��Ϊʧȥ���������ӣ����뾶С��Li�����뾶��K>Na>Li>Li+��B����ȷ��
C. ����ͬ����Ԫ�ش��ϵ���Ԫ�صĻ�ԭ�Ա�ǿ�����������ԣ�Li+>Na+>K+>Rb+>Cs+��C�����
D. ����ͬ����Ԫ�ش��ϵ���Ԫ�صĽ����Ա�ǿ�������ԣ�Cs>Rb>K>Na>Li>Be��D����ȷ��
���Բ���ȷ��ѡC��


 ������ϵ�д�
������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����ú�������(FeO��Fe2O3)�ķ�CuO�Ʊ��������徭�����й���(Fe3����pH��5ʱ����ȫ����)��
![]()
![]()
![]() ����
����![]()
![]()
![]()
![]()
![]() ��CuSO4��5H2O����
��CuSO4��5H2O����
���з�������ȷ����
A. ��98%��Ũ���������ܽ����õ�4.5 mol��L��1��ϡ���ᣬֻ��3�ֲ�������
B. �����Ŀ���ǽ���Һ���е�Fe2�����ת����Fe3����ʵ�����������Һ����ͨ����������
C. ����Cu(OH)2���CuOҲ�ɵ�����ҺpH����Ӱ��ʵ����
D. �����֮���ʵ������������ܼ��ᾧ�������������������������ƾ��ơ������ǡ����ż�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Na2CO3��NaHCO3��˵����ȷ����(����)
A.�����ߵ���Һ�м���BaCl2�����ɰ�ɫ����
B.�����ߵ���Һ����μ���HCl����Ӧ������ȫ��ͬ
C.Na2CO3��NaHCO3������֮������ת��
D.�͵�Na2CO3��Һ��ͨ��������CO2���壬�۲첻���κ�ʵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ������ڣ�800��ʱ��Ӧ2NO(g)+O2(g)��2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1��������Ӧ_____(������������������)���淴Ӧ���ڵ�5sʱ��NO��ת����Ϊ____��
��2����ͼ��ʾ����ʾNO2�仯���ߵ���____����O2��ʾ0��2s�ڸ÷�Ӧ��ƽ������v=____��

��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����____(����ĸ)��
a��v(NO2)=2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)=2v��(O2) d���������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25��ʱ����l0mL0.01mol��L-1NaA��Һ����μ���0.01mol��L-1�����ᣬ�ζ���������ͼ��ʾ������˵����ȷ���ǣ� ��

A. a�㵽c��Ĺ����У�c(HA)+c(A-)=0.01mol��L-1��ʽʼ�ճ���
B. b��ʱ����Һ����Ũ�ȴ�С�Ĺ�ϵ��c(A-)>c(Cl-)>c(HA)>c(OH-)>c(H+)
C. c����Һ���ڵĹ�ϵ��c(Na+)+c(H+)=c(HA)+c(OH-)+2c(A-)
D. ��ͼ��֪����Ũ�ȵ�HA��NaA�����Һ�У�HA�ĵ���̶ȴ���A-��ˮ��̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����Fe(s)��![]() O2(g)=FeO(s)����H1����272.0 kJ/mol��
O2(g)=FeO(s)����H1����272.0 kJ/mol��
��2Al(s)��![]() O2(g)=Al2O3(s)����H2����1 675.7 kJ/mol��
O2(g)=Al2O3(s)����H2����1 675.7 kJ/mol��
Al��FeO�������ȷ�Ӧ���Ȼ�ѧ����ʽ��______________________��ijͬѧ��Ϊ�����ȷ�Ӧ�����ڹ�ҵ����������ж���________(��ܡ����ܡ�)�����������________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.������״̬�ܵ��������һ�������ӻ�����
B.CO2��CS2ÿ��ԭ�ӵ�����㶼����8�����ȶ��ṹ
C.�ɱ���ʯӢ�����еĻ�ѧ��������ͬ���ۻ�ʱ��˷����������������Ҳ��ͬ
D.2016��IUPAC����117��Ԫ��ΪTs��Ts��ԭ�Ӻ���������������7���ǵ������ڵڢ�B��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H��0����һ���¶Ⱥ�ѹǿ�����ܱ������У���Ӧ�ﵽƽ�⡣����������ȷ���ǣ� ��
CO2(g)+H2(g) ��H��0����һ���¶Ⱥ�ѹǿ�����ܱ������У���Ӧ�ﵽƽ�⡣����������ȷ���ǣ� ��
A.����һ�����ĵ�����n(H2)����
B.��Сѹǿ��n(CO2)����
C.������Ч������CO��ת��������
D.�����¶ȣ�K����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦmA(g)��nB(g) ![]() pC(g)�����ʺ�ƽ���Ӱ��ͼ�����£������ж���ȷ����
pC(g)�����ʺ�ƽ���Ӱ��ͼ�����£������ж���ȷ����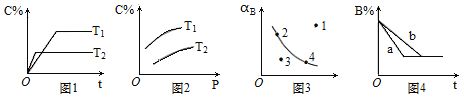
A.��ͼ1��֪��T1��T2���÷�Ӧ����ӦΪ���ȷ�Ӧ
B.��ͼ2��֪���÷�Ӧm��n��p
C.ͼ3�У���ʾ��Ӧ�����������������ǵ�1
D.ͼ4�У���m��n��p����a����һ��ʹ���˴���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com