
【题目】下列说法正确的是
A.在熔融状态能导电的物质一定是离子化合物
B.CO2和CS2每个原子的最外层都具有8电子稳定结构
C.干冰和石英晶体中的化学键类型相同,熔化时需克服微粒间的作用力类型也相同
D.2016年IUPAC命名117号元素为Ts,Ts的原子核外最外层电子数是7,是第七周期第ⅦB族元素
【答案】B
【解析】
A.在熔融状态能导电的物质不一定是化合物,还可以是金属单质,在熔融状态能导电的化合物一定是离子化合物,故A错误;
B.CO2中每个碳原子与氧原子形成两个共用电子对,其电子式为:![]() ,每个原子的最外层都具有8电子稳定结构,CO2和CS2互为等电子体,互为等电子体的微粒具有相同的结构,则二者每个原子的最外层都具有8电子稳定结构,故B正确;
,每个原子的最外层都具有8电子稳定结构,CO2和CS2互为等电子体,互为等电子体的微粒具有相同的结构,则二者每个原子的最外层都具有8电子稳定结构,故B正确;
C.干冰和石英晶体中的化学键类型相同,均含有共价键,但干冰属于分子晶体,熔化时需克服微粒间的作用力为范德华力,石英为原子晶体,熔化时需克服微粒间的作用力为共价键,则熔化时需克服微粒间的作用力类型不相同,故C错误;
D.元素周期表中,118号元素位于第七周期零族,则117号元素Ts位于第七周期第ⅦA族,主族元素最外层电子数等于主族序数,则Ts的原子核外最外层电子数是7,故D错误;
答案选B。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】10L含有丙烯,丁炔和甲烷的混合物与足量O2混合点燃后,恢复到原来状态(常温、常压),气体体积共缩小21L ,则甲烷的体积分数为
A. 20% B. 30% C. 80% D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个1L的密闭容器中,加入2molA和1molB进行如下反应:2A(g)+2B(g)![]() 3C(?)+D(?)。反应一段时间后达到平衡,测得生成0.6molC,且反应前后压强之比为15∶11(相同温度下测量),则下列说法正确的是( )
3C(?)+D(?)。反应一段时间后达到平衡,测得生成0.6molC,且反应前后压强之比为15∶11(相同温度下测量),则下列说法正确的是( )
A. 该反应的化学平衡常数K约为0.043
B. 增加C的物质的量,B的平衡转化率不变
C. 增大该体系的压强,平衡正向移动,化学平衡常数增大
D. A的平衡转化率是40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列短周期元素的数据(已知Be的原子半径为0.089nm):
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
最低负化合价 | -2 | -3 | -1 | -3 |
(1)⑧号元素在周期表中的位置是____;上述元素处于同一主族的有____。(用元素符号表示)
(2span>)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式:____。
(3)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等)。根据下列要求回答问题:
①![]() Li和
Li和![]() Li作核反应堆最佳热载体,
Li作核反应堆最佳热载体,![]() LiH和
LiH和![]() LiD用作高温堆减速剂。下列说法正确的是____。
LiD用作高温堆减速剂。下列说法正确的是____。
A.![]() Li和
Li和![]() Li互为同位素 B.
Li互为同位素 B.![]() Li和
Li和![]() Li属于同种核素
Li属于同种核素
C.![]() LiH和
LiH和![]() LiD的化学性质不同 D.
LiD的化学性质不同 D.![]() LiH和
LiH和![]() LiD是同种物质
LiD是同种物质
②下列说法不正确的是____。
A.碱性:Be(OH)2<LiOH<NaOH<KOH
B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+
D.金属性:Cs>Rb>K>Na>Li>Be
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界____。
(2)表中最活泼的金属与最活泼的非金属形成的物质是___(填化学式)。
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:___,这两种化合物中所含的化学键有____(填字母)。
A.极性共价键 B.非极性共价键 C.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为____(填离子符号)。
(5)d、m对应的离子还原性由强到弱顺序为____(填离子符号)。
(6)d、e、m、p的气态氢化物中,最不稳定的是(填分子式)____。
(7)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐是优良的多功能水处理剂。某实验小组采用如图装置制备高铁酸钾![]() 并探究其性质用途。
并探究其性质用途。
资料:![]() 为紫色固体,微溶于KOH溶液,难溶于有机溶剂;具有强氧化性,在酸性或中性溶液中紫色快速褪去并产生
为紫色固体,微溶于KOH溶液,难溶于有机溶剂;具有强氧化性,在酸性或中性溶液中紫色快速褪去并产生![]() ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
Ⅰ![]() 制备
制备![]() 夹持、加热等装置略
夹持、加热等装置略![]()

(1)![]() 中发生反应的化学方程式为________________;B中所用试剂为________________。
中发生反应的化学方程式为________________;B中所用试剂为________________。
(2)C中反应为放热反应,而反应温度须控制在![]() ,可使用的控温方法为________,充分反应后得到紫色固体,反应方程式为________________________。反应中KOH必须过量的原因是________________________。
,可使用的控温方法为________,充分反应后得到紫色固体,反应方程式为________________________。反应中KOH必须过量的原因是________________________。
(3)C中混合物经过滤、洗涤、干燥,得纯净高铁酸钾晶体,洗涤时洗涤剂可选用________。
![]() 冰水
冰水 ![]() 溶液
溶液 ![]() 异丙醇
异丙醇
Ⅱ![]() 探究
探究![]() 的性质
的性质
(4)![]() 可以将废水中的
可以将废水中的![]() 氧化为
氧化为![]() ,实验表明,
,实验表明,![]() 时
时![]() 去除效果最佳。配平反应离子方程式:______FeO42-+___________CN-__________H2O→Fe(OH)3↓+_______CNO-_________OH-。_________
去除效果最佳。配平反应离子方程式:______FeO42-+___________CN-__________H2O→Fe(OH)3↓+_______CNO-_________OH-。_________
现处理含![]() 离子浓度为
离子浓度为![]() 的废水
的废水![]() ,至少需要
,至少需要![]() ________g。
________g。
(5)用滴定分析法测定样品中![]() 的纯度:现称取
的纯度:现称取![]() 制备的样品溶于适量氢氧化钾溶液中,加入稍过量的
制备的样品溶于适量氢氧化钾溶液中,加入稍过量的![]() ,充分反应后过滤,滤液定容于250mL容量瓶中。
,充分反应后过滤,滤液定容于250mL容量瓶中。
每次取![]() 加入稀硫酸酸化,用
加入稀硫酸酸化,用![]() 的
的![]() 标准溶液滴定,三次滴定消耗标准溶液的平均体积为
标准溶液滴定,三次滴定消耗标准溶液的平均体积为![]() 。有关反应的离子方程式为:
。有关反应的离子方程式为:
![]() ;
;
![]() ;
;
![]() 。
。
样品中高铁酸钾的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组探究铜丝与足量浓硫酸的反应,装置(已略去夹持装置,其中铜丝可抽动)如图,下列有关说法不正确的是( )
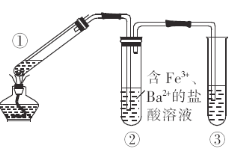
A.①中生成的气体可使品红溶液褪色
B.②中可观察到溶液黄色变浅,且有白色沉淀生成
C.为进行尾气处理,③中装有![]() 溶液
溶液
D.反应后,通过向①中加水,观察溶液颜色可判断反应有硫酸铜生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和。
请回答下列问题:
(1)分子式为BC2的空间构型为__ __;F2+的核外电子排布式为 。
(2)A分别与B、C形成的最简单化合物的稳定性B____C(填“大于”或“小于”);A、C两元素可组成原子个数比为1:1的化合物,C元素的杂化类型为 。
(3)A2C所形成的晶体类型为_ ___;F单质形成的晶体类型为 ,其采用的堆积方式为 。
(4)F元素氧化物的熔点比其硫化物的____(填“高”或 “低”),请解释其原因____。
(5)D跟E可形成离子化合物,其晶胞结构如右图。该离子化合物晶体的密度为pg.cm。3,则晶胞的体积是 。(用含p的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向一定体积的![]() 的
的![]() 溶液中逐滴加入
溶液中逐滴加入![]() 盐酸至过量,溶液中含碳元素的各微粒的物质的量浓度的百分含量随溶液pH的变化如图所示
盐酸至过量,溶液中含碳元素的各微粒的物质的量浓度的百分含量随溶液pH的变化如图所示![]() 因逸出未画出,滴加盐酸的过程中温度的变化忽略不计
因逸出未画出,滴加盐酸的过程中温度的变化忽略不计![]() 。下列说法正确的是
。下列说法正确的是![]()
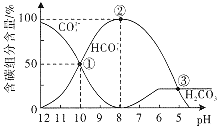
A.点![]() 时溶液中水的电离程度比纯水的大
时溶液中水的电离程度比纯水的大
B.点![]() 所示溶液中:
所示溶液中:![]()
C.当滴加盐酸到点![]() 时,才开始放出
时,才开始放出![]() 气体
气体
D.![]() 第一步水解反应的平衡常数:
第一步水解反应的平衡常数:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com