
【题目】在密闭容器中进行反应:A(g)+3B(g)![]() 2C(g),有关下列图像说法的不正确的是( )
2C(g),有关下列图像说法的不正确的是( )
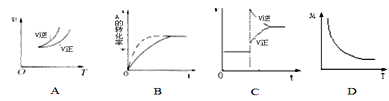
A. 依据图A可判断正反应为放热反应
B. 在图B中,虚线可表示使用了催化剂
C. 若正反应的△H<0,图C可表示升高温度使平衡向逆反应方向移动
D. 由图D中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的△H>0
【答案】D
【解析】
A.依据图a可知:当反应达到平衡后,由于升高温度,V逆>V正 平衡逆向移动,根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,因此可判断正反应为放热反应,故不选A;
B.在图B中,平衡未移动,但是达到平衡所需要的时间缩短,由于该反应是气体体积减小的反应,所以虚线只能表示是加入了催化剂,故不选B;
C.若正反应的ΔH<0,升高温度,根据平衡移动原理,平衡逆向移动,故可以用图c可表示升高温度使平衡向逆反应方向移动,故不选C;
D.由于升高温度,气体的平均相对分子质量减小,则根据平衡移动原理,升高温度,平衡向吸热反应方向移动,平衡逆向移动,可推知正反应的ΔH<0,故选D;
答案:D


科目:高中化学 来源: 题型:
【题目】(1)积极保护生态环境可实现人与自然的和谐共处。
①下列做法会加剧温室效应的是__________(填字母)。
a.植树造林 b.燃煤供暖 c.风力发电
②下列防治“白色污染”的正确方法是_____________(填字母)。
a.使用可降解塑料 b.露天焚烧废旧塑料 c.直接填埋废旧塑料
③为减轻大气污染,多个城市已禁止燃放烟花爆竹。“禁止燃放烟花爆竹”的标识是_____(填字母)。

(2)合理使用化学知识可提高人们的生活质量。
某品牌牙膏的成分有甘油、山梨酸钾、氟化钠等。
①在上述牙膏成分中,属于防腐剂的是_______________。
②甘油的结构简式为____________;油脂水解可生成甘油和_____________。
③氟化钠(NaF)可与牙齿中的羟基磷酸钙[Ca5(PO4)3OH]反应,生成更难溶的氟磷酸钙[Ca5(PO4)3F],从而达到防治龋齿的目的。写出该反应的化学方程式:____________________。
(3)创新发展材料技术科推动人类社会的进步。
①石墨烯(见下图)可用作太阳能电池的电极,这里主要利用了石墨烯的______________性。

②基础工程建设中常用到水泥、玻璃、钢材等。生成水泥和玻璃都用到的原料是__________;在钢材中添加铬、镍等元素的目的是___________。
③新型战斗机常用纳米SiC粉体作为吸波材料。高温下焦炭和石英反应可制得SiC,石英的化学式为________________;高温分解Si(CH3)2Cl2也可制得SiC,同时还生成CH4和一种常见酸性气体,写出该反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正丁醛经催化加氢可制备1丁醇。为提纯含少量正丁醛杂质的1丁醇,现设计如下路线:
![]()
已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1丁醇互溶;③1丁醇的沸点是118℃。
则操作1~4分别是______、_______、________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在。现以Al—H2O2电池电解尿素CO(NH2)2的碱性溶液制备H2,下列说法不正确的是( )
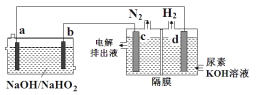
A.电解过程中,电子的流向由a→d→c→b
B.电池的正极反应为:HO2-+2e-+H2O=3OH-
C.电解时,消耗5.4gAl,则产生标况下2.24L N2
D.电极c是阳极,且反应后该电极区pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)我国规定生活用水中镉排放的最大允许浓度为0.005 mg/L。处理含镉废水可采用化学沉淀法。试回答下列问题:
①磷酸镉(Cd3(PO4)2)沉淀溶解平衡常数的表达式Ksp=_____________________。
②在某含镉废水中加人Na2S,当S2-浓度达到7.9 × 10-8mol/L时,水体中Cd2+浓度为_____mol/L(已知:Ksp(CdS)=7.9 × 10-27,Cd的相对原子质量:112);此时是否符合水源标准?______(填“是”或“否”)。
(2)炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:
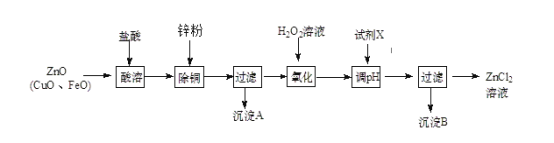
下表列出了相关金属离子生成氢氧化物沉淀的pH (开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子 | Fe3+ | Zn2+ | Fe2+ |
开始沉淀的pH | 1. 1 | 5. 2 | 5. 8 |
沉淀完全的pH | 3. 2 | 6. 4 | 8. 8 |
①加入H2O2溶液的作用是________________。
②流程图中,调节pH时,加入的试剂X可以是________(填序号);
a、ZnO b、NaOH c、Zn2(OH)2CO3 d、ZnSO4
pH应调整到______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过碳酸钠(2Na2CO3·H2O2),俗名固体双氧水,具有Na2CO3和H2O2双重性质,可用作无毒漂白剂和供氧剂。一种利用双氧水和纯碱在稳定剂作用下制备过碳酸钠的工艺流稳定程如下图。已知:2Na2CO3+3H2O2![]() 2Na2CO3·3H2O2
2Na2CO3·3H2O2

下列说法不正确的是
A.FeCl3溶液可加速过碳酸钠的失效
B.加入NaCl的作用是降低2Na2CO3·3H2O2的溶解度,以析出更多晶体
C.生产过碳酸钠的流程中遗漏了晶体的洗涤一步,导致产品纯度降低
D.该生产流程中可循环使用的物质是CO2和NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X____。
(2)上述实验流程中①②③步均要进行的实验操作是____(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是____________。
(4)按此实验方案得到的溶液3中肯定含有杂质。为了解决这个问题,可以向溶液3中加入适量的________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸奥布卡因临床主要用作眼科表面麻醉用药,我国科研人员最近报道了盐酸奥布卡因新的合成路线:
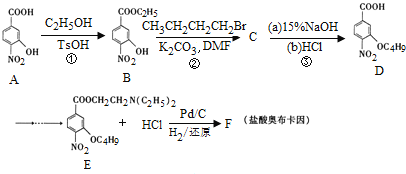
(1)A中含有的官能团名称是 ______ ;A→B的反应类型为 ______ ;
(2)步骤①③的目的是 ______ ;
(3)写出②的化学方程式 ______ ;
(4)G是A的同分异构体,具有下列特征:①苯环上连有硝基和酚羟基,且位于对位;②能发生水解反应,则G的结构有 ______ 种.
(5)下列说法正确的是 ______ ;
a.1molA最多可与含1molNaOH的烧碱溶液反应
b.步骤②中,K2CO3的作用是与生成的HBr反应,使平衡正向移动,提高产率
c.CH3CH2CH2Br系统命名为4-溴丁烷
d.E→F是将-NO2还原为-NH2.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,取浓度均为0.1molL-1的醋酸溶液和氨水溶液各20mL,分别用0.1molL-1NaOH溶液、0.1molL-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是
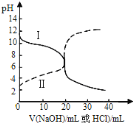
A.曲线Ⅰ:滴加溶液到10mL时![]()
B.曲线Ⅱ:滴加溶液到20mL时:![]()
C.根据滴定曲线,可得![]()
D.由曲线Ⅱ可知,选用酚酞和选用甲基橙作指示剂,消耗NaOH溶液的体积相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com