
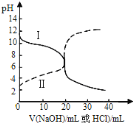
【题目】25℃时,取浓度均为0.1molL-1的醋酸溶液和氨水溶液各20mL,分别用0.1molL-1NaOH溶液、0.1molL-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是
A.曲线Ⅰ:滴加溶液到10mL时![]()
B.曲线Ⅱ:滴加溶液到20mL时:![]()
C.根据滴定曲线,可得![]()
D.由曲线Ⅱ可知,选用酚酞和选用甲基橙作指示剂,消耗NaOH溶液的体积相同
【答案】B
【解析】
A. 曲线Ⅰ表示用盐酸滴定氨水,滴加溶液到10mL时,溶液中的溶质是等物质的量的氨水和氯化铵,溶液呈碱性,氨水电离大于氯化铵水解,所以![]() ,故A错误;
,故A错误;
B. 曲线Ⅱ表示氢氧化钠溶液滴定醋酸,滴加溶液到20mL时,恰好反应,溶质是醋酸钠,根据物料守恒![]() ,根据电荷守,
,根据电荷守,![]() ,所以
,所以![]() ;故B正确 ;
;故B正确 ;
C. 根据滴定曲线,0.1molL-1的氨水溶液pH=11,所以Kb(NH3H2O)= ![]() ≈
≈![]() =10-5 ,故C错误;
=10-5 ,故C错误;
D.曲线Ⅱ表示氢氧化钠溶液滴定醋酸,甲基橙的变色范围是3.1~4.4,酚酞的变色范围是8~10,使酚酞变色需要碱性,选用酚酞作指示剂消耗NaOH溶液的体积大,故D错误;
故答案选B。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:A(g)+3B(g)![]() 2C(g),有关下列图像说法的不正确的是( )
2C(g),有关下列图像说法的不正确的是( )
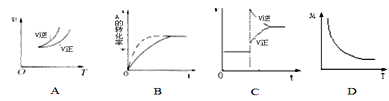
A. 依据图A可判断正反应为放热反应
B. 在图B中,虚线可表示使用了催化剂
C. 若正反应的△H<0,图C可表示升高温度使平衡向逆反应方向移动
D. 由图D中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所学知识回答下列问题:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1 ____ΔH2(填“>”、“<”或“=”,下同)。
(2)相同条件下,1 mol氮气和氢气反应断键吸收能量____形成2 mol氨气成键所放出的能量。
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1___ΔH2。①P4(白磷,s)+5O2(g)= 2P2O5(s) ΔH1, ②4P(红磷,s)+5O2(g)= 2P2O5(s) ΔH2。
(4)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36 kJ热量,该反应的热化学方程式是_______。
(5)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式是_______。
(6)已知:C(s)+O2(g)=CO2(g) △H=-437.3kJmol﹣1,H2(g)+![]() O2(g)=H2O(g) △H=-285.8kJmol﹣1,CO(g)+
O2(g)=H2O(g) △H=-285.8kJmol﹣1,CO(g)+![]() O2(g)=CO2(g) △H=-283.0kJmol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=__kJmol﹣1。
O2(g)=CO2(g) △H=-283.0kJmol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=__kJmol﹣1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的混合气体在密闭容器中发生反应 mA(g)+nB(g)![]() pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是
pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是
A. C的体积分数增加 B. A的转化率降低
C. 平衡向正反应方向移动 D. m+n>p
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是

A. 放电时,a电极反应为
B. 放电时,溶液中离子的数目增大
C. 充电时,b电极每增重![]() ,溶液中有
,溶液中有![]() 被氧化
被氧化
D. 充电时,a电极接外电源负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:
2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)放出热量99kJ,请回答下列问题:
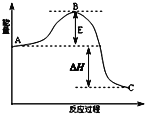
(1)图中A、C分别表示_____________、_____________.
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点_________(填“升高”,“降低”),△H_______(填“变大”,“变 小”或“不变”),理由是______________________.
(3)图中△H=________kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F、G、H八种原子序数依次增大的元素(原子序数均小于30).A原子的核外电子数与电子层数相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,A、E同主族,F的基态原子s能级的电子总数与p能级的电子数相等,B、G同族,H的基态原子的3d轨道电子数是4s电子数的4倍.请回答下列问题:
(1)H元素在周期表中属于 ______ 区.G的基态原子电子排布式为 ______ CD2+中C的杂化类型是 ______
(2)下列说法不正确的是 ______ .
a.B2A2分子中含有σ键和π键 b.B2A2分子的沸点明显低于A2D2分子
c.A2D2分子的空间构型为直线形 d.B、C、D的电负性由大到小的顺序为D>C>B
e.B、C、D的第一电离能由大到小的顺序为D>C>B
f.H2+能与BD分子形成[H(BD)]2+,其原因是BD分子中含有空轨道
g.B和G的单质能形成相同类型的晶体,其熔点B>G
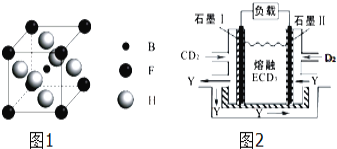
(3)由B、F、H三种元素形成的一种具有超导性的晶体,B位于F和H原子紧密堆积所形成的空隙当中.晶胞如图1所示,该晶体的化学式为 ______
(4)CD2、D2和熔融ECD3可制作燃料电池,其原理如图2所示.该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,石墨Ⅰ电极反应式为 ______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通常状况下,A为固态单质。根据下图转化关系,回答:
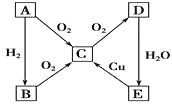
(1)写出A、E的化学式:A__________,E__________。
(2)写出下列反应的化学方程式:
①E→C :________________________________________________________;
②C→D :________________________________________________________。
(3)B与E的浓溶液能反应,当B、E等物质的量反应时,化学方程式为_______________________,反应现象_________________________。
(4)若A为气态单质,则写出B、D化学式:B__________,D__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.课堂上,老师提问如何鉴别浓硫酸与稀硫酸,某学习小组设计方案如下
方案 | 结论 | |
① | 往酸中投入火柴梗 | 变黑者为浓硫酸 |
② | 加入铝片 | 产生刺激性气味者为浓硫酸 |
② | 加少量酸于盛水的小烧杯中 | 放热者为浓硫酸 |
④ | 用玻璃棒蘸浓氨水靠近酸的瓶口 | 冒白烟者为浓硫酸 |
⑤ | 将酸滴加到胆矾晶体上 | 变白者为浓硫酸 |
(1)以上方案中,可行的是______________(填序号)
(2)其中一个稍作改进就能成为可行方案是________________,改进方法为____________。
(3)完全错误的是__________,因为_________________________________________。
Ⅱ.实验室用浓硫酸配制1.0mol/L硫酸溶液480mL,回答下列问题:
(1)如下图所示的仪器中配制溶液肯定不需要的是____________(填字母),配制上述溶液还需要用到的玻璃仪器是_________________________(填仪器名称)。
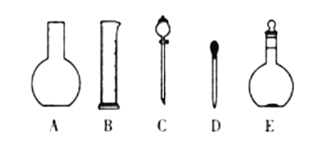
(2)容量瓶上标有以下5项中的_____________(填序号)
①压强 ②温度 ③容量 ④浓度 ⑤刻度线
(3)在配制过程中,下列操作使所配溶液浓度偏大的是______________(填序号)。
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
②定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
③定容时,仰视刻度线
④使用容量瓶前用蒸馏水洗涤且没干燥
(4)计算实验室配制上述溶液需用量筒取质量分数为98%、密度为1.84g/mL的浓硫酸的体积为_____________________mL。(保留小数点后一位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com