
【题目】请根据所学知识回答下列问题:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1 ____ΔH2(填“>”、“<”或“=”,下同)。
(2)相同条件下,1 mol氮气和氢气反应断键吸收能量____形成2 mol氨气成键所放出的能量。
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1___ΔH2。①P4(白磷,s)+5O2(g)= 2P2O5(s) ΔH1, ②4P(红磷,s)+5O2(g)= 2P2O5(s) ΔH2。
(4)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36 kJ热量,该反应的热化学方程式是_______。
(5)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式是_______。
(6)已知:C(s)+O2(g)=CO2(g) △H=-437.3kJmol﹣1,H2(g)+![]() O2(g)=H2O(g) △H=-285.8kJmol﹣1,CO(g)+
O2(g)=H2O(g) △H=-285.8kJmol﹣1,CO(g)+![]() O2(g)=CO2(g) △H=-283.0kJmol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=__kJmol﹣1。
O2(g)=CO2(g) △H=-283.0kJmol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=__kJmol﹣1。
【答案】= < < S(s)+O2(g)==SO2(g) △H=-299.52 kJmol﹣1 CH4(g)+H2O==CO(g)+3H2(g) △H=+2a kJmol﹣1 +131.5
【解析】
(1)反应热与反应物的总能量和生成物的总能量,与反应条件无关;
(2)化学键断裂为吸热过程,新键生成放热的过程;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多;
(4)根据题意,求出1 mol S燃烧放出的热量,再根据热化学方程式的含义以及书写方法来回答;
(5)根据热化学方程式的含义以及书写方法来回答;
(6)根据热化学方程式和盖斯定律计算得到,反应焓变与反应过程无关。
(1)反应热与反应物的总能量和生成物的总能量,与反应条件无关,则光照和点燃条件的△H相同;
故答案为:=;
(2)氮气与氢气反应合成氨气,属于放热反应,根据△H=反应物断开吸收的能量-生成物形成放出的能量可知,1 mol氮气和氢气反应断键吸收能量小于形成2 mol氨气成键所放出的能量,故答案为:<;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多,因△H<0,则放出的能量越多反应热越小;
故答案为:<;
(4) 25℃、1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36 kJ热量,则1mol硫粉充分燃烧放出的热量为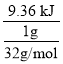 =299.52 kJmol﹣1,故热化学方程式为:S(s)+O2(g)==SO2(g) △H=-299.52 kJmol﹣1;
=299.52 kJmol﹣1,故热化学方程式为:S(s)+O2(g)==SO2(g) △H=-299.52 kJmol﹣1;
(5) 0.5 mol CH4(g)与0.5 mol水蒸气在t℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,所以1mol甲烷与1mol水蒸气在t℃、pkPa时,完全反应生成一氧化碳和氢气(合成气),吸收了2akJ热量,热化学方程式为:CH4(g)+H2O==CO(g)+3H2(g) △H=+2a kJmol﹣1;
故答案为:CH4(g)+H2O==CO(g)+3H2(g) △H=+2a kJmol﹣1;
(6)已知
①C(s)+O2(g)=CO2(g) △H=-437.3 kJmol﹣1,
②H2(g)+![]() O2(g)=H2O(g) △H=-285.8 kJmol﹣1,
O2(g)=H2O(g) △H=-285.8 kJmol﹣1,
③CO(g)+![]() O2(g)=CO2(g) △H=-283.0 kJmol﹣1,
O2(g)=CO2(g) △H=-283.0 kJmol﹣1,
依据盖斯定律①②③,得到:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.5kJmol﹣1,故答案为:+131.5。


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】正丁醛经催化加氢可制备1丁醇。为提纯含少量正丁醛杂质的1丁醇,现设计如下路线:
![]()
已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1丁醇互溶;③1丁醇的沸点是118℃。
则操作1~4分别是______、_______、________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X____。
(2)上述实验流程中①②③步均要进行的实验操作是____(填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液的目的是____________。
(4)按此实验方案得到的溶液3中肯定含有杂质。为了解决这个问题,可以向溶液3中加入适量的________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸奥布卡因临床主要用作眼科表面麻醉用药,我国科研人员最近报道了盐酸奥布卡因新的合成路线:
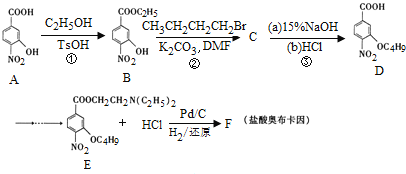
(1)A中含有的官能团名称是 ______ ;A→B的反应类型为 ______ ;
(2)步骤①③的目的是 ______ ;
(3)写出②的化学方程式 ______ ;
(4)G是A的同分异构体,具有下列特征:①苯环上连有硝基和酚羟基,且位于对位;②能发生水解反应,则G的结构有 ______ 种.
(5)下列说法正确的是 ______ ;
a.1molA最多可与含1molNaOH的烧碱溶液反应
b.步骤②中,K2CO3的作用是与生成的HBr反应,使平衡正向移动,提高产率
c.CH3CH2CH2Br系统命名为4-溴丁烷
d.E→F是将-NO2还原为-NH2.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将33.6LHCl气体溶于50mL水再配成500mL溶液,求:
(1)所得盐酸的物质的量浓度为___________________。
(2)若将此溶液再加水稀释至1.5L,则稀释后盐酸的物质的量浓度为__________。
(3)将(2)的溶液取出1L与足量的石灰石反应,产生的CO2在标准状况下的体积为___________?(此问写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2。符合上述转化关系的A、C可能是
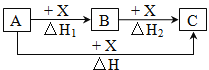
①Fe、FeCl3②C、CO2③AlCl3、NaAlO2④NaOH、NaHCO3⑤S、SO3⑥Na2CO3、CO2
A.只有②③④⑥B.除①外C.除⑤外D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )

A.该实验说明氨气是一种极易溶于水的气体
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性
C.氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化
D.形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,取浓度均为0.1molL-1的醋酸溶液和氨水溶液各20mL,分别用0.1molL-1NaOH溶液、0.1molL-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是
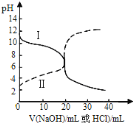
A.曲线Ⅰ:滴加溶液到10mL时![]()
B.曲线Ⅱ:滴加溶液到20mL时:![]()
C.根据滴定曲线,可得![]()
D.由曲线Ⅱ可知,选用酚酞和选用甲基橙作指示剂,消耗NaOH溶液的体积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:正四面体形分子E和直线形分子G反应,生成四面体形分子L和直线形分子M(组成E分子的元素的原子序数均小于10,组成G分子的元素为第三周期元素)。下列判断中正确的是( )
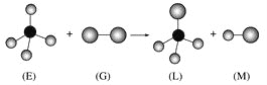
A. 常温常压下,L是一种液态有机物
B. E的二溴代物只有两种结构
C. G具有强氧化性和漂白性
D. 上述反应的类型是取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com