
【题目】标准状况下,将33.6LHCl气体溶于50mL水再配成500mL溶液,求:
(1)所得盐酸的物质的量浓度为___________________。
(2)若将此溶液再加水稀释至1.5L,则稀释后盐酸的物质的量浓度为__________。
(3)将(2)的溶液取出1L与足量的石灰石反应,产生的CO2在标准状况下的体积为___________?(此问写出计算过程)
【答案】3 mol/L 1 mol/L 11.2L
【解析】
(1)根据n=![]() 计算HCl物质的量,再根据c=
计算HCl物质的量,再根据c=![]() 计算;
计算;
(2)稀释前后HCl的物质的量不变,根据c=![]() 计算;
计算;
(3)根据n=cV计算HCl物质的量,再根据V=nVm计算二氧化碳体积。
(1)标况下,33.6L HCl的物质的量为![]() =1.5mol,溶于50mL水再配成500mL溶液,所得盐酸的物质的量浓度为
=1.5mol,溶于50mL水再配成500mL溶液,所得盐酸的物质的量浓度为![]() =3mol/L;
=3mol/L;
(2)稀释前后HCl的物质的量不变,将此溶液再稀释成1.5L溶液,则稀释后盐酸的物质的量浓度变为![]() =1mol/L;
=1mol/L;
(3)n(HCl)=1mol/L×1L=1mol,由反应CaCO3+2HCl═CaCl2+H2O+CO2↑可知n(CO2)=0.5mol,标准状况下V(CO2)=0.5mol×22.4L/mol=11.2L。


科目:高中化学 来源: 题型:
【题目】如图某学校实验室从化学试剂商店买回的硝酸试剂标签上的部分内容。据此下列说法错误的是( )

A.该硝酸应贮在棕色试剂瓶中
B.该硝酸与等体积的水混合所得溶液的质量分数小于31.5%
C.该硝酸试剂的物质的量浓度为11.4mol·L-1
D.该硝酸中溶质与溶剂的物质的量之比为9:50
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式或离子方程式。
(1)H2O2将碱性工业废水中的CN-氧化为碳酸盐和氨气的离子方程式:____________。
(2)硫化氢具有还原性,可以和许多氧化剂反应。在硫酸溶液中,H2S和KMnO4反应生成S、MnSO4、K2SO4和 H2O,写出该反应的化学方程式:________。
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2,写出该反应的离子方程式:__。
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:____。
(5)催化反硝化法中,H2能将![]() 还原为N2,反应进行一段时间后溶液呈碱性,写出该反应的离子方程式:________。
还原为N2,反应进行一段时间后溶液呈碱性,写出该反应的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:—CHO+ +H2O,由于醚键比较稳定故利用此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
+H2O,由于醚键比较稳定故利用此反应可保护醛基,也可以合成缩醛类有机物,下列说法中不正确的是( )
A.保护1mol醛基时也可用![]()
B.合成1mol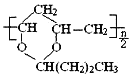 需要1mol
需要1mol![]() 和
和![]()
C.通过上述反应合成的![]() 其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3
其核磁共振氢谱中峰面积之比为1:1:1:1:1:2:2:3
D.![]() 可由
可由![]() 与
与![]() 通过上述反应得到
通过上述反应得到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、 Y、Z三种气体的物质的量随时间变化的曲线如图所示:

下列描述正确的是( )
A. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)-1
B. 反应开始到l0s,X的物质的量浓度减少了0.79mol/L
C. 反应开始到10s时,Y的转化率为79.0%
D. 反应的化学方程式为:X(g)+Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所学知识回答下列问题:
(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,ΔH1 ____ΔH2(填“>”、“<”或“=”,下同)。
(2)相同条件下,1 mol氮气和氢气反应断键吸收能量____形成2 mol氨气成键所放出的能量。
(3)已知常温时红磷比白磷稳定,比较下列反应中ΔH的大小:ΔH1___ΔH2。①P4(白磷,s)+5O2(g)= 2P2O5(s) ΔH1, ②4P(红磷,s)+5O2(g)= 2P2O5(s) ΔH2。
(4)25℃ 1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36 kJ热量,该反应的热化学方程式是_______。
(5)已知:0.5 mol CH4(g)与0.5 mol水蒸气在t℃、p kPa时,完全反应生成CO和H2的混合气体,吸收了a kJ热量,该反应的热化学方程式是_______。
(6)已知:C(s)+O2(g)=CO2(g) △H=-437.3kJmol﹣1,H2(g)+![]() O2(g)=H2O(g) △H=-285.8kJmol﹣1,CO(g)+
O2(g)=H2O(g) △H=-285.8kJmol﹣1,CO(g)+![]() O2(g)=CO2(g) △H=-283.0kJmol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=__kJmol﹣1。
O2(g)=CO2(g) △H=-283.0kJmol﹣1,煤的气化主要反应的热方程式C(s)+H2O(g)=CO(g)+H2(g) △H=__kJmol﹣1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z均为短周期主族元素,Y的原子序数是W和Z的原子序数之和的一半,Y原子的最外层电子数与核外电子总数之比为2:7;W和Z形成的可溶性化合物WZ溶于水中不能促进水的电离;W、X、Z三种元素形成的某种化合物能消毒杀菌.下列说法正确的是
A.四种元素原子中,原子半径最大的是Z
B.X、Y形成的化合物能溶于盐酸
C.最高价氧化物对应水化物的酸性:Z强于Y
D.1molW单质与足量X单质反应,转移的电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是

A. 放电时,a电极反应为
B. 放电时,溶液中离子的数目增大
C. 充电时,b电极每增重![]() ,溶液中有
,溶液中有![]() 被氧化
被氧化
D. 充电时,a电极接外电源负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用如图所示装置制取(必要时可加热)、净化、收集的气体是
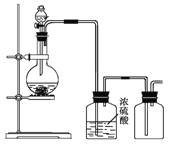
A.亚硫酸钠固体与硫酸反应制二氧化硫
B.氯化铵与氢氧化钙固体反应制氨气
C.锌和稀硫酸反应制氢气
D.铜与稀硝酸反应制一氧化氮
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com