
【题目】下列说法正确的是
A. 碳酸铵分解是吸热反应,根据焓判据判断能自发分解
B. 物质A三态间的转化如下:A(g)→A(l)→A(s),则该转化过程中ΔS>0
C. 反应2Mg(s)+CO2(g)![]() C(s)+2MgO(s)能自发进行,则该反应的ΔH<0
C(s)+2MgO(s)能自发进行,则该反应的ΔH<0
D. 室温下水结成冰是自发过程
科目:高中化学 来源: 题型:
【题目】下列递变规律正确的是
A. 钠、镁、铝、硅的还原性依次增强
B. P、S、Cl的原子半径依次增大
C. HCl、H2S、PH3的稳定性依次增强
D. Al(OH)3、Mg(OH)2、NaOH的碱性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)bZ(g),反应达到平衡后,测得X的转化率为50%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的 ![]() ,则a和b的数值可能是( )
,则a和b的数值可能是( )
A.a=1,b=1
B.a=2,b=1
C.a=2,b=2
D.a=3,b=3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)![]() 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:

下列说法中正确的是
A. 30~40 min间该反应使用了催化剂
B. 反应方程式中的x=1,正反应为吸热反应
C. 30 min时降低温度, 40 min时升高温度
D. 8 min前A的平均反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
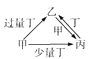
【题目】甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示,下列各组物质中不能按图示关系转化的是
选项 | 甲 | 乙 | 丙 | 丁 |
A | Ca(OH)2 | Ca(HCO3)2 | CaCO3 | CO2 |
B | FeCl3 | Fe | FeCl2 | Zn |
C | Fe | Fe(NO3)2 | Fe(NO3)3 | HNO3 |
D | SO2 | Na2SO3 | NaHSO3 | NaOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制100ml1.0mol/LNa2SO4溶液,正确的方法是
①将14.2gNa2SO4溶于100ml水中
②将32.2gNa2SO4·10H2O溶于少量水中,再用水稀释至100mL
③将20mL5.0 mol/LNa2SO4溶液用水稀释至100mL
A. ①② B. ①②③ C. ①③ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库.目前,世界各国都在研究如何充分利用海洋资源.全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mgL﹣1 . 其工业提取法有:
(1)空气吹出纯碱吸收法.方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴.该方法涉及的反应有:
①(写出离子方程式);
②3Br2+3CO32﹣═BrO3﹣+5Br﹣+3CO2↑;
③(写出离子方程式);
(2)空气吹出SO2吸收法.该方法基本同(1),只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴.写出溴与二氧化硫反应的化学方程式 .
(3)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢﹣水双温交换法”富集HDO.其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO.如图为“硫化氢﹣水双温交换法”所发生的两个反应中涉及的四种物质在反应体系中的物质的量随温度的变化曲线.写出100℃时所发生的反应的化学方程式;工业上富集HDO的生产过程中,可以循环利用的一种物质是 . 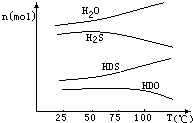
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下 转化为两种无毒气体E和F的方法(已知该反应△H<0). 在2 L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
| NO | CO | E | F |
初始 | 0.100 | 0.100 | 0 | 0 |
T1 | 0.020 | 0.020 | 0.080 | 0.040 |
T2 | 0.010 | 0.010 | 0.090 | 0.045 |
① 请结合上表数据,写出NO与CO反应的化学方程式________________________。
② 根据表中数据判断,温度T1和T2的关系是(填序号)_________________________。
A.T1>T2 B.T1<T2 C.T1=T2 D.无法比较
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g) ΔH= - 1266.8 kJ/mol,N2(g) + O2(g) = 2NO(g) ΔH = + 180.5kJ/mol,则氨催化氧化的热化学方程式为_________________。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
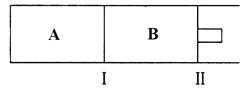
当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为_______________;保持温度和压强不变,向此容器中通入0.36molN2,平衡将_______________(填“正向”、“逆向”或“不”)移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com