
【题目】下列递变规律正确的是
A. 钠、镁、铝、硅的还原性依次增强
B. P、S、Cl的原子半径依次增大
C. HCl、H2S、PH3的稳定性依次增强
D. Al(OH)3、Mg(OH)2、NaOH的碱性依次增强
科目:高中化学 来源: 题型:
【题目】如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+2B(g)![]() xC(g)△H=﹣192kJmol﹣1,向M、N中都通入1mol A和2mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
xC(g)△H=﹣192kJmol﹣1,向M、N中都通入1mol A和2mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )

A. 若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N)
B. 若x>3,达到平衡后B的转化率关系为:α(M)>α(N)
C. 若x<3,C的平衡浓度关系为:c(M)>c(N)
D. x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是一种能量转换效率高、对环境友好的化学电源,图为一种氢氧燃料电池的结构装置. 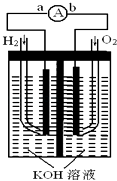
(1)电极b为该燃料电池的极(填“正”或“负”),电极方程式为;
(2)电池工作时,溶液中的OH﹣移向极(填“a”或“b”);
(3)电池工作时,在导线中电子流动方向为(用a、b表示);
(4)电池使用一段时间后,溶液的pH值(填“增大”或“减小”);
(5)当电池工作一段时间后消耗标准状况下H2为6.72L时,转移电子mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中一定量混合气体发生反应:xA(g)+yB(g) ![]() zC(g)平衡时测得A的浓度为0.5 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为0.2 mol·L-1,下列判断正确的是( )
zC(g)平衡时测得A的浓度为0.5 mol·L-1,保持温度不变,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为0.2 mol·L-1,下列判断正确的是( )
A. 平衡向正反应方向移动 B. x+y>z
C. C的体积分数保持不变 D. B的转化率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质特征是
A. 胶体粒子带电荷 B. 胶体粒子的直径在1~100nm之间
C. 胶体粒子能够发生布朗运动 D. 胶体粒子不能穿过半透膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 氧化还原反应的本质是元素化合价发生了改变
B. 物质所含元素化合价降低的反应是氧化反应
C. 有单质参加的化合反应一定是氧化还原反应
D. 还原剂在同一反应中既可以是反应物,也可以是生成物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物莫沙朵林(F)是一-种镇痛药,它的合成路线如下:

(1)A![]() B的转化属于______________反应(填反应类型),1mol B与足量的金属钠反应可以生成标况下的氢气_________L,B的沸点远高于相对分子质量接近的烃类,其原因是_______。
B的转化属于______________反应(填反应类型),1mol B与足量的金属钠反应可以生成标况下的氢气_________L,B的沸点远高于相对分子质量接近的烃类,其原因是_______。
(2)化合物D中含氧官能团的名称为__________
(3)化合物C与新制氢氧化铜悬浊液反应的化学方程式为____________
(4)下列有关化合物E的说法中正确的是__________(填序号)。
A.化合物E的分子式为C9H12O3
B.化合物E能使酸性KMnO4溶液和溴水褪色
C.1mol E发生加成反应最多消耗2 mol H2
D.E中既有非极性共价键也有极性共价键
(5)写出同时满足下列条件的E的一种同分异构体的结构简式:__________;
I.分子的核磁共振氢谱图中有4组峰;
Ⅱ.能发生银镜反应和水解反应;
Ⅲ.能与FeCl3溶液发生显色反应,且与溴水反应。
1mol该同分异构体与足量NaOH溶液反应,最多可消耗________molNaOH。
(6)已知E+X![]() F为加成反应,则化合物X的结构简式为__________。
F为加成反应,则化合物X的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热.
化学键 | Si﹣O | Si﹣Cl | H﹣H | H﹣Cl | Si﹣Si | Si﹣C |
E(kJmol﹣1) | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) ![]() Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi﹣Si键),该反应的产生的热量为( )
Si(s)+4HCl(g),(已知1mol晶体Si中有2molSi﹣Si键),该反应的产生的热量为( )
A.吸收412 kJmol﹣1
B.放出412 kJmol﹣1
C.吸收236 kJmol﹣1
D.放出236 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 碳酸铵分解是吸热反应,根据焓判据判断能自发分解
B. 物质A三态间的转化如下:A(g)→A(l)→A(s),则该转化过程中ΔS>0
C. 反应2Mg(s)+CO2(g)![]() C(s)+2MgO(s)能自发进行,则该反应的ΔH<0
C(s)+2MgO(s)能自发进行,则该反应的ΔH<0
D. 室温下水结成冰是自发过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com