
【题目】燃料电池是一种能量转换效率高、对环境友好的化学电源,图为一种氢氧燃料电池的结构装置. 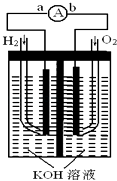
(1)电极b为该燃料电池的极(填“正”或“负”),电极方程式为;
(2)电池工作时,溶液中的OH﹣移向极(填“a”或“b”);
(3)电池工作时,在导线中电子流动方向为(用a、b表示);
(4)电池使用一段时间后,溶液的pH值(填“增大”或“减小”);
(5)当电池工作一段时间后消耗标准状况下H2为6.72L时,转移电子mol.
【答案】
(1)正;O2+2H2O+4e﹣=4OH﹣
(2)a
(3)a流向b
(4)减少
(5)0.6
【解析】解:(1.)电极b通入氧气,为该燃料电池的正极,电极方程式为O2+2H2O+4e﹣=4OH﹣ , 故答案为:正;O2+2H2O+4e﹣=4OH﹣;
(2.)原电池中阴离子向负极移动,溶液中的OH﹣移向a,故答案为:a;
(3.)电子流动由负极流向正极,所以由a流向b,故答案为:a流向b;
(4.)总的反应式为:O2+2H2=2H2O,生成水溶液浓度变稀,所以溶液的PH减小,故答案为:减少;
(5.)产生标准状况下H2 为6.72L,所以物质的量为 ![]() =0.3mol,生成1mol的氢气转移2mol的电子,所以转移电子的物质的量为:0.3mol×2=0.6mol,故答案为:0.6.
=0.3mol,生成1mol的氢气转移2mol的电子,所以转移电子的物质的量为:0.3mol×2=0.6mol,故答案为:0.6.
(1)电极b通入氧气,为该燃料电池的正极,电极方程式为O2+2H2O+4e﹣=4OH﹣;(2)原电池中阴离子向负极移动;(3)电子流动由负极流向正极;(4)总的反应式为:O2+2H2=2H2O,生成水溶液浓度变稀;(5)产生标准状况下H2 为6.72L,所以物质的量为 ![]() =0.3mol,生成1mol的氢气转移2mol的电子.
=0.3mol,生成1mol的氢气转移2mol的电子.


科目:高中化学 来源: 题型:
【题目】下列反应中乙醇分子断裂的仅是碳氧键的是( )
A.乙醇与金属钠反应产生氢气
B.乙醇在浓硫酸140℃条件下反应
C.乙醇与氢卤酸发生取代反应生成卤代烃
D.乙醇在酸性重铬酸钾的氧化下生成乙醛或乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关平衡常数K的说法正确的是
A. 已知碳酸: K1=4.4×10-7,K2=4.7×10-11,次氯酸: K1=2.98×10-8,碳酸钠溶液中滴加少量氯水的离子方程式为: CO32-+Cl2+H2O=HCO3-+Cl-+HClO
B. 1.0mol/LNH4HCO3溶液pH=8.0。由此可知Ka1(H2CO3)> Kb(NH3·H2O)>Ka2(H2CO3)
C. 常温下电离常数为Ka 的酸HA溶液中c(H+)= ![]()
D. 将0.1mol/LMgSO4溶液滴入NaOH 溶液中至不再有沉淀产生,再滴加0.1mo/LCuSO4溶液,白色沉淀变为蓝色沉淀,可得出Ksp[Cu(OH)2]sp[Mg(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Co2O3在酸性溶液中易被还原成Co2+;②Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。则下列在水溶液中的反应不可能发生的是( )
A. 3Cl2+6FeI2===2FeCl3+4FeI3B. Cl2+FeI2===FeCl2+I2
C. Co2O3+6HCl===2CoCl2+Cl2↑+3H2OD. 2Fe3++2I-===2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了进一步提高合成氨的生产效率,科研中具有开发价值的是( )
A.研制高温下活性较大的催化剂
B.寻求NH3的新来源
C.研制低温下活性较大的催化剂
D.研制耐高温高压的新型材料建造合成塔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、油脂、蛋白质都是人体必需的营养物质。
①油脂被摄入人体后.在酶的作用下水解为高级脂肪酸和_____(写名称).进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料.
②氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—N H2)和_______(写结构简式).
③淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6 ),写出相应的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以获得淡水、食盐并可提取镁和溴等物质.
(1)海水淡化的方法主要有(填一种);
(2)下列物质不需要经过化学变化就能从海水中获得的物质是 (填序号);
A.液溴
B.食盐
C.氢气
D.淡水
(3)从海水中提取溴和镁的流程如下: 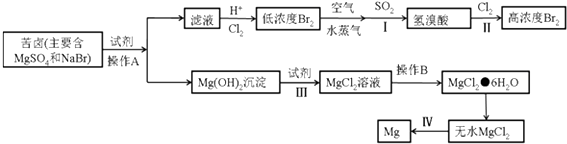
①写出下列步骤的离子方程式或化学方程式
步骤I的化学方程式: ,
步骤III的离子方程式: ,
步骤IV的化学方程式: .
②操作A是 , 操作B是 , 从步骤II得到的溶液中提取溴还需要进行的操作有:、萃取、蒸馏.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律正确的是
A. 钠、镁、铝、硅的还原性依次增强
B. P、S、Cl的原子半径依次增大
C. HCl、H2S、PH3的稳定性依次增强
D. Al(OH)3、Mg(OH)2、NaOH的碱性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)bZ(g),反应达到平衡后,测得X的转化率为50%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的 ![]() ,则a和b的数值可能是( )
,则a和b的数值可能是( )
A.a=1,b=1
B.a=2,b=1
C.a=2,b=2
D.a=3,b=3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com