
【题目】用间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图所示,质子膜允许H+和H2O通过。下列说法正确的是
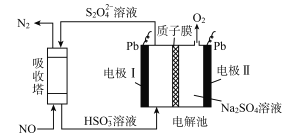
A. 电极I为阴极,电极反应式为2H2O+2e-=2OH-+H2↑
B. 电解时H+由电极I向电极II迁移
C. 吸收塔中的反应为2NO+2S2O42-+2H2O=N2+4HSO3-
D. 每处理1molNO,可同时得到32gO2
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】学习化学可以防止走入生活和学习的误区.你认为下列说法不正确的是( )
A.水银不是银,而是金属汞
B.纯碱不是碱,而是盐
C.干冰不是冰,而是固体二氧化碳
D.烧碱不是碱,而是一种常见的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,向x g KNO3不饱和溶液中加入a g KNO3或蒸发掉b g水,恢复到t ℃,溶液均达到饱和,据此,下列推论不正确的是( )
A. 在t ℃时,KNO3的溶解度为![]() g
g
B. 若原溶液中溶质的质量分数为![]() ,则x=2b
,则x=2b
C. 在t ℃时,所配的KNO3溶液中溶质的质量分数为w≤![]() %
%
D. 若将原溶液蒸发掉2b g水,恢复到原温度析出2a g KNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为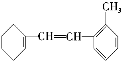
据此填写下列空格。
(1)该物质苯环上一氯代物有________种;
(2)1 mol该物质和溴水混合,消耗Br2的物质的量为________mol;
(3)1 mol该物质和H2加成需H2________mol;
(4)下列说法不正确的是________。
A.该物质可发生加成、取代、氧化等反应
B.该物质与甲苯属于同系物
C.该物质使溴水褪色的原理与乙烯相同
D.该物质使酸性KMnO4溶液褪色发生的是加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,不能按 ![]() (“→”表示反应一步完成)关系转化的是( )
(“→”表示反应一步完成)关系转化的是( )
选项 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | NaOH | NaHCO3 | Na2CO3 |
C | Al | Al(OH)3 | Al2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下面的方案进行某些离子的检验,其中方案设计严密的是
A. 检验试液中的SO42-![]()
B. 检验试液中的Fe2+![]()
C. 检验试液中的I-![]()
D. 检验试液中的CO32-![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化镓是继硅之后研究最深入、应用最广泛的半导体材料。回答下列问题:
(1)Ga基态原子核外电子排布式为__________________,As基态原子核外有____个未成对电子。
(2)Ga、As、Se的第一电离能由大到小的顺序是___________,Ga、As、Se的电负性由大到小的顺序是_________________。
(3)比较下列镓的卤化物的熔点和佛点,分析其变化规律及原因:_________________。
镓的卤化物 | GaI3 | GaBr3 | GaCl3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是______________。
(4)二水合草酸镓的结构如图1所示,其中镓原子的配位数为___________,草酸根中碳原子的杂化轨道类型为______________。

(5)砷化镓的立方晶胞结构如图2所示,晶胞参数为a=0.565nm,砷化镓晶体的密度为_____g/cm3(设NA为阿伏加德罗常数的值,列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料。
(1)写出实验室制取氯气反应的化学方程式________________________。
(2)资料显示:Ca(ClO)2 +CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
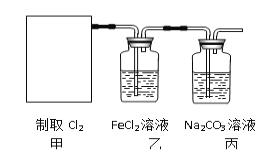
①在该实验中,甲部分的装置是_______(填字母)。
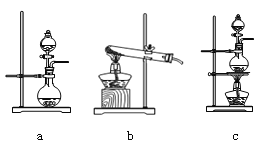
②乙装置中FeCl2溶液与Cl2反应的离子方程式是________________。
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质,这种物质是_______(化学式)。
④有人认为该实验存在明显的缺陷,如何改进:______________
请你写出Cl2和“④”中“最合适的化学试剂”反应的离子方程式______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com