
����Ŀ������(Ni��Cd)�ɳ�������ִ��������й㷺Ӧ�á���֪ij���ӵ�صĵ������ҺΪKOH��Һ����䡢�ŵ簴��ʽ���У�
Cd��2NiO(OH)��2H2O![]() Cd(OH)2��2Ni(OH)2
Cd(OH)2��2Ni(OH)2
�йظõ�ص�˵����ȷ����( )
A. ���ʱ������Ӧ��Ni(OH)2��e����OH��===NiO(OH)��H2O
B. �������ǻ�ѧ��ת��Ϊ���ܵĹ���
C. �ŵ�ʱ����������Һ�ļ��Բ���
D. �ŵ�ʱ�������Һ�е�OH���������ƶ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W�����ڱ��е����λ����ͼ��ʾ������WԪ�ص�ԭ�ӽṹʾ��ͼΪ![]() ��
��
W | X | Y |
Z |
��ش��������⣺
��1��ZԪ����Ԫ�����ڱ��е�λ����___________��
��2��X��Y��Z����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳��Ϊ___________��Ԫ�ط��ű�ʾ����
��3��X��Z��W����Ԫ�ص�����������Ӧˮ�����������ǿ����___________���û�ѧʽ��ʾ����
��4���õ���ʽ��ʾWY2���γɹ��̣�___________��
��5��д��W������Ũ���ᷴӦ�Ļ�ѧ����ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ��֬������ʹ��ˮ��ɫ
B. �����������Ի���������ᡢ�Ӧ������
C. �������ֿ�����ʳƷ������
D. ���Ǻ���ѿ�ǵ�ˮ����ﶼ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ��ԭ���ԭ�������˶��ֵ�أ������㲻ͬ����Ҫ������ÿС���еĵ�ع㷺ʹ�����ճ���������Ϳ�ѧ�����ȷ��棬����������ṩ����Ϣ����д�ո�
(1)Ǧ�����ڷŵ�ʱ�����ĵ�ط�ӦʽΪ��Pb��PbO2��2H2SO4===2PbSO4��2H2O��
�����缫��ӦʽΪ______________��
(2)FeCl3��Һ�����ڸ�ʴӡˢ��·ͭ�壬����2FeCl3��Cu===2FeCl2��CuCl2�������˷�Ӧ��Ƴ�ԭ��أ������õ缫����Ϊ_____________������·��ת��0.2 mol����ʱ����ʴͭ������Ϊ_____________g��
(3)����Ƭ��ͭƬ�õ���������һ�����Ũ�����У�һ������ռ���Һ�У��ֱ��γ���ԭ��أ���������ԭ����У������ֱ�Ϊ______________��
A����Ƭ��ͭƬ B��ͭƬ����Ƭ C����Ƭ����Ƭ
(4)ȼ�ϵ����һ�ָ�Ч�������ѺõĹ���װ�ã���ͼ�ǵ����Ϊϡ������Һ������ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺

������ȼ�ϵ�ص��ܷ�Ӧ��ѧ����ʽ�ǣ�________________��
�ڵ�ع���һ��ʱ���������Һ��Ũ��_____________(���������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2012��6��16��18ʱ37��24�룬���۾źųɹ����䡣�ɴ���������������̫���ܵ�أ������ڲ������и�Ч��MCFC��ȼ�ϵ�ء���ȼ�ϵ�ؿ�ͬʱ��Ӧ���ˮ������������ȼ��Ϊ�����������Ϊ���ڵ�̼��ء���֪��ȼ�ϵ�ص��ܷ�ӦΪ2H2��O2===2H2O��������ӦΪH2��CO![]() ��2e��===CO2����H2O���������ƶ���ȷ����( )
��2e��===CO2����H2O���������ƶ���ȷ����( )
A.��ع���ʱ��CO![]() ���ƶ�
���ƶ�
B.��طŵ�ʱ�����Ӿ����·��ͨ��������������ͨ�����ĸ���
C.�����ĵ缫��ӦʽΪ4OH����2e��===O2����2H2O
D.ͨ�����ĵ缫Ϊ����������������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ����ʽ̼����MgaAlb(OH)c(CO3)d��xH2O��һ�ֲ�����ˮ����������ȼ���������ȷֽ�����е�MgO��Al2O3�۵�ϸ��Ҷ���ȼ�գ�����ȼ���á����������գ�
��1�����þ����ʽ̼���ε����ַǽ���Ԫ�ص�ԭ�Ӱ뾶��С�����˳����______________��̼ԭ�����������Ų�ʽ��________________����ԭ�Ӻ�����_________��������ͬ�ĵ��ӡ�
��2����MgaAlb(OH)c (CO3)d��x H2O��ʾ�����������ʽ��2aMgO��bAl2O3��2dCO2����________��H2O��
��3����̿��ʯӢ�������ڵ������з������·�Ӧ����ҵ�Ͽ��ɴ��Ƶ�һ�������մɲ��ϵ�����(Si3N4)��3SiO2(s)��6C(s)��2N2(g)![]() Si3N4(s)��6CO(g) + Q (Q>0)��
Si3N4(s)��6CO(g) + Q (Q>0)��
�ٸ÷�Ӧ��������������________________________������÷�Ӧ����4.48 L CO���壨��״���£�����ת�Ƶĵ��ӵ����ʵ���Ϊ_____________��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽK=_____________________________���������¶ȣ�Kֵ____________(���������С�����䡱)��
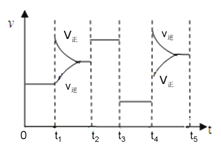
�۸÷�Ӧ�������뷴Ӧʱ��Ĺ�ϵ����ͼ��ʾ��t4ʱ���������淴Ӧ���ʱ仯��ԭ����___________________________��д��һ�ּ��ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���ӦA2(g)+B2(g)![]() 2AB(g)�ﵽ�ȵı�־�ǣ� ��
2AB(g)�ﵽ�ȵı�־�ǣ� ��
A. ��λʱ��������n mol A2ͬʱ����n mol AB
B. �����ڵ������ʵ�������ʱ��仯
C. ��λʱ��������2n mol AB��ͬʱ����n mol B2
D. ��λʱ��������n mol A2��ͬʱ����n mol B2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�����ᴿ���ʵķ�����ȷ���ǣ� ��
A.������ķ�����ȡ����ˮ
B.�ù��˵ķ�����ȥNaCl��Һ�к��е��������۽���
C.���ܽ⡢���˵ķ����ᴿ��������BaSO4��BaCO3
D.�ü��ȡ������ķ������Գ�ȥCaCl2��MgCl2������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���� ( )
A.O2���Ӽ�����ŷǼ��Թ��ۼ�B.CO2�����ڴ����ż��Թ��ۼ�
C.SO2��H2O��Ӧ�IJ��������ӻ�����D.�����к���H+��Cl-,��HClΪ���ӻ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com