
����Ŀ����ⷨ��ȡ�й㷺��;��Na2FeO4,ͬʱ��ȡ����:Fe+2H2O+2OH-![]() FeO42-+3H2��,����ԭ����ͼ(a)��ʾ,�������ҺΪ����������Һ,������������ҺŨ�ȹ���,���缫����������ɫɫ���ʡ�C(Na2FeO4)���ʼC(NaOH)�ı仯��ͼ(b)��ʾ����֪Na2FeO4ֻ��ǿ�����������ȶ�,�ױ�H2��ԭ������˵������ȷ����
FeO42-+3H2��,����ԭ����ͼ(a)��ʾ,�������ҺΪ����������Һ,������������ҺŨ�ȹ���,���缫����������ɫɫ���ʡ�C(Na2FeO4)���ʼC(NaOH)�ı仯��ͼ(b)��ʾ����֪Na2FeO4ֻ��ǿ�����������ȶ�,�ױ�H2��ԭ������˵������ȷ����
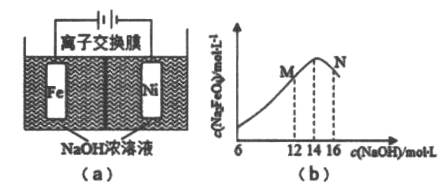
A. ���һ��ʱ���,������c(OH-)����
B. ��·�о���0.2mol����ʱ,����������H2 2.24L(��״��)
C. M��C(Na2FeO4)�������ֵ��ԭ�������缫����Fe(OH)3����
D. �����ĵ缫��Ӧ:Feһ6e-+8OH-===FeO42-+4H2O
���𰸡�C
���������������⣬�����Դ�����������������ص�������������ӦʽΪ��Fe-6e-+8OH-=FeO![]() +4H2O���������У�����������OH-��c(OH)���ͣ�A��ȷ�����缫�����ݲ�����������ӦʽΪ��2H2O+2e-=H2��+2OH-����·�о���0.2mol����ʱ,����������H2 2.24L(��״��)��B��ȷ����������Na2FeO4ֻ��ǿ�����������ȶ�����M�㣬c(OH-)�ͣ�Na2FeO4�ȶ��Բ�ҷ�Ӧ��������M��C(Na2FeO4)�������ֵ��C���������缫����������Ӧ��������ӦʽΪ��Fe-6e-+8OH-=FeO
+4H2O���������У�����������OH-��c(OH)���ͣ�A��ȷ�����缫�����ݲ�����������ӦʽΪ��2H2O+2e-=H2��+2OH-����·�о���0.2mol����ʱ,����������H2 2.24L(��״��)��B��ȷ����������Na2FeO4ֻ��ǿ�����������ȶ�����M�㣬c(OH-)�ͣ�Na2FeO4�ȶ��Բ�ҷ�Ӧ��������M��C(Na2FeO4)�������ֵ��C���������缫����������Ӧ��������ӦʽΪ��Fe-6e-+8OH-=FeO![]() +4H2O��D��ȷ����ȷѡ��C��
+4H2O��D��ȷ����ȷѡ��C��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�����ڱ��ж����ڵ�һ���֣�A��B��C����Ԫ��ԭ�Ӻ���ĵ�����֮�͵���Bԭ�ӵ���������Bԭ�Ӻ��ڵ�����������������ȡ�������������ȷ���ǣ� ��
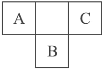
A. ����Ԫ�ص�ԭ�Ӱ뾶�Ĵ�С˳����B��C��A
B. AԪ������������Ӧ��ˮ�������ǿ������
C. BԪ�ص�������⻯���ˮ��Һ��������
D. CԪ���Ƿǽ�������ǿ��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ण�������ʹ������������Ѫ�ܼ�����һ��ҩ�Ŀǰ��������ͼ��ʾ�ĺϳ�·������ȡ��

��1��B ��ϵͳ����Ϊ________��C �к��еĺ�������������Ϊ________��
��2����Ӧ�ڵķ�Ӧ����Ϊ_____��Ӧ��
��3�������л���ķ��࣬������ि�����______������ĸ��ţ���
A.���� B.���� C.�߷��ӻ����� D.���� E.�����廯����
��4��д�����·�Ӧ�Ļ�ѧ����ʽ��
��____________________
��____________________
��5�������� I �� B ��ͬϵ���Է��������� B �� 14��I �ж���ͬ���칹�壬����������������������_________�֡�
a.����̼��������Һ��Ӧ�ų����� b.����һ NH2 c.���ڷ����廯����
(6��д���Ա����ᡢ�Ҵ�����������Ϊԭ�Ϻϳ�����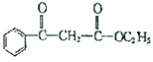 ������ͼ������������ԭ����ѡ����(����
������ͼ������������ԭ����ѡ����(���� )______________________________��
)______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ָ����(C5H8)nͨʽ�������Լ��䲻ͬ���ͳ̶Ⱥͺ�����������,�㷺�����ڶ�ֲ�����ڡ��������л���a��b�����������,�й����ǵ�˵������ȷ����
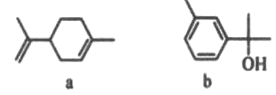
A. b�ķ���ʽΪC10H14O
B. a����Ԫ���ϵ�һ�ȴ��ﹲ��5��(�����������칹)
C. a��b����������̼ԭ�Ӿ�����ͬһƽ����
D. ��������ˮ������a��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(Mo)��һ����Ҫ�Ĺ��ɽ���Ԫ��,�������ϼ�Ϊ+6��+5��+4,������㷺����ұ�𡢻�е���졢���ӡ�������һЩ�߿Ƽ�����������(Na2MoO4)��һ����������ȴˮϵͳ�Ľ�����ʴ��,Ҳ����������������ī�����ʡ�������ϵȡ���ͼ�ǻ����������Ʊ�������������Ƶ���Ҫ����ͼ,��֪�⾫�����Ҫ�ɷ�ΪMoS2,����������ˮ��
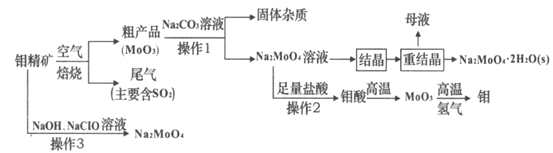
(1)MoS2����ʱ��Ӧ�Ļ�ѧ����ʽΪ________��������β���Ի�������ҪΣ����_______��
(2)����1��,�ֲ�Ʒ�е�MoO3��Na2CO3��Һ��ַ�Ӧ��,����Na2MoO4������һ������,�����ʵĵ���ʽΪ_____���ֲ�Ʒ������ּ�������õļ��Һ�в������ӵ�Ũ��:c(MoO42-)=0.40mol��L-1��c(SO42-)=0.05mol��L-1���ᾧǰӦ�ȳ�ȥSO42-,�����Ǽ���Ba(OH)2���塣�������Ba(OH)2�������Һ�������,��BaMoO4,��ʼ����ʱ,SO42-��ȥ����Ϊ___����֪:Ksp(BaSO4)=1.1��10-10,Ksp(BaMoO4)=4.0��10-8
(3)�������в���2Ϊ����,�����ʵ����ģ��ò���ʱ,������Һ������������,��ʵ������ĽǶȷ���,���ܵ�ԭ����_______________________________��
(4)�ؽᾧ�õ���ĸҺ�������´��ؽᾧʱ�ظ�ʹ��,���ﵽһ����������뾻������,ԭ��______________________________________��
(5)��ҵ����MoO3�Ʊ�Mo��Ҳ�������ȷ�Ӧ,д���÷�Ӧ�ķ���ʽ_______________��
(6)����3�ڼ���������,���⾫����뵽������NaC1O��Һ��,Ҳ�����Ʊ������ơ��÷�Ӧ�����ӷ���ʽΪ___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2SO2(g)��O2(g)![]() 2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2(g)����Ϊ1 mol SO3(g)����H����99 kJ��mol��1����ش��������⣺
2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol SO2(g)����Ϊ1 mol SO3(g)����H����99 kJ��mol��1����ش��������⣺
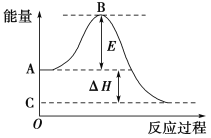
��1��ͼ��A���ʾ��___________, B���ʾ��__________��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ��________(����������������)Ӱ�졣
��2��ͼ����H��________kJ��mol��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1mol������������ȫȼ������ˮ�����ų�241.8ǧ�������������Ȼ�ѧ����ʽ��ȷ����
A. 2H2��g��+O2��g����2H2O��g��+241.8kJ
B. H2��g��+1/2O2��g����H2O��s��+241.8 kJ
C. H2��g��+1/2O2��g����H2O��g��-241.8 kJ
D. H2O��g����H2��g��+1/2O2��g��-241.8 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ(1)��ͼ(2)��A��B�������ʵĺ˴Ź������ס���֪A��B�������ʶ������࣬������6����ԭ�ӡ������ͼ(1)��ͼ(2)�������ʵĺ˴Ź�������ͼѡ�����������ͼ(1)��ͼ(2)���������� (�� ��)
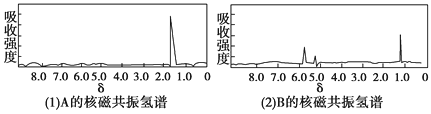
A. A��C3H6��B��C3H6 B. A��C6H6��B��C4H10
C. A��C3H8��B��C6H6 D. A��C3H6��B��C2H6
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com