
【题目】下面图(1)和图(2)是A、B两种物质的核磁共振氢谱。已知A、B两种物质都是烃类,都含有6个氢原子。请根据图(1)和图(2)两种物质的核磁共振氢谱图选择出可能属于图(1)和图(2)的两种物质 ( )
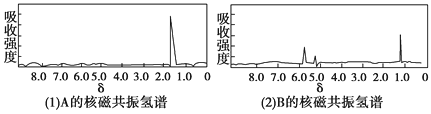
A. A是C3H6;B是C3H6 B. A是C6H6;B是C4H10
C. A是C3H8;B是C6H6 D. A是C3H6;B是C2H6
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】电解法制取有广泛用途的Na2FeO4,同时获取氢气:Fe+2H2O+2OH-![]() FeO42-+3H2↑,工作原理如图(a)所示,电解质溶液为氢氧化钠溶液,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色色物质。C(Na2FeO4)随初始C(NaOH)的变化如图(b)所示。已知Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法不正确的是
FeO42-+3H2↑,工作原理如图(a)所示,电解质溶液为氢氧化钠溶液,若氢氧化钠溶液浓度过高,铁电极区会产生红褐色色物质。C(Na2FeO4)随初始C(NaOH)的变化如图(b)所示。已知Na2FeO4只在强碱性条件下稳定,易被H2还原。下列说法不正确的是
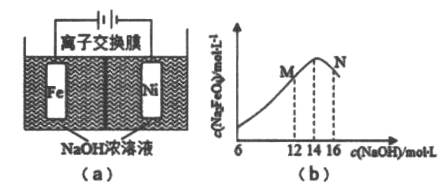
A. 电解一段时间后,阳极室c(OH-)降低
B. 电路中经过0.2mol电子时,阴极室生成H2 2.24L(标准状况)
C. M点C(Na2FeO4)低于最高值的原因是铁电极上有Fe(OH)3生成
D. 阳极的电极反应:Fe一6e-+8OH-===FeO42-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和反应速率的测定。将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
(1)可以判断该分解反应已经达到平衡的是________。
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
E.单位时间内消耗1 molNH2COONH4 ,同时生成2mol NH3
F.密闭容器中混合气体的平均摩尔质量不变 G.容器内NH3与CO2的浓度之比为2∶1 H.6个N—H键断裂的同时,有2个C=O键形成
(2)根据表中数据,计算25.0 ℃时的分解平衡常数______________。
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量________(填“增加”、“减少”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定一种气态烃A的化学式,取一定量的A置于一密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气。学生甲、乙设计了两个方案,均认为根据自己的方案能求出A的最简式,他们测得的在一定条件下的有关数据如下(图中的箭头表示气流的方向,实验前系统内的空气已排尽):
甲方案:燃烧产物![]() 浓硫酸增重2.52 g
浓硫酸增重2.52 g![]() 碱石灰增重1.32g
碱石灰增重1.32g![]() 生成CO21.76 g
生成CO21.76 g
乙方案:燃烧产物![]() 碱石灰增重5.60 g
碱石灰增重5.60 g![]() 固体减小0.64 g
固体减小0.64 g![]() 石灰水增重4g。试回答:
石灰水增重4g。试回答:
(1)甲、乙两方案中,你认为哪种方案能求出A的最简式_______?
(2)请根据你选择的方案,通过计算求出A的最简式_______。(要求写出计算过程)
(3)若要确定A的分子式,是否需要测定其它数据?并说明原因_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面:锂混杂于其中。(已知Co2O3的氧化性>Cl2的氧化性)从废料中回收氧化钴(CoO)的工艺流程如下:
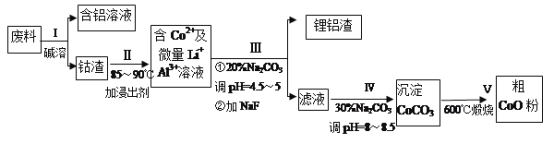
已知:①CoCO3的溶度积为:Ksp=1.0×10-13;
②溶液中离子浓度小于1.0×10-5mol/L时认为该离子沉淀完全。
(1)“碱溶”前通常将废料粉碎,其目的是____________。
(2)过程I中采用NaOH溶液溶出废料中的A1,反应的离子方程式为_________________。
(3)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出含钻物质的反应化学方程式为 (产物中只有一种酸根) _______________________________________。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请分析不用盐酸浸出钴的主要原因______________________________________。
(4)过程III得到锂铝渣的主要成分是LiF和AI(OH)3,碳酸钠溶液在产生 Al(OH)3时起重要作用,请写出该反应的离子方程式__________________________________。
(5)将2.0×10-4 mol/LCoSO4与2.2×10-4mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为__________,Co2+是否沉淀完全? __________(填“是”或“否”)。
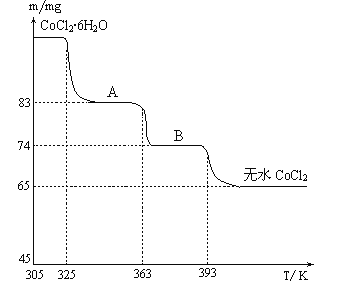
(6)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,物质B的化学式是____________________。
【答案】 略 略 略 略 略 略 略 略
【解析】(1). “碱溶”前通常将废料粉碎,可以增大固体反应物的接触面积,加快反应速率,故答案为:增大反应物接触面积,加快反应速率;
(2). NaOH溶液和Al反应生成偏铝酸钠和氢气,离子方程式为:2A1+2OH-+2H2O=2A1O2-+3H2↑,故答案为:2A1+2OH-+2H2O=2A1O2-+3H2↑;
(3). 废料中钴以Co2O3·CoO的形式存在,钴的化合价为+2价和+3价,由流程图可知,加入Na2S2O3溶液后,钴全部变为+2价,说明Co3+氧化S2O32-,还原产物为Co2+,由产物中只有一种酸根离子可知氧化产物为SO42-,根据得失电子守恒和原子守恒,浸出含钴物质的反应化学方程式为:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O,由题中信息可知,Co2O3的氧化性>Cl2的氧化性,则Co2O3·CoO可氧化盐酸产生Cl2,污染环境,所以实际工业生产中不用盐酸浸出含钴物质,故答案为:4Co2O3·CoO+Na2S2O3+11H2SO4=12CoSO4+Na2SO4+11H2O;Co2O3·CoO可氧化盐酸产生Cl2,污染环境;
(4). 在过程III中加入碳酸钠溶液,碳酸根离子和铝离子发生双水解反应生成氢氧化铝沉淀,离子方程式为:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑,故答案为:2A13++3CO32-+3H2O=2A1(OH)3↓+3CO2↑;
(5). 将2.0×10-4mol/LCoSO4与2.2×10-4mol/L的Na2CO3等体积混合,Co2+与CO32-反应生成CoCO3,离子方程式为:Co2++ CO32-= CoCO3,由离子方程式可知,反应后的溶液中c(CO32-)=( 2.2×10-4-2.0×10-4)mol/L÷2=1×10-5mol/L,则反应后的溶液中c(Co2+)=![]() =1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案为:1.0×10-8mol/L;是;
=1.0×10-8mol/L,c(Co2+)<1.0×10-5mol/L,所以Co2+沉淀完全,故答案为:1.0×10-8mol/L;是;
(6). 据图可知,n(CoCl2)=65×10-3g÷130g/mol=5×10-4mol,B中含有水的物质的量为n(H2O)=(74-65)×10-3g÷18g/mol=5×10-4mol,则n(CoCl2): n(H2O)=1:1,则物质B为CoCl2·H2O,故答案为:CoCl2·H2O。
【题型】综span>合题
【结束】
10
【题目】砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。
(1)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O3转化为As2O5的热化学方程式__________________________________。
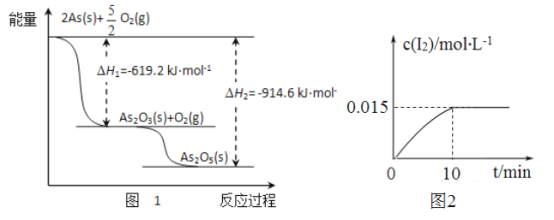
(2)砷酸钠具有氧化性,298K时,在100mL烧杯中加入10mL0.1 mol/L Na3AsO4溶液、20mL0.1 mol/L KI溶液和20mL0.05mol/L硫酸溶液,发生下列反应:AsO43-(无色)+12(浅黄色)+H2O △H。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
①升高温度,溶液中AsO43-的平衡转化率减小,则该反应的△H________0(填“大于”“小于”或“等于”)。
②0~10min内,I的反应速率v(Iˉ)= ____________。
③下列情况表明上述可逆反应达到平衡状态的是_______(填字母代号)。
a.c(AsO33-)+c(AsO42-)不再变化 b.溶液颜色保持不再变化
C.c(AsO33-)与c(AsO42-)的比值保持不再变化 d.I的生成速率等于I2的生成速率
④在该条件下,上述反应平衡常数的表达式K=______________。
(3)利用(2)中反应可测定含As2O3和As2O5的试样中的各组分含量(所含杂质对测定无影响),过程如下:
①将试样02000g溶于NaOH溶液,得到含AO33-和AsO43-的混合溶液。
②上述混合液用0.02500 mol·L-1的I2溶液滴定,用淀粉试液做指示剂,当________________,则滴定达到终点。重复滴定3次,平均消耗I2溶液40.00mL。则试样中As2O5的质量分数是_________(保留四位有效数字)。若滴定终点时,仰视读数,则所测结果_________ (填“偏低”,“偏高”,“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
(1)丙烷脱氢可得丙烯. 已知:C3H8(g)=CH4(g)+HC≡CH(g)+H2(g);△H1=+156.6kJmol﹣1
CH3CH=CH2(g)=CH4(g)+HC≡CH(g);△H2=+32.4kJmol﹣1
则相同条件下,反应C3H8(g)=CH3CH=CH2(g)+H2(g)的△H=kJmol﹣1
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2 , 负极通入丙烷,电解质是熔融碳酸盐.电池总反应方程式;放电时,CO32﹣移向电池的 (填“正”或“负”)极.
(3)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10﹣5 mol/L.若忽略水的电离及H2CO3的第二级电离,则H2CO3HCO3﹣+H+的平衡常数K1= . (已知:10﹣5.60=2.5×10﹣6)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁盐、铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用,现用铁屑与硫酸反应制备硫酸亚铁。
已知:①4Fe2++O2+4H+===4Fe3++2H2O
②硫酸亚铁在水中的溶解度如下图:
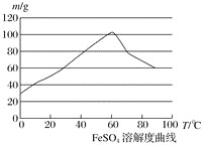
(1)首先,将铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。此步骤中,分离出液体的方法通常不用过滤,使用的操作是____________(填写操作名称)。
(2)向处理过的铁屑中加入适量的硫酸,在一定温度下使其反应到不再产生气体,趁热过滤,得硫酸亚铁溶液。
①硫酸浓度应选择(填字母序号)__________;
A.浓硫酸 B.10 moL·L-1硫酸
C.3 moL·L-1硫酸 D.任意浓度硫酸
②温度宜控制在________,加热的同时需适当补充水,原因是___________________;
③反应中应保持![]() _________ (填“<”“>”或“=”) 1。
_________ (填“<”“>”或“=”) 1。
(3)亚铁盐在空气中易被氧化,但形成复盐可稳定存在,如“摩尔盐”,即(NH4)2SO4·FeSO4·6H2O(硫酸亚铁铵),就是在硫酸亚铁溶液中加入少量稀硫酸溶液,再加入饱和硫酸铵溶液,经过_______、_______、_______、_______等一系列操作后所得。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com