
【题目】在探究新制饱和氯水成分的实验中,下列实验现象或结论不正确的是( )
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D.向氯水中滴加紫色石蕊,溶液颜色变成红色,说明氯水中含有HClO
【答案】D
【解析】
氯水中存在平衡Cl2+H2O![]() HCl+HClO,氯气为黄绿色,因此氯水中因含有Cl2而呈浅黄绿色,溶液中含有Cl-,与硝酸银反应生成AgCl白色沉淀;氯水呈酸性,含有H+,能与NaHCO3反应生成CO2;氯水中有HClO存在,因此具有漂白性。
HCl+HClO,氯气为黄绿色,因此氯水中因含有Cl2而呈浅黄绿色,溶液中含有Cl-,与硝酸银反应生成AgCl白色沉淀;氯水呈酸性,含有H+,能与NaHCO3反应生成CO2;氯水中有HClO存在,因此具有漂白性。
A. 氯水中因含有Cl2而呈浅黄绿色,A项正确,不符合题意;
B. 氯水中存在Cl-,与硝酸银反应生成AgCl白色沉淀,B项正确,不符合题意;
C. 氯水呈酸性,含有H+,能与NaHCO3反应生成CO2,C项正确,不符合题意;
D. 向氯水中滴加紫色石蕊,溶液颜色变成红色,说明溶液呈酸性,含有H+,又因氯水中有HClO存在,HClO具有漂白性,最终溶液变为无色,D项错误,符合题意;
答案选D。


科目:高中化学 来源: 题型:
【题目】已知部分弱酸的电离平衡常数如表:
弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是( )
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-═CO![]() +2HClO
+2HClO
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO
C.少量SO2通入Na2CO3溶液中:SO2+H2O+2CO![]() ═SO
═SO![]() +2HCO
+2HCO![]()
D.相同浓度NaHCO3溶液与醋酸溶液等体积混合:H++HCO![]() ═CO2↑+H2O
═CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应,实际通 常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在 实验室制备溴乙烷的装置如图,实验操作步骤如下:
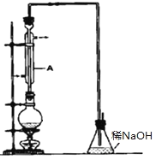
①检查装置的气密性;②在圆底烧瓶中加入 95%乙醇、80% 硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;③小心加热, 使其充分反应。请回答下列问题。
(1)装置 A 的作用是_____。
(2)反应时若温度过高,则有 SO2 生成,同时观察到还有一种红棕色气体产生,该气体的分子式是_____。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中 的_________(填写上正确选项的字母)。
a 亚硫酸钠溶液 b 乙醇 c 四氯化碳
该实验操作中所需的主要玻璃仪器是______。(填仪器名称)。
(4)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水 CaCl2,然后进行的实验操作是__________。(填写正确选项的字母)。
a 分液 b 蒸馏 c 萃取
(5)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因 是_________。通常采用的方法是取少量溴乙烷,然后_____(按 实验的操作顺序选填下列序号)。
①加热 ②加入 AgNO3 溶液 ③加入稀 HNO3 酸化 ④加入 NaOH 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学科学研究中,物质发生化学反应的反应热可通过实验测定,也可通过化学计算的方式间接地获得。
(1)实验方法测反应反应热
①中和热测定
实验中所需要使用的玻璃仪器除烧杯、量筒外还需要___、___。
为了减少实验误差:实验过程中将NaOH溶液___(选填“一次”或“分多次”)倒入盛有盐酸的小烧杯中;溶液混合后,准确读取混合溶液的___,记为终止温度。
②实验测定在一定温度下,0.2molCH4(g)与足量H2O(g)完全反应生成CO2(g)和H2(g)吸收33kJ的热量。该反应的热化学方程式___。
(2)通过化学计算间接获得
①已知拆开1mol的H—H键、I—I、H—I键分别需要吸收的能量为436kJ、153kJ、299kJ。则反应H2(g)+I2(g)=2HI(g)的反应热△H=___kJ·mol-1
②工业生产甲醇的常用方法是:CO(g)+2H2(g)=CH3OH(g) △H=-90.8kJ·mol-1。
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ·mol-1
H2(g)+![]() O2(g)=H2O(g) △H=-241.8 kJ·mol-1
O2(g)=H2O(g) △H=-241.8 kJ·mol-1
根据上述反应确定:H2燃烧热为___kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的一些物质或概念之间的从属关系不正确的是( )
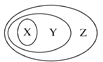
X | Y | Z | |
例 | 氧化物 | 化合物 | 纯净物 |
A | 含氧酸 | 酸 | 化合物 |
B | 溶液 | 分散系 | 混合物 |
C | 强电解质 | 电解质 | 化合物 |
D | 置换反应 | 氧化还原反应 | 离子反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。反应过程和能量关系可用如图简单表示(图中的ΔH表示生成1mol含硫产物的数据)。由图得出的结论正确的是( )
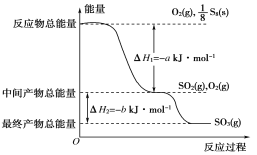
A.S8(s)的燃烧热ΔH=-8(a+b)kJ·mol-1
B.2SO3(g)![]() 2SO2(g)+O2(g) ΔH=-2bkJ·mol-1
2SO2(g)+O2(g) ΔH=-2bkJ·mol-1
C.S8(s)+8O2(g)=8SO2(g) ΔH=-akJ·mol-1
D.由1molS8(s)生成SO3的反应热ΔH=-8(a+b)kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式:__。
(2)下列三种情况下,离子方程式与(1)相同的是__(填字母)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至![]() 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图中的__曲线表示(填字母)。
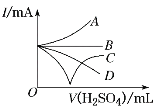
(4)化合物高铁酸钾K2FeO4可作为一种“绿色高效多功能”的水处理剂,可由FeCl3和KClO在强碱条件下反应制得,该反应的离子方程式为__(反应物写Fe3+)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
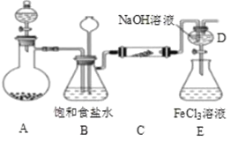
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为__;装置B中饱和食盐水的作用是___;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象__。
(2)甲同学为验证氯气是否具有漂白性,在装置C中放入干燥的有色布条,实验中观察到有色布条褪色,能否说明氯气具有漂白性___,说明理由__。
(3)利用D、E装置可制取高效的水处理剂高铁酸钠(Na2FeO4),请写出E中的化学反方程式___。
(4)上述制备氯气并进行相关实验的装置存在明显的缺陷,请指出___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1—溴丁烷的反应如下:
NaBr+H2SO4HBr+NaHSO4 ①
R—OH+HBr![]() R—Br+H2O ②
R—Br+H2O ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br—被浓硫酸氧化为Br2等。有关数据列表如下;
乙醇 | 溴乙烷 | 正丁醇 | 1—溴丁烷 | |
密度/g·cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
请回答下列问题:
(1)溴乙烷和1—溴丁烷的制备实验中,下列仪器最不可能用到的是________。(填字母)
a.圆底烧瓶 b.量筒 c.锥形瓶 d.长颈漏斗
(2)溴代烃的水溶性______(填“大于”、“等于”或“小于”)相应的醇,将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在______(填“上层”、“下层”或“不分层”)
(3)制备操作中,加入的浓硫酸必需进行稀释,其目的是____________。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是____________。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(5)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于______________ ;
但在制备1—溴丁烷时却不能边反应边蒸出产物,其原因是_______________________。
(6)得到的溴乙烷中含有少量乙醇,为了制得纯净的溴乙烷,可用蒸馏水洗涤,分液后,再加入无水CaCl2后进行的实验操作是______(填字母)
a.分液 b.蒸馏 c.萃取 d.过滤
(7)为了检验溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后______(按实验的操作顺序选填下列序号)①加热 ②加入AgNO3 ③加入稀HNO3 ④加入NaOH溶液.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com