
【题目】一同学欲从量筒中取出部分液体,他先俯视凹液面的最低处,读数为50mL,倒出液体后,他又仰视凹液面的最低处,读数为10mL他实际倒出液体的体积为( )
A.40mL
B.大于40mL
C.小于40mL
D.不一定
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 工业上用Cl2和石灰水为原料生产漂白粉
B. “霾尘积聚难见路人”,雾霾所形成的气溶胶具有丁达尔效应
C. 氢氧化铁胶体用于饮用水的净化、消毒
D. 将饱和FeCl3溶液滴入NaOH溶液中制备Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有250C 101KPa条件下的氯化氢(HCl)气体49L(注:250C 101KPa条件下气体摩尔体积为24.5L/mol)则:
①该气体所含原子总数为____________。
②该气体的质量为____________g。
③该气体溶于127mL水中,得到密度为1.20g/mL的盐酸,此盐酸的物质的量浓度为______________。
④取出20.0 mL该溶液,配成浓度为2.00 mol/L的稀溶液,则稀释后溶液的体积是________ ml
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上湿法制高铁酸钾的基本流程如下:
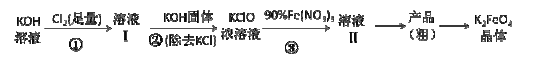
已知:高铁酸盐热稳定性差
回答下列问题:
(1)第③步发生反应的离子方程式 。
(2)第③步反应的体系,温度不宜过高,并最好控制温度在 30℃以下,其原因是 。
(3)通过结晶方法从溶液II得到的粗产品中主要含有杂质 (填化学式),可通过重结晶法提纯K2FeO4,具体操作步骤有:将粗产品先用饱和KOH溶液溶解,然后浓缩、冷却结晶、过滤、洗涤、干燥。其干燥可采用的方法是 (写出一种干燥方法)。
(4)利用电化学原理,用铁钉和氢氧化钾溶液为原料可以获得K2FeO4。在制备过程中铁钉作______极,请写出获得FeO42-的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量混合气体在密闭容器中发生如下反应:mA(g)+nB(g) ![]() pC(g),达到平衡后,温度不变,将气体体积压缩到1/2,当达到平衡时C的浓度为原来的1.9倍,则下列叙述正确的是( )
pC(g),达到平衡后,温度不变,将气体体积压缩到1/2,当达到平衡时C的浓度为原来的1.9倍,则下列叙述正确的是( )
A. m+n>p B. A的转化率增加
C. 平衡向逆反应方向移动 D. C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用钠镁铝分别与盐酸反应填写下面几种情况的空白:
(1)称取相同质量的钠镁铝,然后分别与足量盐酸反应,则产生的氢气在通常条件下的体积之比为_____________。
(2)取相同物质的量的钠镁铝,分别与足量盐酸反应,则产生氢气质量之比为_________。
(3)如果要制取相同体积的氢气(同温同压下),与足量的盐酸分别反应时所消耗的钠镁铝的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某学生设计如下实验方案:已知②加入的试剂为KOH

(1)操作①为_______________;A中的沉淀为_____
(2)操作③所加的试剂为______________,发生的离子反应为 ,
(3)操作④所加的试剂为 ,发生的离子反应为_______________
(4)该同学的实验设计方案是否严密? (填“是”或“否”)如何改进
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种正盐的混合溶液中含有0.2mol Na+、0.25mol Mg2+、0.4mol Cl﹣ , 则SO42﹣的物质的量为( )
A.0.5 mol
B.0.3 mol
C.0.15 mol
D.0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中,能表示反应X(g)+2Y(g)![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比是1∶2∶2
②X、Y、Z的浓度不再发生变化
③恒容时容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④ C.②③ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com