
【题目】镁-过氧化氢燃料电池具有比能量高。安全方便等优点。其结构示意图如图所示、关于该电池的叙述正确的是
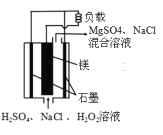
A. 该电池能在高温下正常工作
B. 电流工作时, H+向 Mg 电极移动
C. 电池工作时,正极周围溶液的pH将不断变小
D. 该电池的总反应式为: 该电池的总反应式为Mg+H2O2+H2SO4=MgSO4+2H2O
科目:高中化学 来源: 题型:
【题目】完成下列反应化学方程式:
(1)用氯乙烯制聚氯乙烯;
(2)湿法炼铜;
(3)用CO还原赤铁矿(Fe2O3)冶炼铁;
(4)用铝矾土(Al2O3)冶炼铝;
(5)丁烷裂解获得乙烯 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎,下图是氢氧燃料电池驱动LED发光的装置.下列有关叙述正确的是( ) 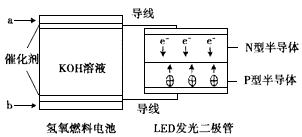
A.电池负极电极反应式为H2﹣2e﹣+2OH﹣=2H2O
B.a处通入氧气,b处通入氢气
C.该装置中能量转化只涉及两种形式的能量
D.P一型半导体连接的是电池负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(1)相同条件下,0.1molL﹣1的NH4Al(SO4)2中c(NH4+)(填“等于”、“大于”或“小于”)0.1molL﹣1NH4HSO4中c(NH4+).
(2)均为0.1molL﹣1的几种电解质溶液的pH随温度变化的曲线如图1所示. 
①其中符合0.1molL﹣1NH4Al(SO4)2的pH随温度变化的曲线是 , 导致pH随温度变化的原因是;
②20℃时,0.1molL﹣1的NH4Al(SO4)2中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)=(取近似值)
(3)室温时,向100mL0.1molL﹣1NH4HSO4溶液中滴加0.1molL﹣1NaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图2所示: 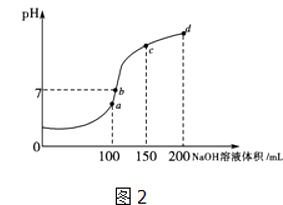
试分析图中a、b、c、d四个点,水的电离程度最大的是点;在b点,溶液中各离子浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d为淡黄色的离子化合物,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法正确的是
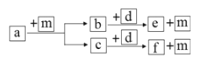
A. 原子半径: W<X<Y<Z
B. 阴离子的还原性: Y>W
C. 图中物质的转化过程均为氧化还原反应
D. a 一定由 W、X 两种元素组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电池在通讯、交通及日常生活中有着广泛的应用.
(1)下列相关说法正确的是(填序号).
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提到议事日程,其首要原因是电池外壳的金属材料需要回收
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为: 2Ni(OH)2+Cd(OH)2 ![]() Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O
已知Ni(OH)2 和Cd(OH)2 均难溶于水,但能溶于酸,以下说法正确的是 .
A.电池放电时Cd作负极
B.反应环境为碱性
C.以上反应是可逆反应
D.该电池是一种二次电池
(3)在宇宙飞船和其他航天器上经常使用的氢氧燃料电池是一种新型电源,其构造如图所示:a、b两个电极均由多孔的碳块组成,通入的氢气和氧气由孔隙中逸入,并在电极表面发生反应而放电. ①a电极是电源的极;
②若该电池为飞行员提供了360kg的水,则电路中通过了mol电子.
③已知H2的燃烧热为285.8kJmol﹣1 , 则该燃料电池工作产生36gH2O时,实际上产生了468.8kJ的电能,则该燃料电池的能量转化率是 . (准确到0.01)(能量转化率是实际上释放的电能和理论上反应放出的热能的比率)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是__________。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的 pH 均增大
②在相同时间内, 两烧杯中产生气泡的速度: 甲__________乙(填“>”、 “<”或“=”)。
③请写出图中构成原电池的负极电极反应式: ____________。
④当甲中溶液质量增重 31.5 克时,电极上转移电子数目为______。
(2)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是 KOH。通甲烷一极的电极反应方程式为 ______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mL 0.1molL﹣1的H2SO4溶液加入纯水中制成200mL溶液,该溶液中由水自身电离产生的c(H+)最接近于( )
A.1×10﹣3 molL﹣1
B.1×10﹣13 molL﹣1
C.1×10﹣7 molL﹣1
D.1×10﹣11 molL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com