

分析 Ⅱ.(1)铜和氧化亚铜都能和硝酸生成Cu2+;氧化亚铜与稀硫酸反应生成Cu和Cu2+,金属铜和稀硫酸不反应;
(2)根据铜元素守恒计算得出正确结论;
Ⅲ.(3)Zn和稀硫酸反应生成氢气;
(4)根据大气压强原理来检验装置的气密性;
(5)根据水的存在会对实验结果造成影响来回答判断.
解答 解:Ⅱ.(1)铜和氧化亚铜都能和硝酸反应生成Cu2+,故方案1不合理;氧化亚铜与稀硫酸反应生成Cu和Cu2+,金属铜和稀硫酸不反应,故方案2合理,
故答案为:不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液;合理,因为氧化亚铜与稀硫酸生成Cu和Cu2+,导致溶液呈蓝色;
(2)根据铜元素守恒,
则2Cu~Cu2O
128 144
b-a c-a,$\frac{128}{144}=\frac{b-a}{c-a}$,解得c=$\frac{9b-a}{8}$,故若红色粉末中含有Cu2O,则a、b与c的应符合的数学关系式为c<$\frac{9b-a}{8}$,
在空气中高温灼烧至质量恒定,这一步骤至少需称量2次,加上前面的2次称量,故该实验方案最少得进行4次称量,
故答案为:c<$\frac{9b-a}{8}$,4;
Ⅲ.(3)Zn和稀硫酸反应生成氢气,离子方程式为Zn+2H+=Zn2++H2↑;
故答案为:Zn+2H+=Zn2++H2↑;
(4)检验装置气密性的方法:关闭活塞,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置漏气,
故答案为:关闭活塞,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置漏气;
(5)根据硫酸铜是否变蓝判断是否含有氧化亚铜时,要注意水的干扰因素,所以制取的氢气要干燥,可以在氢气发生器与硬质玻璃管之间加一个干燥装置,并且要将空气中的水的干扰排除,可以在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管,实验前要将装置中的空气排净,防止干扰,
故答案为:ABC.
点评 本题是一道探究物质组成和实验方案设计的综合性试题,要求学生具有分析和解决问题的能力,难度较大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
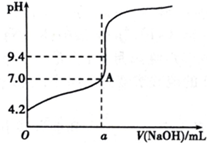 现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:| 滴定次数 | 1 | 2 | 3 | 4 |
| V(标准溶液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应都是吸热反应 | |
| B. | 化学反应都是放热反应 | |
| C. | 物质发生化学反应都伴随着能量变化 | |
| D. | 有能量变化的物质变化都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -870.3KJ•mol-1 | B. | -571.6KJ•mol-1 | C. | +787.0KJ•mol-1 | D. | -488.3KJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④ | C. | ①③④⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O | |
| B. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3 | |
| C. | Cl2+H2O?HCl+HClO | |
| D. | 2NO2?N2O4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com