
某温度下,在2 L密闭容器中,3种气态物质X、Y、Z的物质的量随时间变化曲线如下图
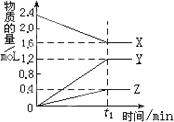
(1)①该反应的化学方程式是________.
②在t1min时,该反应达到了________状态,下列可作为判断反应已达到该状态的是________.
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为2∶3
C.容器内气体压强保持不变
D.生成1 mol Z的同时生成2 mol X
(2)①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1 mol氨气分解成氮气和氢气要吸收46 kJ的热量,则该反应的热化学反应方程式为:________.
②两位同学讨论放热反应和吸热反应.甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应.你认为他们说法正确的是________同学.
科目:高中化学 来源:福建省厦门六中2010-2011学年高一下学期期中考试化学试题 题型:022
已知2NH3(g)![]() N2(g)+3H2(g);在某温度下,在2 L密闭容器中加入一定量的NH3,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
N2(g)+3H2(g);在某温度下,在2 L密闭容器中加入一定量的NH3,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
![]()
该时间内平均反应速率v(N2)=________
达到平衡状态后,下列说法正确的是:________
a.通过改变反应条件可使现有平衡移动
b.NH3的分解速率和合成速率相等
c.NH3不再分解了
d.通过改变反应条件可使NH3全部分解成N2和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
(4分)已知2NH3(g) N2(g) +3 H2(g) ;在某温度下,在2 L密闭容器中加入一定量的NH3 ,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
| 物质 | NH3 | N2 | H2 |
| 物质的量(mol) | 0. 1 | 0.2 | 0.6 |
该时间内平均反应速率v(N2) =
达到平衡状态后,下列说法正确的是:
a.通过改变反应条件可使现有平衡移动
b.NH3的分解速率和合成速率相等
c.NH3不再分解了
d.通过改变反应条件可使NH3全部分解成N2和 H2
查看答案和解析>>
科目:高中化学 来源:2010-2011学年福建省厦门六中高一下学期期中考试化学试卷 题型:填空题
(4分)已知2NH3(g)  N2(g) +3 H2(g) ;在某温度下,在2 L密闭容器中加入一定量的NH3,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
N2(g) +3 H2(g) ;在某温度下,在2 L密闭容器中加入一定量的NH3,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
| 物质 | NH3 | N2 | H2 |
| 物质的量(mol) | 0. 1 | 0.2 | 0.6 |
 条件可使现有平衡移动
条件可使现有平衡移动查看答案和解析>>
科目:高中化学 来源:2013-2014学年河北省石家庄市毕业班教学质量检测(二)理综化学试卷(解析版) 题型:填空题
合成氯是人类研究的重要课题,目前工业合成氨的原理为:
N2(g)+3H2(g)  2NH3(g) ΔH=-93.0kJ/mol
2NH3(g) ΔH=-93.0kJ/mol
(1)某温度下,在2 L密闭容器中发生上述反应,测得数据如下
??????????? 时间/h 物质的量/mol | 0 | 1 | 2 | 3 | 4 |
N2 | 2.0 | 1.83 | 1.7 | 1.6 | 1.6 |
H2 | 6.0 | 5.49 | 5.1 | 4.8 | 4.8 |
NH3 | 0 | 0.34 | 0.6 | 0.8 | 0.8 |
①0~2 h内,v(N2)=??????????? 。
②平衡时,H2的转化率为____;该温度下,反应2NH3(g)  N2(g)+3H2(g)的平衡常数K=?? 。
N2(g)+3H2(g)的平衡常数K=?? 。
③若保持温度和体积不变,起始投入的N2、H2、NH3的物质的量分别为a mol、b mol、c mol,达到平衡后,NH3比的浓度与上表中相同的为?????? (填选项字母)。
A.a=l、b=3.c=0? ?????? B.a=4、b=12、c=0
C.a=0、b=0.c=4? ???? D.a=l、b=3、c=2
(2)另据报道,常温、常压下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成NH3和O2。已知:H2的燃烧热ΔH=-286kJ/mol,则陪制NH3反应的热化学方程式为 ??????? 。
(3)采用高质子导电性的SCY陶瓷(能传递H'),通过电解法也可合成氨,原理为:
N2(g)+3H2(g)  2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入?? ___极,该电极反应式为?????????????????????? 。
2NH3(g)。在电解法合成氨的过程申,应将N2不断地通入?? ___极,该电极反应式为?????????????????????? 。
查看答案和解析>>
科目:高中化学 来源:2013届福建省高一下学期期中考试化学试卷 题型:填空题
(4分)已知2NH3(g)  N2(g) +3 H2(g) ;在某温度下,在2 L密闭容器中加入一定量的NH3 ,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
N2(g) +3 H2(g) ;在某温度下,在2 L密闭容器中加入一定量的NH3 ,反应到10分钟时各组分的浓度不再改变,此时测得各组分的浓度如下:
|
物质 |
NH3 |
N2 |
H2 |
|
物质的量(mol) |
0. 1 |
0.2 |
0.6 |
该时间内平均反应速率v(N2) =
达到平衡状态后,下列说法正确的是:
a.通过改变反应条件可使现有平衡移动
b.NH3的分解速率和合成速率相等
c.NH3不再分解了
d.通过改变反应条件可使NH3全部分解成N2和 H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com