
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是
A.2 g氦气(He)含有的氦原子数为NA
B.0.1 mol/L硫酸钠溶液中,含有0.2NA个Na+
C.100g质量分数为46%的乙醇(C2H5OH)水溶液,含有4NA个氧原子
D.16.25g FeCl3溶于水形成的Fe(OH)3胶体粒子数为0.1NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室回收废水中的苯酚的过程如图所示。下列说法正确的是
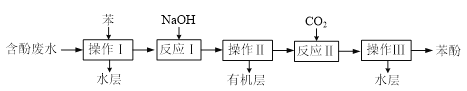
A.操作I为蒸馏B.反应Ⅰ也可加入Na2CO3
C.操作Ⅱ所得有机层可循环利用D.操作Ⅲ所得水层为Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素是最好的抵抗疟疾的药物,可从黄花蒿茎叶中提取,它是无色针状晶体,可溶于乙醇、乙醚等有机溶剂,难溶于水。常见的提取方法如下

(1)操作I、II中,不会用到的装置是________(填序号)。

(2)向干燥、破碎后的黄花蒿中加入乙醚的作用是________。
(3)操作III的目的是_________。
(4)如图是几种实验中常用的仪器:

写出序号所代表的仪器的名称:
A.__________;B.__________;C.__________;D.__________;E.__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:

(1)①如图所示的仪器中配制溶液肯定不需要的是____________________(填字母),
②配制上述溶液还需用到的玻璃仪器是__________________(填仪器名称)。
③下列有关容量瓶使用说法不正确的是( )
a.容量瓶使用前一定要检查是否漏液。其操作为装水盖上瓶塞→倒立观察是否漏夜→正立→玻璃塞旋转180°→再倒立观察是否漏夜。
b.不能作为反应容器或长期贮存溶液的容器;但是可以配制任意体积的溶液。
c.不能将固体或浓溶液直接在容量瓶中溶解或稀释;不能加入过冷或过热的液体 。
d.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小。
(2)在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为________g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___________(填“>”、“<”或“=”)0.1 mol·L-1;
③若NaOH固体溶解后立即移入容量瓶→洗涤烧杯和玻璃棒→洗涤液移入容量瓶→定容,则所得溶液浓度___________(填“>”、“<”或“=”) 0.1 mol·L-1。
(3)在配制硫酸溶液时:
①所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为__________(计算结果保留一位小数)mL;
②如果实验室有15 mL、50 mL、100 mL量筒,应选用___________mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验过程的评价,正确的是( )
A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B.某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO![]()
C.某无色溶液滴入紫色石蕊试液显红色,该溶液一定显碱性
D.验证某溶液中是否含有Cl-,先加稀硝酸酸化,再加入AgNO3溶液,有白色沉淀,证明含Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D 4种可溶性盐,它们的阳离子可能分别是Ca2+、Ag+、Na+、Cu2+中的某一种,阴离子可能分别是NO3-、SO42-、Cl-、CO32-中的某一种。
①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为_________、___________
(2)写出A与D反应的化学方程式:______________________________________;
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是_________和________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)等质量的氧气和臭氧其物质的量之比为___,原子个数之比为__。
(2)标准状况下,36.5gHCl气体的体积约为___。将该气体溶于水中得到2L溶液,则该溶液的浓度为____。
(3)质量分数为w的MgCl2溶液,密度为dg/mL,该溶液中氯离子的物质的量浓度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24LHF含分子数目为0.1NA
B. 120 g NaHSO4固体含有H+的数目为NA
C. 100mL0.1mol/L的Na2CO3溶液中,含阴离子的数目大于0.01NA
D. 1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、量筒、0.5 mol![]() 盐酸、0.55 mol
盐酸、0.55 mol![]() NaOH溶液,实验尚缺少的玻璃用品是________________。
NaOH溶液,实验尚缺少的玻璃用品是________________。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?_____________(填“能”或“否”)
(3)他们记录的实验数据如下:

已知:Q=cm(t2﹣t1),反应后溶液的比热容c为4.18 J℃﹣1g﹣1,
各物质的密度均为1 gcm﹣3。
①计算完成上表ΔH=_____________________________(保留2位小数)。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:__。
(4)若用醋酸代替HCl做实验,对测定结果___填“有”或“无”)影响。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com