
【题目】现有25 ℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中![]() _______(填“增大”“减小”或“不变”)。
_______(填“增大”“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式_____________;若所得溶液的pH=5,则溶液中由水所电离出的氢离子浓度为___________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol/L,则c(SO42-)=______。
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的关系是_____________________________________________。
【答案】 减小 NH3·H2O+H+=NH4++H2O 10-5mol/L a/2 mol·L-1 c(NH4+)>c(SO42-)>c(H+)>c(OH-)
【解析】现有25 ℃时0.1 mol/L的氨水,溶液中存在电离平衡NH3H2O![]() NH4++OH- 。
NH4++OH- 。
(1)若向氨水中加入少量硫酸铵固体,可以增大氨水中铵根的浓度,所以氨水的电离平衡逆向移动,此时溶液中![]() 减小;
减小;
(2)向氨水中加入稀硫酸使其恰好中和得到硫酸铵溶液,反应的离子方程式NH3·H2O+H+===NH![]() +H2O;硫酸铵水解使溶液呈酸性,溶液中的H+全部来自于水,所以若所得溶液的pH=5,则溶液中由水所电离出的氢离子浓度为10-5mol/L。
+H2O;硫酸铵水解使溶液呈酸性,溶液中的H+全部来自于水,所以若所得溶液的pH=5,则溶液中由水所电离出的氢离子浓度为10-5mol/L。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH![]() )=a mol/L,由电荷守恒得则c(SO
)=a mol/L,由电荷守恒得则c(SO![]() )=
)=![]() c(NH
c(NH![]() )=
)=![]() mol/L;
mol/L;
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则两溶液改好完全反应得到硫酸铵溶液,铵根水解使溶液呈酸性,所以,所得溶液中各离子物质的量浓度由大到小的关系是c(NH4+)>c(SO42-)>c(H+)>c(OH-)。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
①NaHCO3溶液加水稀释时,![]() 将增大;
将增大;
②浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO![]() )+c(HCO)];
)+c(HCO)];
③在0.1 mol·L-1氨水中滴加0.1 mol·L-1盐酸,恰好完全中和时pH=a,则由水电离产生的c(OH-)=10-amol·L-1;
④已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2Cr2O4)=2.0×10-12,则Ag2Cr2O4的溶解度小于AgCl
A. ①② B. ②④ C. ① D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、用0.1 molL-1 NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 molL-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

①滴定盐酸的曲线是______________(填“I”或“Ⅱ”);
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是_____________________;
③V1和V2的关系:V1 _____ V2(填“>”、“=”或“<”)。
Ⅱ、已知25℃时,2.0×103 mol/L氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F)与溶液pH的变化关系如图所示。

(1)25℃时,HF的电离平衡常数Ka=_____________。
(2)已知HF(aq)![]() H+(aq)+F(aq) ΔH=10.4 kJ/mol,现将室温下0.1 mol/L HF溶液升温至30℃(不考虑溶质和溶剂的挥发),下列各量增大的是__________。
H+(aq)+F(aq) ΔH=10.4 kJ/mol,现将室温下0.1 mol/L HF溶液升温至30℃(不考虑溶质和溶剂的挥发),下列各量增大的是__________。
a.Ka b.Kw c.n(H+) d. 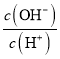
(3)25℃时,在20 mL 0.1 mol/L氢氟酸中加入V mL 0.1 mol/L NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是__________________。

a.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
b.①点时pH=6,此时溶液中,c(F)c(Na+)=9.9×107 mol/L
c.②点时,溶液中的c(F)=c(Na+)
d.③点时V=20 mL,此时溶液中c(F)<c(Na+)=0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种主族元素的原子序数依次增大,且均小于18.A原子的最外层电子比B原子的最外层电子少2个,B原子的质子数是其电子层数的4倍.A、B、C三种元素能结合成化合物C2AB3 , 在1mol C2AB3中共有52mol电子.D元素的单质0.5mol与酸全部反应生时,有9.03×1023个电子转移.E元素的单质是一种黄绿色气体,水溶液具有漂白性.试填写下列空白:
(1)写出元素A和E的名称:A , E .
(2)元素B在周期表中的位置为第二周期族.
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有键(填“极性”或“非极性”)的化合物(填“离子”或“共价”),写出该化合物的电子式 .
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学将金属钠露置于空气中,观察到下列现象:银白色→变灰暗→变白色→出现液滴→白色固体。其变质过程中不可能产生的物质是
A. Na2O B. NaOH
C. Na2CO3 D. NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于营养物质的说法正确的是( )
A. 油脂的氢化属于还原反应,又属于加成反应,生成物为纯净物
B. 1 mol蔗糖的水解产物是1 mol葡萄糖和1 mol果糖
C. 淀粉溶液和稀硫酸共热后发生水解反应,冷却后加少量银氨溶液,水浴加热后出现光亮的银镜
D. 鸡蛋白溶液中滴加饱和的硫酸铵溶液,出现白色沉淀,该过程叫做蛋白质的变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂对工业污泥中的Cr元素回收与再利用的工艺如下(己知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3* | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时 的pH | 1.9 | 7.0 | — | 一 | — |
沉淀完全时 的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(1)实验室用98% (密度为1.84 g·cm-3)的浓硫酸配制200mL4.8 mol·L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为_________mL (保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒外,还需__________________________________。
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏小的操作是____________________(填序号)
a.定容时俯视刻度线 b.量取浓硫酸时,俯视刻度线
c.当容置瓶中液体占容积2/3左右时,未振荡摇匀 d.转移溶液时,没有等溶液冷却至室温
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是_____________________________。(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是___________________。
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是_____________________。
(6)通SO2气体时,还原过程发生以下反应(填写缺项物质并配平)
____________________________________________________________Na2SO4.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 酿酒过程中,葡萄糖可通过水解反应生成酒精
B. 鸡蛋清溶液中加入饱和硫酸钠溶液,生成的沉淀物不能再溶解
C. 酸性高锰酸钾紫色溶液中加入植物油充分振荡后,溶液颜色会褪去
D. 脂肪能发生皂化反应,生成甘油和高级脂肪酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com