
【题目】向Fe和Fe2O3组成的6.56 g混合物中加入100 mL某浓度的盐酸,恰好完全反应,生成896mLH2(标准状况下),若向反应后的溶液中滴入几滴KSCN溶液,溶液不呈红色。求:
(1)原混合物中Fe2O3的质量分别为______,Fe的质量为________。
(2)原盐酸的物质的量浓度____________。
【答案】3.20 g 3.36g 2.0 mol /L
【解析】
(1)设原混合物中Fe、Fe2O3的物质的量分别为x、y ,混合物中加入盐酸,反应的有关方程式是Fe2O3 + 6H+=2Fe3+ + 3H2O 2Fe3+ + Fe = 3Fe2+ Fe + 2H+= Fe2+ + H2↑,反应放出氢气的物质的量为:![]() ,
,
根据方程式中物质间的关系可得方程x-y= 0.04mol,根据原固体质量可得56x+160y =6.56g
解得x=0.06mol,y=0.02mol,所以原混合物中Fe的质量为m(Fe)=0.06mol×56g/mol=3.36g,含有的Fe2O3质量为m(Fe2O3)=0.02mol×160g/mol=3.20g;
(2)由于反应后溶液中只有FeCl2,故根据元素守恒,可知参与反应的HCl物质的量为:n(HCl)=2n(FeCl2)=2n(Fe)+4n (Fe2O3)=2×0.06mol+4×0.02mol=0.20mol,则c(HCl)=![]() 。
。


科目:高中化学 来源: 题型:
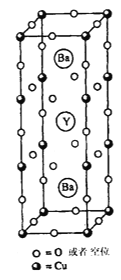
【题目】1911年,科学家发现汞在4.2K以下时电阻突然趋近于零——即低温超导性。1986年,科学家又发现了Nb3Ge在23K下具有超导性。1987年2月,赵忠贤及合作者独立发现了在液氮温区(沸点77 K)的高温超导体,其晶胞如图所示,元素组成为Ba-Y-Cu-O(临界温度93 K),推动了国际高温超导研究。赵忠贤院士获得2016年度国家最高科学技术奖。
回答下列问题:
(1)铌Nb位于第五周期,Nb的外围电子排布式为4d45s1,Nb位于_______族
(2)下列关于Ge元素叙述正确的是______(从下列选项中选择)
A.Ge晶体属于准金属,且为共价晶体 B.Ge属于p区的过渡金属
C.Ge的第一电离能比As、Se均要小 D.Ge的电负性比C大
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是______________
(4)NH3也常作致冷剂,其键角_______(填“大于”或“小于”)109°28′,NH3的沸点(239.6 K)高于N2沸点的主要原因是___________________________
(5)图示材料的理想化学式(无空位时)为___________________,若Y(钇)元素的化合价为+3,则Cu的平均化合价为_______
(6)金属铜属于面心立方最密堆积,其晶胞中Cu原子的最近距离为a cm,金属铜的晶体密度为ρ g/cm3,阿伏伽德罗常数为NA,则铜的相对原子质量为________ (只含一个系数,用a、ρ、NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年11月30日第21届联合国气候大会在巴黎召开,会议的一项主题是温室气体减排。如图是科学家正在研发的实现CO2和H2合成甲醇的燃烧电池。下列叙述正确的是
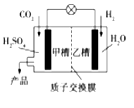
A.乙槽中反应生成水
B.甲槽中的电极反应式为:CO2+6e-+5H2O=CH3OH+6OH-
C.质子从乙槽通过质子交换膜进入甲槽
D.放电过程中,乙槽的电极附近溶液的pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业硫酸盐废水中含有大量的Fe2+、Fe3+、较多的Cu2+和少量的Na+。工厂计划从该废水中回收硫酸亚铁和金属铜,设计如下流程图。

回答下列问题;
(1)A的化学式为_________,D的化学式为_______。
(2)在工业废水中加入过量A时,发应的离子方程式有:___________、__________。
(3)得到FeSO47H2O晶体的操作Ⅲ为:加热浓缩、冷却结晶、______、______、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·mL-1,溶质的质量分数为w,其中含有NH4+的物质的量是b mol,下列叙述正确的是( )
A. 溶质的质量分数w=![]() ×100%
×100%
B. 溶质的物质的量浓度c=![]() mol·L-1
mol·L-1
C. 溶液中c(OH-)=![]() mol·L-1+c(H+)
mol·L-1+c(H+)
D. 向上述溶液中加入V mL水,所得溶液的质量分数大于0.5w
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知100℃时,水的离子积常数Kw=1×10-12,对于该温度下pH=l1的氨水,下列叙述正确的是
A. 向该溶液中加入同温同体积pH=1的盐酸,反应后溶液呈中性
B. 温度降低至25℃,该氨水溶液中H2O电离出的H+浓度小于10-11mol/L
C. 该氨水溶液中加入NH4Cl溶液,NH3·H2O的电离能力增强
D. 滴加等浓度等体积的硫酸,得到的溶液中存在电离平衡:NH4HSO4(aq)![]() NH4+(aq)+H+(aq)+SO42-(aq)
NH4+(aq)+H+(aq)+SO42-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:
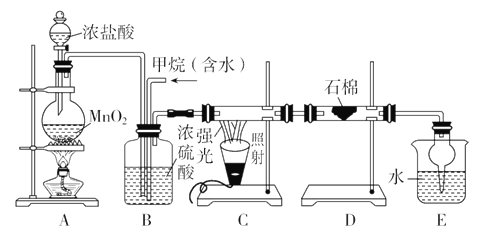
根据设计要求回答:
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③____________。
(2)D装置的石棉中均匀混有KI粉末,其作用是_______________。
(3)E装置的作用是________(填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(4)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出生成黑色小颗粒的化学方程式_________________________________________________________。
(5)E装置除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为________。该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为________(填编号)。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3 e.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1) 同温同压下,同体积的NH3和H2S气体的质量比是________________;同质量的NH3和H2S气体的体积比是_____________,同质量的NH3和H2S气体中所含氢原子个数比是_____________,若两者所含氢原子个数相等,它们的物质的量比是__________;
(2)在100ml Al2(SO4)3溶液中含0.6molSO42-,从中取出1/4 体积的该溶液再稀释到100 ml,则稀释后的溶液中SO42-的物质的量浓度为_______________。。
(3)在氯化镁和硫酸镁的混合液中,若Mg2+与Cl-的物质的量浓度之比为4∶3时,则Mg2+与SO42-物质的量浓度之比为_____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,A和I都是金属单质,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
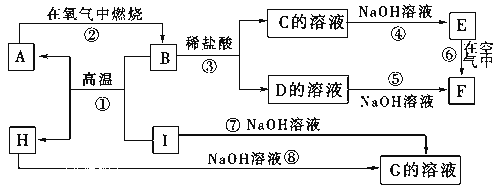
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是________。
(2)反应③的离子方程式为________________________
反应⑧的化学方程式为_____________________________________
(3)反应⑥过程中的现象是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com