
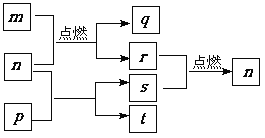
����Ŀ������������Ԫ��X��Y��Z��Wԭ��������������m��W�ĵ��ʣ�r��X�ĵ��ʣ�s��Y�ĵ��ʣ�n��p��q����ЩԪ����ɵĶ�Ԫ�����t�����е�����Ԫ����ɣ���ˮ��Һ�ʼ��ԣ�p�ǵ���ɫ���壬q��һ�����²��ϣ����ǵĹ�ϵ����ͼ��ʾ������˵����ȷ����
A. Y��Z��W�ļ����ӵĵ��Ӳ�ṹ��ͬ
B. ԭ�Ӱ뾶��r��X����r��Y����r��Z����r��W��
C. ���⻯����ȶ��ԣ�X��Y
D. Y��Z����Ԫ���γɵĻ�����һ��ֻ�����Ӽ�
���𰸡�A
���������������������������Ԫ��X��Y��Z��Wԭ��������������p�ǵ���ɫ����pΪNa2O2��t�����е�����Ԫ����ɣ���ˮ��Һ�ʼ��ԣ�tΪNaOH�����ݿ�ͼ��nΪˮ�������̼��sΪ������rΪ������̼��q��һ�����²��ϣ�qΪ������������þ�����mΪþ������������rΪ̼��qΪ����þ�����XΪCԪ�أ�YΪOԪ�أ�ZΪNaԪ�أ�WΪMgԪ�ء�A��O��Na��Mg�ļ����ӵĵ��Ӳ�ṹ��ͬ����Ϊ2��8�Ų�����A��ȷ��B��ԭ�Ӱ뾶��r��C����r��O������B����C��Ԫ�صķǽ�����Խǿ�����⻯����ȶ���Խǿ���ȶ���C��O����C����D�����������д��ڹ��ۼ�����D����ѡA��


 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д� ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ش�
��1��Na2O2�ĵ���ʽ ��
��2����ȥFeCl3������FeCl2�����ӹ����漰�Ļ�ѧ��Ӧ����ʽ ��
��3��������Na2CO3��Һ��ͨ��CO2���壬��Һ�г��ְ�ɫ���ǣ�д���÷�Ӧ�����ӷ���ʽ ��
��4��˫��ˮ��ʹ���Ը��������Һ��ɫ�������������ط�Ӧ�����ӷ���ʽ��
�� ��MnO4������ ��H2O2�� ���� ��Mn2+���� ��H2O�� ��
����������A ��NaH������Ҫ�Ļ�ԭ������ˮ��ǿ�ҷ�Ӧ��һ�������£�2.40g NaH������B��Ӧ����3.90g������A�� 2.24L��������ɱ�״������H2����֪����B��ʹʪ���ɫʯ����ֽ��������֪��NH3+ NH3��NH4++NH2-
��ش��������⣺
��1��A�Ļ�ѧʽ�� ��
��2��A���������ᷢ����������ԭ��Ӧ�Ļ�ѧ����ʽ ��
��3���ڸ������⻯�ƣ�NaH���ɽ����Ȼ��ѣ�TiC14����ԭ�ɽ����ѣ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ��������������� ��

A��ͼ�ױ�ʾij���淴Ӧ���ʵ�Ũ����ʱ��ı仯������tʱ�̴ﵽƽ��״̬
B��ͼ�ұ�ʾ��0.1 mol��L�C1����ˮ��Һ����ˮʱ��Һ�ĵ����Ա仯
C��ͼ����ʾij���ȷ�Ӧ�ֱ����С����������������Ӧ�����е������仯
D��ͼ����ʾ��CH3COOH��Һ������CH3COONa�������ҺpH�ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��80��ʱ��NO2��g����SO2��g��![]() SO3��g����NO��g�������¶��£��ڼס��ҡ������������ܱ������У�Ͷ��NO2��SO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��NO2��ת����Ϊ50%�������жϲ���ȷ������ ��
SO3��g����NO��g�������¶��£��ڼס��ҡ������������ܱ������У�Ͷ��NO2��SO2����ʼŨ�����±���ʾ�����м�2min��ƽ��ʱ��NO2��ת����Ϊ50%�������жϲ���ȷ������ ��
��ʼŨ�� | �� | �� | �� |
c��NO2��/mol ��L��1 | 0.10 | 0.20 | 0.20 |
c��SO2��/mol ��L��1 | 0.10 | 0.10 | 0.20 |
A��ƽ��ʱ������SO2��ת���ʴ���50%
B������Ӧƽ��ʱ������c��SO2���Ǽ��е�2��
C���¶�����90����������Ӧƽ�ⳣ��Ϊ25/16��������ӦΪ���ȷ�Ӧ
D�������������䣬����ʼʱ���������г���0.10mol ��L��1 NO2��0.20 mol ��L��1 SO2���ﵽƽ��ʱc��NO����ԭƽ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ĥ����Ƭ����������NaOH��Һ�У��й����ӷ���ʽ��ȷ����
A. Al2O3 + OH- �� AlO2- + H2O B. 2Al3+ + 6OH- �� 2Al(OH)3��
C. 2Al + 2OH- + 2H2O �� 2AlO2- + 3H2�� D. 2Al + 6H2O �� 2Al3+ + 6OH- +3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������γɵ�һ�������1Co��NH3��5NO2]Cl2���Ʊ�����������
![]()
��1��Co2+��̬��������Ų�ʽΪ ��
��2�������1Co��NH3��5Cl]Cl2����Co3+�γ���λ����ԭ��Ϊ ����Ԫ�ط������������� 1Co��NH3��5NO2]2+�������е�ԭ�ӵ��ӻ��������Ϊ ��
��3����NO2����Ϊ�ȵ�����ĵ��ʷ���Ϊ ��д��ѧʽ����
��4��H2O2��H2O��������������ܣ�����Ϊ���Ƕ��Ǽ��Է����⣬����Ϊ ��
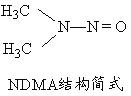
��5������������ˮ���п�ת��Ϊǿ�°�����������������NDMA���ṹ��ʽ��ͼ��ʾ��1molNDMA�����к���![]() ������ĿΪ mol��
������ĿΪ mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������CO��SO2�̵�����Ⱦ��һ�ַ����ǽ����ڴ���������ת��Ϊ����S����֪����CO(g)��![]() O2(g)=CO2(g) ��H����283.0 kJ��mol-1
O2(g)=CO2(g) ��H����283.0 kJ��mol-1
��S(s)��O2(g)=SO2(g) ��H����296.0 kJ��mol-1
�˷�Ӧ���Ȼ�ѧ����ʽ��________________________________��
��2��������������ɹ⻯ѧ�����ͳ�������ĵ���Ҫ���塣��֪��
CO(g)��NO2(g)=NO(g)��CO2(g) ��H����a kJ��mol-1(a>0)
2CO(g)��2NO(g)=N2(g)��2CO2(g) ��H����b kJ��mol-1(b>0)
���ñ�״����3.36 L CO��ԭNO2��N2(CO��ȫ��Ӧ)������������ת�Ƶ��ӵ����ʵ���Ϊ____________mol���ų�������Ϊ____________kJ(�ú���a��b�Ĵ���ʽ��ʾ)��
��3����CH4����ԭNOxҲ�������������������Ⱦ��������
CH4(g)��4NO2(g)=4NO(g)��CO2(g)��2H2O(g)��H1����574 kJ��mol-1��
CH4(g)��4NO(g)=2N2(g)��CO2(g)��2H2O(g) ��H2������
��1 mol CH4��ԭNO2��N2�����������зų�������Ϊ867 kJ������H2��____________��
��4��ij���ʳ�������ˮ�еĵ�Ԫ�ض���NH![]() ��NH3��H2O��ʽ���ڣ��÷�ˮ�Ĵ��������У�NH
��NH3��H2O��ʽ���ڣ��÷�ˮ�Ĵ��������У�NH![]() ���������õ������¾���������Ӧ��������NO
���������õ������¾���������Ӧ��������NO![]() ��������Ӧ�������仯ʾ����ͼ��ʾ��
��������Ӧ�������仯ʾ����ͼ��ʾ��
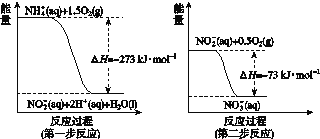
1 mol NH![]() (aq)ȫ��������NO
(aq)ȫ��������NO![]() (aq)���Ȼ�ѧ����ʽ��________________��
(aq)���Ȼ�ѧ����ʽ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں���H+��Cl-��Na+����Һ�У������Դ��������������
A. CO32- B. AlO2- C. Ca2+ D. Ag+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com