
| A. | ①②③ | B. | ①④⑤⑥ | C. | ①③④⑤⑥ | D. | ①②③④⑤⑥ |
分析 种短周期元素X和Y可组成化合物XY3,则X为ⅢA族元素时,Y为ⅤⅡA族元素;或X、Y均为ⅥA族元素;还有可能为X在ⅤA族,Y为ⅤⅡA族或H,还有可能为NaN3等,据此分析解答.
解答 解:两种短周期元素X和Y可组成化合物XY3,则:
X为ⅢA族元素时,Y为ⅤⅡA族元素时,当X的原子序数为m时,Y的原子序数可能为m+4、m+12、m-4;
X、Y均为ⅥA族元素,为三氧化硫,X的原子序数为m时,Y的原子序数为m-8;
X在ⅤA族,Y为ⅤⅡA族,当X的原子序数为m时,Y的原子序数可能为m+2、m+10、m-6;
X在ⅤA族,Y为H,当X的原子序数为m时,Y的原子序数可能为m-6、m-14;
还有可能为NaN3,当X的原子序数为m时,Y的原子序数可能为m-4;
故选D.
点评 本题考查原子结构与元素性质,注意根据XY3判断元素在周期表中的可能位置,难度中等,注意利用列举法解答.


科目:高中化学 来源: 题型:填空题
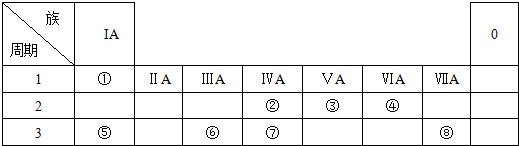
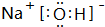
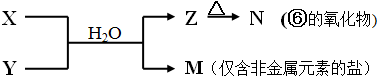
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石的网状结构中,最小的环上有6个碳原子 | |
| B. | 分子晶体熔化时,不破坏共价键;原子晶体熔化时,破坏共价键 | |
| C. | 在金属铜的晶体中,由于存在自由电子,因此铜能导电 | |
| D. | 在氯化铯晶体中,每个氯离子周围最近且等距离的氯离子有8个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用1L水里含有溶质物质的量来表示的浓度叫做物质的量浓度 | |
| B. | 用一定量溶液里含有溶质的多少来表示的浓度叫做物质的量浓度 | |
| C. | 用1L溶液里含有溶质的量来表示的浓度叫做物质的量浓度 | |
| D. | 用1L溶液里含有多少摩尔溶质来表示的浓度叫做物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入一定体积的NaCl溶液 | B. | 加入一定体积的KNO3饱和溶液 | ||
| C. | 加入少量的Na2CO3固体 | D. | 加入少量的CuSO4固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a=b>0时,该反应达到化学平衡状态 | |
| B. | 该反应达到化学平衡状态时,一定有a>b | |
| C. | 当密闭容器内气体密度不再改变时,该反应达到化学平衡状态 | |
| D. | 密闭容器中X和Y的物质的量之比为1:2时,该反应达到化学平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 甲 | 495.8 | 4562 | 6910.3 | 9543 | 13354 |
| 乙 | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
| 丙 | 786.5 | 1577.1 | 3231.6 | 4355.5 | 16091 |
| 丁 | 1251.2 | 2298 | 3822 | 5158.6 | 6542 |
| A. | 甲的金属性比乙强,且甲和乙的最高价氧化物的水化物可以相互反应 | |
| B. | 乙的最外层电子轨道表达式: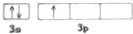 | |
| C. | 丙的最高价氧化物性质稳定,属于原子晶体,常温下不和强酸、强碱、强氧化剂反应 | |
| D. | 丁的常见的气态氢化物一定是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
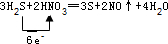 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com