
| 0.01mol?L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol?L-1Na2SO3溶液的体积/mL | H2O的体积/mL | 实验温度 /℃ |
溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
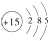 ,故答案为:
,故答案为: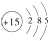 ;
;

科目:高中化学 来源: 题型:
| A、减小压强(通过改变容积体积)时,正反应速率减小,逆反应速变增大,平衡向逆反应方向移动 |
| B、增大压强(通过改变容积体积)时,Z的物质的量浓度增大,X、Y的物质的量浓度减小 |
| C、升高温度时,正、逆反应速率都增大,平衡向正反应方向移动 |
| D、容积体积不变,再通入一定量的X,平衡正向移动,Z的物质的量分数一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胆矾 CuSO4?5H2O 混合物 |
| B、氖气 Ne 单质 |
| C、烧碱 NaOH 氧化物 |
| D、纯碱 NaOH 碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D、E、X为原子序数依次增大的短周期元素,A的基态原子有三个未成对电子,B、E最外层电子数相同,E的核电荷数是B的2倍,C的焰色反应呈黄色,D第三周期中原子半径最小的金属元素,X元素为同周期电负性最大的主族元素.Y为第四周期ⅠB的元素.
A、B、C、D、E、X为原子序数依次增大的短周期元素,A的基态原子有三个未成对电子,B、E最外层电子数相同,E的核电荷数是B的2倍,C的焰色反应呈黄色,D第三周期中原子半径最小的金属元素,X元素为同周期电负性最大的主族元素.Y为第四周期ⅠB的元素.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com