
 ,
, ;
;| 催化剂 |
| 催化剂 |
| △ |
| 浓硫酸 |
| △ |
| 催化剂 |
| 催化剂 |
| △ |
| 浓硫酸 |
| △ |


科目:高中化学 来源: 题型:
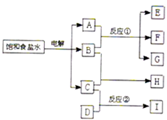 如图所示,每一方框中的字母各代表一种反应物或生成物:
如图所示,每一方框中的字母各代表一种反应物或生成物:| C | D | I | |
| 起始组成/mol | 6 | 4 | 0 |
| 平衡组成/mol | 3 | 3 | 1 |
| A、物质H的化学式是HCl | ||
| B、反应①的化学方程式是Cl2+2NaOH═NaCl+NaClO+H2O | ||
C、反应②的平衡常数等于
| ||
| D、电解饱和食盐水的阴极可以是铁棒,阳极可以是碳棒或铁棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 | 实验现象 | 结论 |
| A | 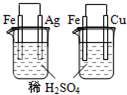 烧杯中银表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Fe>Cu>Ag |
| B |  边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C |  淡黄色固体先变为白色,后变为黑色 | 溶解性:AgCl>AgBr>Ag2S |
| D | 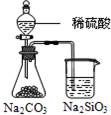 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:S>C>Si |
| A、A | B、B | C、B | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 粒子 | 立体结构 | 中心原子 氧化数 | 中心原子 杂化轨道类型 |
| SO2Cl2 | |||
| ICl4- |
| 2π | 4 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com