
A、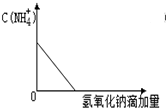 |
B、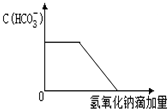 |
C、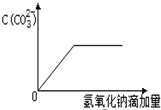 |
D、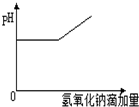 |


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
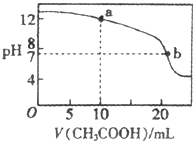 常温下有下列四种溶液:
常温下有下列四种溶液:| ① | ② | ③ | ④ | ||
| 溶液 | pH=4的NH4Cl | pH=4的盐酸 | 0.1mol?L-1的醋酸 | 0.1mol?L-1的NaOH | |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要的时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
| a |
| b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(1)(3) |
| B、(1)(4) |
| C、(2)(3) |
| D、(2)(4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.1g C12与足量NaOH溶液反应转移0.2×6.02×1023个电子 |
| B、1mol乙酸分子与1mol甲酸甲酯分子中都含有7×6.02×1023个共用电子对 |
| C、28g乙烯和丙烯的混合气体中含有2×6.02×1023个碳原子 |
| D、2 mol/L的 MgCl2溶液中含有2×6.02×1023个Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,将铜放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中钝化 |
| B、浓硝酸在光照下变黄,证明硝酸不稳定,且产物有红棕色气体可溶于浓硝酸 |
| C、溴蒸气使湿润的碘化钾淀粉试纸变蓝,说明溴可与淀粉反应 |
| D、液氨是一种重要的制冷剂,说明氨气在液化时吸收大量的热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(1)(2)(3)均能说明该物质是酸 |
| B、(1)(2)(3)均不能说明该物质是酸 |
| C、只有(3)能说明该物质是酸 |
| D、(2)(3)能说明该物质是酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硝酸中加入过量铁粉:Fe+NO3-+4 H+═Fe3++NO↑+2 H2O |
| B、向碘化亚铁溶液中通少量氯气:Cl2+2Fe2+═2Fe3++2Cl- |
| C、工业刻蚀印刷电路板:2 Fe3++Cu═2 Fe2++Cu2+ |
| D、氢氧化铁溶于氢碘酸:Fe(OH)3+3 H+═Fe3++3 H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、按系统命名法命名时,图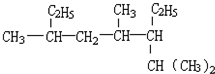 的名称是3,5,7-三甲基-6-乙基辛烷 的名称是3,5,7-三甲基-6-乙基辛烷 |
B、有机物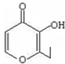 的一种芳香族同分异构体能发生银镜反应 的一种芳香族同分异构体能发生银镜反应 |
| C、等质量的乙酸甲酯和甲酸乙酯完全燃烧生成水的量相等 |
D、高分子化合物 ,其单体为对苯二甲酸和乙醇 ,其单体为对苯二甲酸和乙醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com