
【题目】利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是

A.a极反应:CH4 -8e-+4O2-=CO2+2H2O
B.A、C膜均为阳离子交换膜,B膜为阴离子交换膜,
C.可用铁电极替换阴极的石墨电极
D.a极上通入2.24 L(标准状况下)甲烷,阳极室Ca2+减少0.4 mol
【答案】D
【解析】
根据题干信息,左侧为原电池,右侧为电解池,a极为原电池的负极,电极反应式CH4 -8e-+4O2-=CO2+2H2O,b极为正极,电极反应式O2+4e-=2O2-,阳极室的电极反应:2Cl--2e-=Cl2↑,阳极室的Ca2+通过A膜(阳离子交换膜)进入产品室,阴极室的电极反应:2H2O+2e-=H2↑+2OH-,阴极不参与反应,可以用铁电极替换石墨电极,原料室的Na+通过C膜(阳离子交换膜)进入阴极室,原料室的H2PO4-通过B膜(阴离子交换膜)进入产品室,在产品室中制得产品Ca(H2PO4)2,据此分析解答。
A.根据上述分析可知,a极为原电池的负极,电极反应式CH4 -8e-+4O2-=CO2+2H2O,A选项正确;
B.阳极室的Ca2+通过A膜(阳离子交换膜)进入产品室,原料室的Na+通过C膜(阳离子交换膜)进入阴极室,原料室的H2PO4-通过B膜(阴离子交换膜)进入产品室,在产品室中制得产品Ca(H2PO4)2,B选项正确;
C.阴极室的电极反应:2H2O+2e-=H2↑+2OH-,阴极不参与反应,可以用铁电极替换石墨电极,C选项正确;
D.a极上通入2.24 L(标准状况下)甲烷,转移电子0.8mol,根据e-守恒,阳极室中Cl-失去的电子也为0.8mol,所以消耗的Cl-0.4mol,即负电荷减少0.4mol,所以阳极室中带正电荷的0.2molCa2+移向产品室,D选项错误;
答案选D。


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】设 NA 为阿伏加德罗常数的值。下列说法中正确的是( )
A.标准状况下,11.2L H2 与 11.2L D2 所含的质子数均为NA
B.1L0.1mol·L-1Fe2(SO4)3 溶液中含 Fe3+数目为 0.2 NA
C.3.2g 铜与 3.2g 硫隔绝空气加热使之充分反应,转移电子数为 0.1 NA
D.0.1mol 乙醇与 0.1mol 乙酸在一定条件下反应生成乙酸乙酯分子数为 0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,反应2A![]() B(g) +C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是( )
B(g) +C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是( )
A. 正反应是吸热反应,且A不是气态
B. 正反应是放热反应,且A是气态
C. 其他条件不变,加入少量A,该平衡向正反应方向移动
D. 改变压强对该平衡的移动无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂所选用的试剂及操作方法均正确的一组是(括号内为杂质)( )
选项 | 物质 | 选用的试剂 | 操作方法 |
A | NaCl(泥沙) | 水 | 过滤 |
B | CO2(CO) | O2 | 点燃 |
C | Fe(Zn) | 稀硫酸 | 结晶 |
D | CO2(HCl) | NaOH溶液 | 洗气 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
①NH4Cl固体;②硫酸;③NaOH固体;④水;⑤加热;⑥加入少量MgSO4固体。
A. ①②③⑤ B. ③⑥ C. ③ D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s) ![]() N2(g)+CO2(g) △H = -213.5kJ/mol,达到平衡的数据如下:
N2(g)+CO2(g) △H = -213.5kJ/mol,达到平衡的数据如下:
温度/℃ | n(活性炭)/mol | n(CO2)/mol |
T1 | 0.70 | —— |
T2 | —— | 0.25 |
下列说法不正确的是( )
A. 上述信息可推知:T1<T2
B. T1℃时,该反应的平衡常数K=9/16
C. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
D. T2℃时,若反应达平衡后再缩小容器的体积。c(N2)/c(NO)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为 -5.5℃,易水解。已知:AgNO2 微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2,某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。

(1)制备 Cl2 的发生装置可以选用 _________ (填字母代号)装置,发生反应的离子方程式为________________________________________ 。
(2)欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 a→_______→______→ _____→________→_______→______→______→______。(按气流方向,用小写字母表示,根据需要填,可以不填满,也可补充)。
(3)实验室可用下图示装置制备亚硝酰氯。其反应原理为:Cl2+2NO=2ClNO

①实验室也可用 B 装置制备 NO , X 装置的优点为___________________ 。
②检验装置气密性并装入药品,打开 K2,然后再打开 K3,通入一段时间气体,其目的是 ___________________,然后进行其他操作,当 Z 中有一定量液体生成时,停止实验。
(4)已知:ClNO 与 H2O 反应生成 HNO2 和 HCl。
①设计实验证明 HNO2 是弱酸:_________________________________________。(仅提供的试剂:1 molL-1 盐酸、 1 molL-1HNO2 溶液、 NaNO2 溶液、红色石蕊试纸、蓝色石蕊试纸)。
②通过以下实验测定ClNO 样品的纯度。取 Z 中所得液体m g 溶于水,配制成 250 mL 溶液;取出 25.00 mL 样品溶于锥形瓶中,以 K2CrO4 溶液为指示剂,用 c molL-1 AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 20.00mL。滴定终点的现象是_____亚硝酰氯(ClNO)的质量分数为 _________。(已知: Ag2CrO4 为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表前四周期的一部分,下列有关R、W、X、 Y、Z五种元素的叙述中,正确的是( )
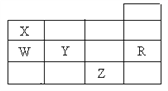
A. 通常情况下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的电负性比X的的电负性大
D. 第一电离能:R>W>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是两种溶液进行电解的装置。电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,B,C,D都是铂电极,P,Q是电池的两极,电路接通后,电极B上金属有M沉淀出来,

请回答下列问题:
(1)其中P是______极,B是______极。
(2)写出A极、B极、C极、D极上的电极反应式。
A极上电极反应式为____________________________________________________。
B极上电极反应式为____________________________________________________。
C极上电极反应式为____________________________________________________。
D极上电极反应式为____________________________________________________。
(3)当电路中通过2.4081022个电子时,B极上沉淀出1.28gM,则M的相对原子质量为__________。
(4)如果将电池的正负极交换,接入原电路通过1.2041022个电子时,则 B极上的电极反应式为____________________________________________,A极上析出______ g ______(填物质名称),甲池的总反应式为________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com