
【题目】如图是两种溶液进行电解的装置。电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,B,C,D都是铂电极,P,Q是电池的两极,电路接通后,电极B上金属有M沉淀出来,

请回答下列问题:
(1)其中P是______极,B是______极。
(2)写出A极、B极、C极、D极上的电极反应式。
A极上电极反应式为____________________________________________________。
B极上电极反应式为____________________________________________________。
C极上电极反应式为____________________________________________________。
D极上电极反应式为____________________________________________________。
(3)当电路中通过2.4081022个电子时,B极上沉淀出1.28gM,则M的相对原子质量为__________。
(4)如果将电池的正负极交换,接入原电路通过1.2041022个电子时,则 B极上的电极反应式为____________________________________________,A极上析出______ g ______(填物质名称),甲池的总反应式为________________________________。
【答案】正 阴 M-2e- =M2+ M2+ + 2e- = M 4OH- - 4e- = 2H2O + O2↑ 2H+ + 2e- = H2↑ 64 4OH- - 4e- = 2H2O + 2↑ 0.64 铜 2Cu2+ + 2H2O ![]() 2Cu + O2↑ + 4H +
2Cu + O2↑ + 4H +
【解析】
电极A是由金属M制成的,M的硝酸盐的化学式为M(NO3)2,电路接通后,电极B上金属有M沉淀,则B电极M2++2e-=M,得电子,为电解池的阴极,则D为电解池的阴极,Q为电池的负极。
(1)电路接通后,电极B上金属有M沉淀出来,B电极得电子,作电解池的阴极,则B、D为电解池的阴极,A、C为电解池的阳极,P为电池的正极;
(2)A极为阳极,M失电子生成+2价的离子,则电极反应式为M-2e- =M2+;
B极为阴极,M2+得电子生成M,电极反应式为M2+ + 2e- = M;
C极为阳极,水失电子生成氧气和氢离子,电极反应式为2H2O - 4e- =4H++ O2↑;
D极为阴极,氢离子得电子生成氢气,电极反应式为2H+ + 2e- = H2↑;
(3)电路中通过2.408![]() 1022个电子时,即0.04mol电子,B极上析出的M的化合价由+2价变为0,其物质的量为0.02mol,其质量为1.28g,则摩尔质量=1.28g/0.02mol=64g/mol,相对原子质量为64;
1022个电子时,即0.04mol电子,B极上析出的M的化合价由+2价变为0,其物质的量为0.02mol,其质量为1.28g,则摩尔质量=1.28g/0.02mol=64g/mol,相对原子质量为64;
(4)将电池的正负极交换,B极为惰性电极,则做阳极,溶液中的水失电子生成氧气和氢离子,电极反应式为2H2O - 4e- =4H++ O2↑;电路通过1.204![]() 1022个电子时,即0.02mol,则有0.01molCu析出,即0.64g;则总反应式为2Cu2+ + 2H2O
1022个电子时,即0.02mol,则有0.01molCu析出,即0.64g;则总反应式为2Cu2+ + 2H2O ![]() 2Cu + 4H ++ O2↑。
2Cu + 4H ++ O2↑。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法不正确的是

A.a极反应:CH4 -8e-+4O2-=CO2+2H2O
B.A、C膜均为阳离子交换膜,B膜为阴离子交换膜,
C.可用铁电极替换阴极的石墨电极
D.a极上通入2.24 L(标准状况下)甲烷,阳极室Ca2+减少0.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丙苯(![]() )催化脱氢生成2-苯基丙烯(
)催化脱氢生成2-苯基丙烯(![]() ),下列有关这两种有机物说法不正确的是( )
),下列有关这两种有机物说法不正确的是( )
A.苯、异丙苯互为同系物
B.2-苯基丙烯最多有9个碳原子共平面
C.异丙苯一氯代物有5种同分异构体
D.在一定条件下,二者都能发生加聚反应合成高分化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有饱和硫酸钠溶液的烧杯中,保持温度不变,用惰性电极电解一定时间后( )
A. 溶液的pH值将增大B. 钠离子数和硫酸根离子数的比值将变小
C. 溶液的浓度逐渐增大,有一定量晶体析出D. 溶液的浓度不变,有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解CuCl2和CuSO4的混合溶液(物质的量浓度均为0.1mol/L)500 mL,当阴极析出4.8g固体时,在阳极可得到标准状况下的气体体积为( )
A. 1.68LB. 1.4LC. 3.36LD. 2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元弱酸(简写为H2B)溶液,按下式发生一级和二级电离:
H2B![]() H++HB-
H++HB-
HB-![]() H++B2-
H++B2-
已知相同浓度时的电离度a(H2B)>>a(HB-),现有下列四种溶液:
①0.01molL-1的H2B溶液
②0.01molL-1的NaHB溶液
③0.02molL-1的HCl溶液与0.04molL-1的NaHB溶液等体积混合后的溶液
④0.02molLL-1的NaOH溶液与0.02molL-1的NaHB溶液等体积混合后的溶液
下列说法错误的是( )
A.溶液④一定显碱性B.c(H2B)最大的是③
C.c(B2-)最小的是①D.c(H+)最大的是③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
2 H2(g)+ O2(g)= 2H2O(g)△H2
C(s)+ O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的△H为
A. 12△H3+5△H2-2△H1 B. 2△H1-5△H2-12△H3
C. 12△H3-5△H2-2△H1 D. △H1-5△H2-12△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂N205,装置图如下,下列说法正确的是( )

A. 图中B装置是原电池
B. N2O5在B池的c极区生成,其电极反应式为N2O4+2HNO3-2e-=2N2O5+2H+
C. A装置中通入O2一极的电极反应式为O2+2H2O+4e-=4OH-
D. 若A装置中通入SO2的速率为2.24Lmin-1(标准状况),为稳定持续生产,硫酸溶液的浓度应维持不变,则左侧水的流入速率应为14.6mLmin-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置可以验证非金属性的变化规律。
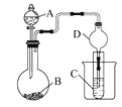
(1)仪器A的名称为________,干燥管D的作用是________________。
(2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。
(3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com