
【题目】某兴趣小组拟制备氯气并验证其一系列性质,实验装置如图所示![]() 省略夹持装置
省略夹持装置![]() 已知:硫代硫酸钠Na2S2O3溶液在工业上可作为脱氯剂
已知:硫代硫酸钠Na2S2O3溶液在工业上可作为脱氯剂

回答下列问题:
(1)仪器a的名称是______,其中盛有浓盐酸,烧瓶A中盛有的固体试剂是______![]() 填化学式
填化学式![]() .
.
(2)装置B中盛有饱和NaCl溶液,装置B的作用是______.
![]() 除去
除去![]() 中的杂质HCl
中的杂质HCl![]() 干燥
干燥 ![]() 提供后续水蒸气
提供后续水蒸气 ![]() 观察装置是否堵塞
观察装置是否堵塞
(3)![]() 处有色布条褪色,而d处不褪色,这说明______.
处有色布条褪色,而d处不褪色,这说明______.
(4)实验结束后,打开e的活塞,使其中的溶液流人到锥形瓶D中,摇匀锥形瓶,静置后可观察到______.
(5)装置E中发生反应的离子方程式为______.
【答案】 分液漏斗 KMnO4(或“KClO3”等) acd Cl2无漂白作用,HC1O起漂白作用 上层溶液为紫红色 S2O32+4Cl2+5H2O=2SO42+8Cl+10H+
【解析】由图中装置可知,装置A中放入KMnO4(或“KClO3”等)、分液漏斗中放入浓盐酸,产生的氯气通入饱和食盐水除去其中的氯化氢气体,然后通入C,干燥的有色布条,固体粒状干燥剂,可观察到c处布条褪色,d处不褪色,氯气通入漏斗D中,溶液变橙色,再滴入KI溶液与苯的分层的液体中,苯层呈紫色,最后多余的氯气用硫代硫酸钠溶液吸收,Na2S2O3中硫显+2价,被氯气氧化SO42-,以此来解答。
解析:
(1)仪器a具有玻璃活塞的漏斗,为分液漏斗,其中盛有浓盐酸,烧瓶A中在常温下氧化氯化氢制取氯气,可选择KMnO4(或“KClO3”等),反应为:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,故答案为:分液漏斗;KMnO4(或“KClO3”等);
(2)氯气难溶于饱和食盐水,但HCl极易溶于水,可用饱和食盐水除去氯气中少量的氯化氢气体,氯气通入C,干燥的有色布条,固体粒状干燥剂,可观察到c处布条褪色,d处不褪色,装置B提供后续水蒸气,发生堵塞时B中的,压强增大,B中长颈漏斗中液面上升,形成水柱,可观察装置是否堵塞,所以acd符合,故答案为:acd;
(3)向装置c中通入氯气,d处的有色布条不褪色,因为干燥的氯气不具备漂白性,c处的有色布条褪色,这说明氯气经过溶液B后带上了水,潮湿的氯气具有漂白性,真正起漂白作用的是氯气和水反应生成的次氯酸具有漂白性,故答案为:Cl2无漂白作用,HC1O起漂白作用;
(4)实验结束后,打开e的活塞,使其中的溶液流人到锥形瓶D中,溴水中加入苯振荡后苯层呈橙红发生萃取,苯的密度比水小,上层溶液为紫红色,故答案为:上层溶液为紫红色;
(5)Na2S2O3中硫显+2价,被氯气氧化SO42,则装置E中相应的离子反应方程式:S2O32+4Cl2+5H2O=2SO42+8Cl+10H+,故答案为:S2O32+4Cl2+5H2O=2SO42+8Cl+10H+


科目:高中化学 来源: 题型:
【题目】有机玻璃是由有机物X加聚制得的热塑性塑料,为透明如玻璃状的无色固体,可用以制造航空窗玻璃、仪表盘、外科照明灯、装饰品和生活用品等.其结构简式为: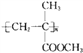 请回答下列问题:
请回答下列问题:
(1)写出X的结构简式_____________________;
(2)有机物X不能发生的反应有________(填写序号);
①和氢气加成 ②使溴水褪色 ③被酸性高锰酸钾溶液氧化 ④水解反应 ⑤酯化反应
(3)有机物X有多种同分异构体,其中含有2个甲基且属于羧酸类的有机分子的结构简式为________________________________(任写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2的漂白能力是漂白粉的4~5倍, NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下:
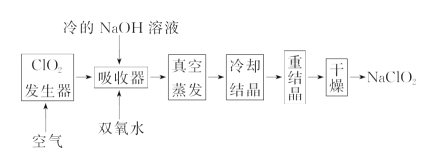
(1)ClO2气体发生器中的反应为:2NaClO3+SO2+H2SO4===2ClO2+2NaHSO4。实际工业生产中,可用硫黄、浓硫酸代替原料中的SO2,其原因为____________(用化学方程式表示)。
(2)反应结束后,向ClO2发生器中通入一定量空气的目的:________________________。
(3)吸收器中生成NaClO2的离子反应方程式为________________________________。
(4)CO和联氨(N2H4)的性质及应用的研究是能源开发、环境保护的重要课题。
①用CO、O2和KOH溶液可以制成碱性燃料电池,则该电池反应的离子方程式为_______________。
②用CO、O2和固体电解质还可以制成如下图所示的燃料电池,则电极d的电极反应式为__________。
(5)联氨的性质类似于氨气,将联氨通入CuO浊液中,有关物质的转化如图所示。
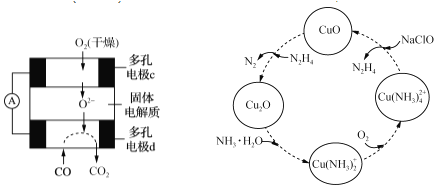
①在转化过程中通入氧气发生反应后,溶液的pH将________(填“增大”、“减小”或“不变”)。转化中当有1 mol N2H4参与反应时,需要消耗O2的物质的量为________。
②加入NaClO时发生的反应为:
Cu(NH3)42++2ClO-+2OH-=Cu(OH)2↓+2N2H4↑+2Cl-+2H2O
该反应需在80℃以上进行,其目的除了加快反应速率外,还有_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关乙烯和乙烷的说法中错误的是![]()
![]()
A. 乙烯是平面分子,乙烷分子中所有原子不可能在同一平面内
B. 溴的四氯化碳溶液和酸性![]() 溶液都可以鉴别乙烯和乙烷
溶液都可以鉴别乙烯和乙烷
C. 溴的四氯化碳溶液和酸性![]() 溶液都可以除去乙烷中混有的乙烯
溶液都可以除去乙烷中混有的乙烯
D. 乙烯的化学性质比乙烷的化学性质活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化氮![]() 是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和
是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和![]() ,请根据要求回答下列问题:
,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为 ______ .
(2)写出该反应的化学方程式 ______ ![]() 若反应中生成
若反应中生成![]()
![]() ,转移的电子数目为 ______ 个
,转移的电子数目为 ______ 个![]()
(3)![]() 是一种无色、无臭的气体,但一旦
是一种无色、无臭的气体,但一旦![]() 在空气中泄漏,还是易于发现
在空气中泄漏,还是易于发现![]() 你判断该气体泄漏时的现象是 ______ .
你判断该气体泄漏时的现象是 ______ .
(4)一旦![]() 泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除
泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除![]() 、NaF、
、NaF、![]() 外,还肯定有 ______
外,还肯定有 ______ ![]() 填化学式
填化学式![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下物质间的每步转化通过一步反应能实现的是( )
A. Al-Al2O3-Al(OH)3-NaAlO2 B. Si-SiO2-H2SiO3-Na2SiO3
C. Cu-CuO-Cu(OH)2-CuSO4 D. Na-Na2O2-Na2CO3-NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A和2 mol B气体置于1 L的密闭容器中,混合后发生如下反应:2A(s) + B(g)=2C(g)。若经2 s后测得C的浓度为1.2 mol/L,下列说法正确的是( )
A. 用物质A表示的反应速率为0.6mol/(L·s)
B. 用物质B表示的反应速率为1.2mol/(L·s)
C. 2 s时物质A的转化率为30%
D. 2 s时物质B的浓度为0.6 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。回答下列问题:
W | X | |||
Y | Z |
(1)X在元素周期表中的位置为____;画出X的简单离子结构示意图____。已知X元素的一种原子,其中子数为10,写出这种原子的原子符号_______。
(2)四种元素简单离子的半径由大到小为______(用离子符号表达)。
(3)W、X的最简单氢化物稳定性为____>____(填化学式)。
(4)Z最高价氧化物的水化物与Y最高价氧化物对应水化物反应的化学方程式为___ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com