
| A. | ②③ | B. | ②③④ | C. | ①②③⑤ | D. | 全部 |
分析 中学常见能与酸、碱反应的物质有:Al、氧化铝、氢氧化铝、弱酸铵盐、弱酸酸式盐、氨基酸、蛋白质等.
解答 解:①NaHCO3属于弱酸酸式盐,既能与盐酸反应又能与NaOH溶液反应,故①符合;
②Al2O3是两性氧化物,溶于强酸强碱,和盐酸反应生成氯化铝和水,与氢氧化钠溶液反应生成偏铝酸钠和水,故②符合;
③Al(OH)3是两性氢氧化物,能与盐酸反应生成氯化铝与水,与氢氧化钠反应生成偏铝酸钠与水,故③符合;
④Na2CO3与盐酸反应生成氯化钠、二氧化碳与水,不能与氢氧化钠反应,故④不符合;
⑤Al与盐酸反应生成氯化铝和氢气,和氢氧化钠溶液反应生成偏铝酸钠和氢气,故⑤符合,
故选C.
点评 本题考查了物质的性质,注意归纳总结中学常见能与酸、碱反应物质,注意基础知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | SiO2不能与HNO3、H2SO4等所有的酸反应 | |
| B. | CO2和SiO2的对应水化物都是酸,碳酸酸性比硅酸弱 | |
| C. | CO2与SiO2均是酸性氧化物,溶于水均得到相应的酸 | |
| D. | 硅胶常用于做干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 实验步骤和操作 | 实验现象 |
| 实验一 | (Ⅰ)取氯化亚铁固体[已部分变质,含有少量难溶于水的杂质Fe(OH)2Cl],向其中加入过量稀盐酸. (Ⅱ)再加入稍过量的铁粉,振荡. | 固体完全溶解,溶液呈黄绿色 Fe(OH)2Cl+2H+=Fe3++Cl-+2H2O |
| 实验二 | (Ⅰ)取实验一得到的溶液,加入KSCN溶液. (Ⅱ)再加入少量H2O2溶液. | 颜色无明显变化 溶液变红,有少量气泡 |
| 实验三 | (Ⅰ)取10mL 0.1mol/L KI溶液,滴加6滴0.1mol/L FeCl3溶液. (Ⅱ)取少量上述黄色溶液,滴加KSCN溶液. (Ⅲ)另取上述的黄色溶液,加入淀粉溶液. | 溶液呈黄色 溶液变红 溶液变蓝 |
| 实验四 | (Ⅰ)向实验三步骤I中所得的黄色溶液中加入2mL CCl4,充分振荡后,分离得到水层;重复操作三次. (Ⅱ)向步骤I中所得水层中加入KSCN溶液. | 颜色无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某同学利用图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )
某同学利用图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )| X气体 | Y试剂 | Z试剂 | |
| A. | NO2 | H2O | H2O |
| B. | CO2 | H2O | H2O |
| C. | HCl | 饱和食盐水 | 水 |
| D. | NO2和O2 | H2O | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液【FeCl3】:加足量铁粉 | B. | NaCl溶液【Na2SO4】:用Ba(OH)2溶液 | ||
| C. | Na2CO3固体【NaHCO3】:加热 | D. | 铁粉【铝粉】:用NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
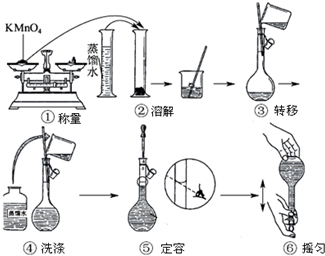
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 27克铝与足量的稀硫酸或氢氧化钠溶液充分反应,转移电子物质的量都为3 NA | |
| B. | 一瓶容积为22.4L 的NO2气体所含氮原子个数为NA | |
| C. | 浓度为0.2 mo1•L-1的CaC12溶液中,C1-离子的数目为0.4 NA | |
| D. | 标准状况下,22.4 L H2O含有的水分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下的某 NaF 溶液中,c(H+)=1×10-10 mol?L-1,说明 NaF 使水的电离减弱 | |
| B. | Mg 在空气中燃烧时发出耀眼的白光,一部分化学能转化为光能 | |
| C. | 纯碱溶于热水中去污效果增强,说明纯碱的水解是吸热反应 | |
| D. | 反应 N2(g)+3H2(g)═2NH3(g)(△H<0)达平衡后,降低温度,正、逆反应速率都减小,平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com