
【题目】H是一种新型香料的主要成分之一,其合成路线如下(部分产物和部分反应条件略去):
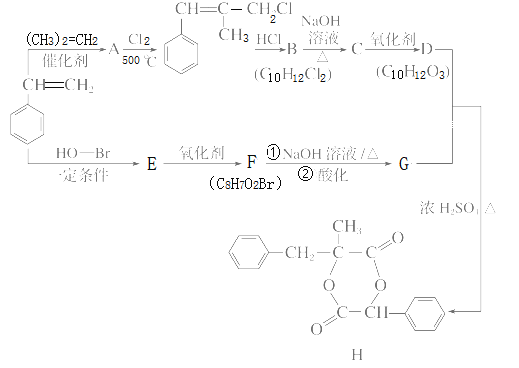
已知:①RCH==CH2+CH2==CHR′![]() CH2==CH2+RCH==CHR′;
CH2==CH2+RCH==CHR′;
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子。
请回答下列问题:
(1)(CH3)2C==CH2的同分异构体中存在顺反异构的有机物的名称为________________。
(2)A的核磁共振氢谱除苯环上的H外,还显示______组峰,峰面积比为____。
(3)D分子中含有的含氧官能团名称是____________________________, E的结构简式为____________________________________________。
(4) D和G反应生成H的化学方程式为_____________________________________。
(5)G的同分异构体中,同时满足下列条件的有种(不包括立体异构)_____________。
①苯的二取代物 ②与FeCl3溶液发生显色反应 ③含“-O-”结构
(6)参照上述合成路线,以丙烯为原料(无机试剂任选),设计制备2,3--丁二醇的合成路线________。
【答案】2—丁烯21∶6羟基、羧基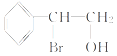
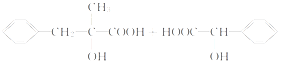
![]()
 12CH3CH===CH2
12CH3CH===CH2![]()

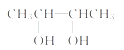
【解析】
根据信息可知,苯乙烯与(CH3)2C==CH2发生反应生成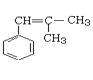 (A),发生取代生成
(A),发生取代生成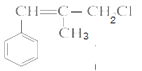 ,再与氯化氢发生加成生成
,再与氯化氢发生加成生成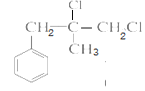 (B),在碱性环境下水解后最终氧化为(D)
(B),在碱性环境下水解后最终氧化为(D)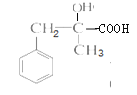 ;苯乙烯与HO-Br发生加成反应生成
;苯乙烯与HO-Br发生加成反应生成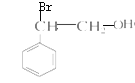 ;接着氧化为
;接着氧化为 ,碱性环境发生取代,酸化后生成
,碱性环境发生取代,酸化后生成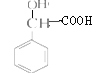 (G),最后
(G),最后 与
与 在浓硫酸作用下发生酯化生成环酯;据以上分析解答。
在浓硫酸作用下发生酯化生成环酯;据以上分析解答。
(1) (CH3)2C==CH2的同分异构体中存在顺反异构的有机物结构简式为CH3-CH=CH-CH3,双键在2号碳上,因此该有机物的名称为2—丁烯;正确答案:2—丁烯。
(2) 由信息方程式①![]() 可推
可推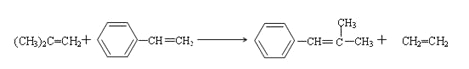 知,所以A为
知,所以A为 ;A的核磁共振氢谱除苯环上的H外,还显示2组峰,峰面积比为1:6;正确答案:2;1∶6。
;A的核磁共振氢谱除苯环上的H外,还显示2组峰,峰面积比为1:6;正确答案:2;1∶6。
(3)有机物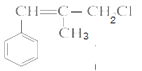 与氯化氢发生加成反应生成
与氯化氢发生加成反应生成 ,该有机物在氢氧化钠溶液中加热发生取代反应生成:
,该有机物在氢氧化钠溶液中加热发生取代反应生成: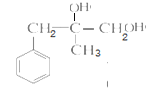 ,该有机物继续发生催化氧化生成(D)
,该有机物继续发生催化氧化生成(D) ;D中含有的官能团为羟基、羧基;苯乙烯与HO-Br发生加成反应生成
;D中含有的官能团为羟基、羧基;苯乙烯与HO-Br发生加成反应生成 ;正确答案:羟基、羧基;
;正确答案:羟基、羧基;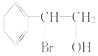 。
。
(4)有机物E为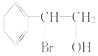 ,发生氧化反应变为
,发生氧化反应变为 ,该有机物在氢氧化钠溶液中加热发生反应,最后在酸化,得到有机物:
,该有机物在氢氧化钠溶液中加热发生反应,最后在酸化,得到有机物: (G),有机物(D)
(G),有机物(D) ;二者发生取代反应生成环状酯;反应的方程式为:
;二者发生取代反应生成环状酯;反应的方程式为: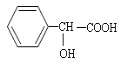 +
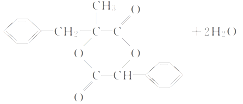
+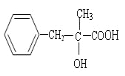 →
→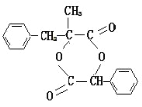 +2H2O;
+2H2O;
正确答案: +
+ →
→ +2H2O。
+2H2O。
(5) 有机物: (G),它的同分异构体满足:①苯的二取代物,环上有2个取代基;②与FeCl3溶液发生显色反应,环上有羟基;③含“-O-”结构;满足条件的有机物有:苯酚的环上连有-CH2COOH取代基,结构有3种,苯酚的环上连有-CH2-OOCH取代基,结构有3种,苯酚的环上连有-OOCCH3 取代基,结构有3种,苯酚的环上连有-COOCH3 取代基,结构有3种,总共有12种;正确答案:12。
(G),它的同分异构体满足:①苯的二取代物,环上有2个取代基;②与FeCl3溶液发生显色反应,环上有羟基;③含“-O-”结构;满足条件的有机物有:苯酚的环上连有-CH2COOH取代基,结构有3种,苯酚的环上连有-CH2-OOCH取代基,结构有3种,苯酚的环上连有-OOCCH3 取代基,结构有3种,苯酚的环上连有-COOCH3 取代基,结构有3种,总共有12种;正确答案:12。
(6)根据信息可知,2个丙烯分子间发生反应生成CH3-CH=CH-CH3,然后该有机物再与溴发生加成生成CH3-CHBr-CHBr-CH3,该有机物在碱性环境下发生水解生成目标产物;具体流程如下:CH3CH===CH2![]()

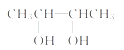 ;正确答案:CH3CH===CH2
;正确答案:CH3CH===CH2![]()

 。
。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.所含质子数和电子数相等的粒子一定是原子
B.具有相同核电荷数的原子或简单的离子,一定是同种元素
C.质量数相同的原子其化学性质一定相同
D.两种粒子如果核外电子排布相同,化学性质就一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向体积为2L的密闭容器中通入NO2 (气体)和N2O4 (无色气体),二者之间可相互转化,反应过程中各物质的物质的量随时间的变化曲线如图所示。回答下列问题:

(1)0~3min内用N2O4表示的平均反应速率为___________。
(2)若升高温度,则v(正)__________(填“加快”“减慢”或“不变”,下同),v(逆)___________。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得:甲中v(NO2)=0.2mol·L-1·s-1,乙中v(N2O4)=9mol·L-1·min-1,则_________(填“甲”或“乙”)中反应更快。
(4)下列叙述能说明该反应已达到化学平衡状态的是(_____)
A v(NO2)=2 v(N2O4)
B 容器内压强不再发生变化
C X的体积分数不再发生变化
D 容器内气体的原子总数不再发生变化
E 相同时间内消耗n mol Y的同时生成2n mol X
F 相同时间内消耗n mol Y的同时消耗2n mol X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是( )
A. 用湿润的pH试纸测稀碱液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D. 测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含氮化合物对能源、环保和生产具有重要的意义。请回答下列问题:
(1)在2 L密闭容器内, 800 ℃时反应2NO(g)+O2(g) ![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①如图所示A点处v正___(填“>”、“<”或“=”,下同)v逆,A点处v正___B点处v正。
②如图所示的曲线,其中表示NO2的变化的曲线是________(填a、b、c、d等字母)。用O2表示2 s内该反应的速率v=________。
(2)已知化学反应N2+3H2![]() 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,
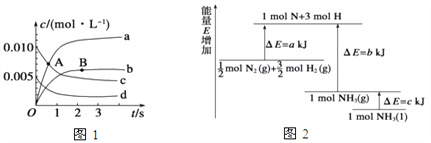
则,1 mol N和3 mol H生成1 mol NH3(g)是______能量的过程(填“吸收”或“释放”),由![]() mol N2(g)和
mol N2(g)和![]() mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。
mol H2(g)生成1 mol NH3(g)过程________(填“吸收”或“释放”)_______kJ能量(用含字母a、b、c的关系式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50 mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),随后取此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO2气体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
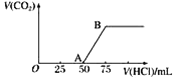
A. OA段所发生反应的离子方程式:H++OH-===H2O
B. NaOH在吸收CO2后,所得溶液的溶质为NaOH和Na2CO3,其物质的量浓度之比为1∶1
C. 产生的CO2体积(标准状况下)为0.056 L
D. 稀释液中NaOH的物质的量浓度为0.025 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题。
(1)写出下列基团(或官能团)的名称或结构简式:-OH________ 、 碳碳双键__________、
(2)相对分子质量为72且沸点最低的烷烃的结构简式_______________;
(3)对下列物质进行系统命名:
![]() :__________;CH2=CHCH2CH3:_______________;
:__________;CH2=CHCH2CH3:_______________;
(4)分子式为C4H8O2的同分异构体中,属于酯类的有______种;
(5)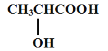 形成六元环酯的产物的结构简式__________________________。
形成六元环酯的产物的结构简式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素且原子序数依次增大,元素Y和W同族。盐ZWX与浓盐酸反应,有黄绿色气体产生,此气体同冷烧碱溶液作用,可得到含ZWX的溶液。根据以上信息,试判断下列问题:
(1)写出这四种元素的元素符号:X_____、Y_____、Z____、W____,并将这四种元素的原子按照半径由大到小的顺序排列______(用具体的元素符号作答)
(2)Y的氢化物稳定性_________W的氢化物稳定性(填“大于”或“小于”),Y的氢化物水溶液酸性_________W的氢化物水溶液的酸性(填“大于”或“小于”)。
(3)写出Z2X2的电子式_____,该物质所含化学键的类型有_________。0.1 mol该物质与水反应转移电子数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液中滴入氢氧化钠溶液后。先产生白色沉淀,然后变为灰绿色,最后变为红褐色,说明该溶液中存在( )
A.NO3-B.Fe2+C.SO42-D.Ca2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com