
【题目】按要求回答问题。
(1)写出下列基团(或官能团)的名称或结构简式:-OH________ 、 碳碳双键__________、
(2)相对分子质量为72且沸点最低的烷烃的结构简式_______________;
(3)对下列物质进行系统命名:
![]() :__________;CH2=CHCH2CH3:_______________;
:__________;CH2=CHCH2CH3:_______________;
(4)分子式为C4H8O2的同分异构体中,属于酯类的有______种;
(5)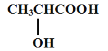 形成六元环酯的产物的结构简式__________________________。
形成六元环酯的产物的结构简式__________________________。
【答案】 羟基 ![]() (CH3)4 C 2-甲基戊烷 1-丁烯 4
(CH3)4 C 2-甲基戊烷 1-丁烯 4 ![]()
【解析】(1)结合常见的官能团的名称和结构简式判断;
(2)根据烷烃的通式为CnH2n+2,求出n,确定分子式,写出可能结构简式;
(3)根据烷烃、烯烃的系统命名规则确定所给结构简式的名称;
(4)写出同分异构体,根据官能团分类方法确定属于酯的同分异构体数目;
(5)醇和羧酸发生酯化反应形成环酯确定生成物的结构简式。
(1)根据官能团的名称,-OH 为羟基,碳碳双键为![]() ,正确答案为:羟基;
,正确答案为:羟基;![]() ;
;
(2)烷烃的通式CnH2n+2,该烷烃的相对分子质量为72,所以有:12n+2n+2=72,即14n=70,解得n=5,即分子式为C5H12,结构简式有:CH3CH2CH2CH2CH3,(CH3)2CHCH2CH3,(CH3)4 C,沸点最低的是:(CH3)4 C,正确答案:(CH3)4 C;
(3)根据烷烃的系统命名规则,![]() 的名称是:2-甲基戊烷;根据烯烃的系统命名规则,CH2=CHCH2CH3的名称是1-丁烯,正确答案: 2-甲基戊烷; 1-丁烯;
的名称是:2-甲基戊烷;根据烯烃的系统命名规则,CH2=CHCH2CH3的名称是1-丁烯,正确答案: 2-甲基戊烷; 1-丁烯;
(4)C4H8O2属于酯类的同分异构体有:HCOOCH2CH2CH3、HCOOCH(CH3)2、CH3COOC2H5、CH3CH2COOCH3,所以属于酯类的同分异构体有4种,正确答案:4
(5)根据酯化反应中醇脱羟基上的氢原子,羧酸脱羧基上的羟基,对于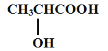 ,要形成六元环的酯,需要2分子
,要形成六元环的酯,需要2分子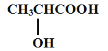 相互脱水,形成六元环酯的产物的结构简式为:
相互脱水,形成六元环酯的产物的结构简式为:![]() ,正确答案:
,正确答案:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列溶液中导电性最强的是
A. 1L0.1mol/L醋酸B. 0.1L 0.1mol/L H2SO4溶液
C. 0.5L 0.1mol/L盐酸D. 2L 0.1mol/L H2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下:

实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气.
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热D并关闭旋塞.
③向装置A中b容器内充入加热介质并加热到210一220℃,然后通入N2O.
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩、结晶.
⑤过滤,用乙醚洗涤,晾干.
已知:NaNH2熔点210℃,沸点400℃,在水溶液中易水解.
回答下列问题:
(1)图中仪器a用不锈钢材质而不用玻璃,其主要原因是___.
(2)装置B中盛放的药品为___;装置C的主要作用是___.
(3)步骤①先加热通氨气的目的是___;步骤②氨气与熔化的钠反应的方程式为___.
(4)步骤③b容器充入的介质为植物油,进行油浴而不用水浴的主要原因是___.
(5)生成NaN3的化学方程式为___.
(6)步骤⑤用乙醚洗涤的主要目的是___.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种新型香料的主要成分之一,其合成路线如下(部分产物和部分反应条件略去):
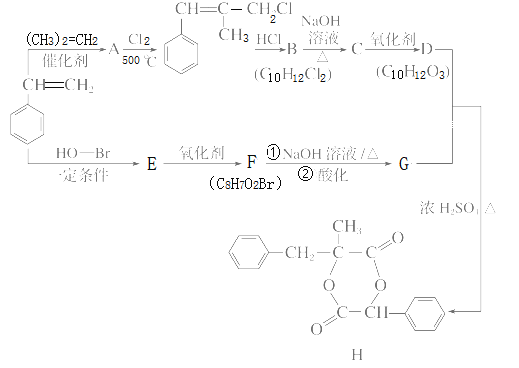
已知:①RCH==CH2+CH2==CHR′![]() CH2==CH2+RCH==CHR′;
CH2==CH2+RCH==CHR′;
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子。
请回答下列问题:
(1)(CH3)2C==CH2的同分异构体中存在顺反异构的有机物的名称为________________。
(2)A的核磁共振氢谱除苯环上的H外,还显示______组峰,峰面积比为____。
(3)D分子中含有的含氧官能团名称是____________________________, E的结构简式为____________________________________________。
(4) D和G反应生成H的化学方程式为_____________________________________。
(5)G的同分异构体中,同时满足下列条件的有种(不包括立体异构)_____________。
①苯的二取代物 ②与FeCl3溶液发生显色反应 ③含“-O-”结构
(6)参照上述合成路线,以丙烯为原料(无机试剂任选),设计制备2,3--丁二醇的合成路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2010年诺贝尔物理学奖所指向的是碳的又一张奇妙脸孔:人类已知的最薄材料——石墨烯。下列说法中,正确的是 ( )

A. 固态时,碳的各种单质的晶体类型相同
B. 石墨烯含有极性键
C. 从石墨剥离得石墨烯需要破坏化学键
D. 石墨烯具有导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
X | L层p电子数比s电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有三个未成对电子 |
(1)写出元素X的离子结构示意图____________。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式______________
(3)写出Y的价电子排布式_________________________。
(4)元素T与氯元素相比,非金属性较强的是_______(用元素符号表示),下列表述中能用于证明这一事实的是_______(填字母代号)。
A.气态氢化物的挥发性 B.两元素的电负性
C.含氧酸的酸性 D.氢化物中X—H键的键长(X代表T和Cl两种元素)
(5)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___(填元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界上最旱发现并使用锌的是中国,明朝末年《天工开物》一书中有世界上最早的关于炼锌技术的记载。回答下列问題:
(1)基态Zn原子的核外电子所占据的最高能层符号为_____________,Zn2+基态核外电子排布式为_______________________。
(2)硫酸锌溶于过量的氨水可形成[Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中阴离子的空间构型为 _____________(用文字描述);
②SO42-中,中心原子的轨道杂化类型为______________;
③写出一种与SO42-互为等电子体的分子的化学式_____________;
④NH3极易溶于水,除因为它们都是极性分子外,还因为_______________________。
(3)Zn与S所形成化合物晶体的晶胞如图所示。
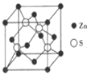
①该化合物的化学式为___________;
②已知该晶体的晶胞参数a=541 pm,其密度为___________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油条和豆浆是我国传统的早餐食物,炸油条时常用到一种白色物质,它既能中和发酵过程中产生的酸,又能起发泡作用,这种白色物质是
A. NaOH B. Ca(OH)2 C. NaHCO3 D. NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com