
����Ŀ��A��B��C��D��E��Ϊ�л������A�Ƿ���ʽΪC5H10O��ֱ�������B��NaHCO3��Һ��ȫ��Ӧ�������ʵ���֮��Ϊ1��2������֮��Ĺ�ϵ��ͼ��ʾ����ʾ��RCH=CHR�������Ը��������Һ�з�Ӧ����RCOOH��R��COOH������R��R��Ϊ���������������������ǣ� ��
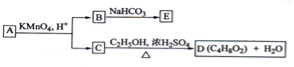
A��B�Ľṹ��ʽΪHOOC��CH2��COOH
B��C���Ҵ�������������Ӧ
C��A�Ľṹ��ʽ��CH3��CH��OH����CH=CH��CH3
D��E�ķ���ʽΪC3H2O4Na2
���𰸡�C
��������
���������A�ķ���ʽΪC5H10O�������Ͷ�Ϊ��2��5+210��/2=1�������Ը��������������B��C������Ϣ��֪��A����1��C=C˫����B��C�������Ȼ���C���Ҵ�����������Ӧ����DΪC4H8O2����CΪCH3COOH��DΪCH3COOC2H5��B��̼ԭ����ĿΪ3������̼�����ư�1��2��Ӧ����B�����к���2���Ȼ�-COOH��˵��A�����л�����1��-OH����A�Ľṹ��ʽΪCH3CH=CHCH2CH2OH����BΪHOOCCH2COOH����̼�����Ʒ�Ӧ����EΪNaOOCCH2COONa��A��������������֪��BΪHOOCCH2COOH��A��ȷ��B��C�����Ȼ������Ҵ�����������Ӧ��B��ȷ��C��A�Ľṹ��ʽΪCH3CH=CHCH2CH2OH��C����D��EΪNaOOCCH2COONa������ʽΪC3H2O4Na2��D��ȷ����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Na2O2��˵���У�����ȷ����
A. ��dz��ɫ���� B. ������������
C. ��H2O��Ӧʱ��H2O����ԭ�� D. ��H2O��Ӧʱ���ų�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ĸ�ҹ���������������ƣ�NaNO2���������س��������ʳ�õ�˵����ij��ȤС�鿪չ����̽�����
�һ����������,NaNO2�ж������������Ժͻ�ԭ�ԣ�NaNO2��Һ�Լ��ԣ������ڷ��ù����У�NaNO3��ת��ΪNaNO2�����ҹ涨����Ʒ��NaNO2�������ܳ���30mg/kg��
���������NaNO2��ʳ��

��1��NaNO2��ʳ�ε�������ƣ��ױ�����ʳ�����ã�����ʳ�ס����ۺ�KI��Һ������ʹ�����Һ��������NaNO2 ��ͬʱ����һ����ɫ���壬����������������Ϊ����ɫ������ɫ���廯ѧʽΪ___��
�����̽��NaNO3��NaNO2���ת��
��2����ȡNaNO2��NaNO3�����Һ��װ��ʾ��ͼ���£���֪��2NO2+2NaOH=NaNO2+NaNO3+H2O����װ��III�з�Ӧ��ȫ�������IJ������ȴ�a���ٹر�b����II�п���ѡ�õ���ҺΪ_________
A. NaCl B. H2O C. H2SO4 D. NaOH
��3����NaNO2��NaNO3�����Һ¶���ڿ�������ҹ�����Һ��pH��С��ԭ�������_________���û�ѧ����ʽ���ͣ���
��ģ����������NaNO2�����ı仯
��4���ֱ�� 1000g���������� 1000g��ҹ��������ȡNaNO3��NaNO2�������Һ���ٷֱ���0.00500mol��L�ĸ������(����)��Һ�ζ����������������12.00mL����ҹ������20.00mL������֪��2MnO4һ+5 NO2һ+6H+=2 Mn2++5NO3һ+3 H2O���ٵζ��յ���ж�����Ϊ_____
�ڸ�ҹ������NaNO2�ĺ�����_____mg��kg��������λ��Ч���֣�
��壺�ۺ�����ʵ��Ͳ������ϻ�֪��������ϸ���������£�NaNO3����ת��ΪNaNO2��ֻҪ����õ�����ҹ�Կ�ʳ�á�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܴﵽʵ��Ŀ���ǣ�������
A.����ˮ���ռ�ͭ����Ũ���ᷴӦ������NO2
B.�ð�ˮ����NaCl��MgCl2��AlCl3��NH4Cl������Һ
C.������KMnO4��Һ��֤����Ļ�ԭ��
D.�ñ���NaHCO3��Һ��ȥCl2�л��е�HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ���壨MgSO4��7H2O����һ����Ҫ�Ļ���ԭ�ϡ�����þ����Ҫ�ɷ���MgCO3��������FeCO3�Ͳ��������ʣ�Ϊԭ����ȡ����þ������������£�

��1��MgCO3����ϡ��������ӷ���ʽ��_________________________��
��2������H2O2��Һ��Ŀ����____________________�������ӷ���ʽ��ʾ����
��3����֪������������������������ʽ����ʱ��Һ��pH���±���
������ | Mg2+ | Fe2+ | Fe3+ |
��ʼ���� | 9.1 | 7.6 | 1.9 |
��ȫ���� | 11.1 | 9.7 | 3.2 |
�������������У��ð�ˮ������ҺpH�ķ�Χ��______________________________��
��4�������ˡ�������Һ�д��ڴ�������������Mg2+��____________��
��5�����ᾧ��������������Ũ����Һ��ʹ�õ�����������̨���ƾ��ƺ�_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���������ճ�������������Ҫ��Ӧ�ã�����˵������ȷ����
A�������������ͻ����
B��Na2O������DZˮͧ�������ߵĹ�����
C�����������Ʊ�ľ�ķ������ԭ��
D��FeCl3��Һ�����ڿ���ӡˢͭ��·��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015�꣬�й���ѧ����ӴӴ��������ű����ҩ�������ػ����ŵ�������������ؽṹ��ʽ��ͼ��ʾ����֪һ��̼ԭ��������4����ͬ��ԭ�ӻ���ţ���̼ԭ�ӳ��ˡ�����̼ԭ�ӡ��������й������ص�˵������ȷ���ǣ� ��
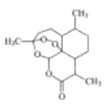
A. �����ط�����6������̼ԭ��
B. �����صĻ�ѧʽΪ��C15H22O5
C. ��������һ������������NaOH��Һ��Ӧ������������
D. ������������ˮ����ȡ�ķ��������л��ܼ���ȡ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ġ������̸���м��أ�������ժ��δ�죬ÿ����ľ����ö���룬��������������ɬζ���������ִ��Ƽ��۵㣬�����е���������ָ
A. ��ϩB. ������C. ������D. ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ؼ��仯�����Ӧ���о���Ŀǰ��ѧ�о���ǰ��֮һ���Իش��������⣺
��1��ԭ������С��36�Ĺ���Ԫ��A��B�������ڱ���λ��ͬһ�壬��ԭ������B��A��1����̬Bԭ���к�������δ�ɶԵ��ӡ���д��BԪ�������ڱ��е�λ��Ϊ______������___��Ԫ�أ�A2���ڻ�̬ʱ�۵����Ų�ͼΪ__________________��
��2������������������ܽ�������Ⱦ���ȩ�������к������ת��Ϊ������̼��ˮ���ﵽ������ˮ��������ԭ�Ӽ۲���Ӷ���Ϊ____��������̼��VSEPRģ��Ϊ______����������̼ԭ�ӵ��ӻ�����Ϊ________��
��3��Co3+�ж���������Co(CN)63����Co(NH3)4Cl2+ �ȡ��Rh����������ͬ��Ԫ�أ�ijЩ�������ơ��������ij�����ΪCsRh(SO4)2��4H2O�����ܽ���ˮ������ˮ��Һ�м���һ��Ũ�ȵ�BaCl2��Һ���������ɡ������������ӵ���λ��Ϊ____����д�������ܽ���ˮ��ĵ��뷽��ʽ��_________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com