
����Ŀ������������ѿ�ӷ���[��Ҫ��Mg(OH)Br���Լ�����NH4Cl�Ͳ�����ˮ���л��ܼ���]��ȡ�������ʵ��������ͼ��
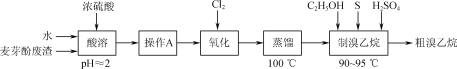
��1����������ʱ��ˮ�������������ԼΪ2��1����ˮ�����˹��ٵ�ԭ����___��
��2��������A����������____��
��3������������Br2ʱ�����ʺϵļ��ȷ�����____��
��4����������������װ����ͼ��ʾ��
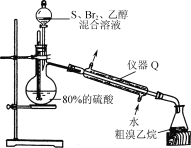
��ͼ������Q��������____��
����ƿ�����������顢����Ļ�ѧ����ʽΪ___��
��5����ƽ�����������д�����ʵ�鷽����___���ô��������������[ʵ���б���ʹ�õ��Լ�������ˮ����ˮCaCl2��1%��NaOH��Һ]��
���𰸡��������ɵ�����þ�ᾧ������Ӱ��������� ��Һ ��ˮԡ ������ 3Br2+S+6C2H5OH![]() 6C2H5Br+2H2O+H2SO4 ��������������1%��NaOH��Һϴ��1��2�Σ���������ˮϴ��2��3�Σ��������ˮCaCl2����
6C2H5Br+2H2O+H2SO4 ��������������1%��NaOH��Һϴ��1��2�Σ���������ˮϴ��2��3�Σ��������ˮCaCl2����
��������
��Ũ�����ܽ�������ѿ�ӷ���[��Ҫ��Mg(OH)Br���Լ�����NH4Cl�Ͳ�����ˮ���л��ܼ���]����������ҺpH=2���ٷ�Һ��ȥ�л��ܼ�������ˮ��Һ��ͨ�����������������Һ�е�Br-����Br2������������������������������£���S��C2H5OH��ϼ����Ƶô������顣
(1)��������ʱ�����ɵ�MgSO4���γɾ��壬���ˮ�����˹��٣�Ŀ���DZ������ɵ�����þ�ᾧ������Ӱ�����������
(2)�л��ܼ���ˮ��Һ�������ܣ��ֲ㣬��ѡ���Һ�������뼴�ɣ�
(3)Br2�ӷ�������ʵ�����̣������¶�Ϊ100��������������Br2ʱֻҪѡ���ˮԡ���ɣ�
(4)��ͼ������Q�������������ܣ�
�������������£�Br2��S��C2H5OH��ϼ����Ƶ������飬Br2����ԭ����S��������������Ӧ�Ļ�ѧ����ʽΪ3Br2+S+6C2H5OH![]() 6C2H5Br+2H2O+H2SO4��
6C2H5Br+2H2O+H2SO4��
(5)���������л����������ˮ�������������д�����ʵ�鷽���ǽ�������������1%��NaOH��Һϴ��1��2�Σ���������ˮϴ��2��3�Σ��������ˮCaCl2���T�ɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯һ�����ڻ�ѧ�仯���ǣ� ��
�ٽ������� ��ȼ�� ��ú�ĸ��� ����ɫ��Ӧ ����ˮ����ͭ��ˮ ��ҵ������ �߰���ת��ɺ��� �����Ũ������ �ᶡ������� ��ú�AҺ��
A.�٢ܢ�B.�ޢ��C.�ڢޢ�D.�ڢۢݢߢ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ڿ��淴ӦA(g)+2B(g)![]() 3C(g)�����������У���˵����Ӧ�Ѵﵽƽ�����
3C(g)�����������У���˵����Ӧ�Ѵﵽƽ�����
A.��λʱ��������a mol A��ͬʱ����3a mol CB.�����ڵ�ѹǿ���ٱ仯
C.![]() D.C������������ٱ仯
D.C������������ٱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2�㷺����ˮ������ֽ��Ư�ȡ�
��1���Ʊ�ClO2ԭ����NaClO2�ȣ�������ClO2(g)������ˮ���յõ�����ҺA��
��ClO2����Ԫ�صĻ��ϼ�Ϊ___��
��NaClO2��������������������ClO2����(������������Cl2)��д���䷴Ӧ����ClO2��NaCl��ˮ�Ļ�ѧ����ʽ��___��
��2���������ⶨClO2����ҺA��ClO2��Cl2��Ũ�ȵ���Ҫʵ�鲽�����£�
����1.����ƿ�м���50mL����ˮ��25mL100g��L-1KI��Һ(����)���������м���5.00mLClO2����Һ(������Ӧ��2ClO2+2KI=2KClO2+I2��Cl2+2KI=2KCl+I2)��
����2.��0.1000mol��L-1Na2S2O3����Һ�ζ�(2Na2S2O3+I2=2NaI+Na2S4O6)��dz��ɫ���ټ���1mL������Һ�������ζ�����ɫ�պ���ʧ������Na2S2O3��Һ6.00mL��
����3.����2����Һ�м���5mL2mol��L-1������Һ�ữ��������Ӧ��KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O��
����4.�ظ�����2�������ڶ��εζ�������0.1000mol��L-1Na2S2O3��Һ20.00mL��
�����������ݣ�����ClO2����ҺA��ClO2��Cl2��Ũ��___(��λg��L-1��д���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ۺ���������ĩ�Ļ�����Ƴɵ����ȼ������ں��Ӹֹ졣��ȡ��ͬ�����ĸ����ȼ��ֱ��100mLͬŨ�ȵ�NaOH��Һ��Ӧ����ȡ���ȼ����������������������ϵ���(����������ڱ�״���²ⶨ)��
�� | �� | �� | |
���ȼ�����/g | 7.5 | 15.0 | 20.0 |
�������/L | 3.36 | 6.72 | 6.72 |
���㣺
��1��NaOH��Һ���ʵ���Ũ��_______
��2�������ȼ���������������_______
��3��15g�����ȼ��������ȷ�Ӧ�����ϲ�������������_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��֪�ɽ������Ƶ������ƣ����ö��ַ�����a.4Na��O2===2Na2O��b.4Na��CO2===2Na2O��C��c.2NaNO2��6Na===4Na2O��N2����
�����������ַ����У���õķ�����________(�����)��ԭ����________________��
��������Ӧc��NaNO2��________��������1 mol NaNO2��Ӧʱ������ת�Ƶ���Ŀ��________________________________________________________________________��
(2)���ý����ƺͿ����Ʊ����Ƚϸߵ�Na2O2�������õ�װ�����¡��ش���������(ע��Na2O2������H2O��CO2��Ӧ)��
��װ�â���ʢ�ŵ�ҩƷ��________����������____________________________��


�����涨�����������������ң������ʵ��װ��ʱ�������ӿڵı����ĸ(a��b����)˳��������________��________��________��________��________��________��________��
��װ�â������____________________________________________________��
�ܲ�����ͨ�����ͼ��ȵ�˳��Ϊ________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1L0.01mol��L��1һԪ��HR��Һ����ͨ�백���۳�����NH3��H2O����ƽ�ⳣ��K��1.76��10��5�ݣ������¶Ⱥ���Һ������䣬�����Һ��pH������Ũ�ȱ仯�Ĺ�ϵ��ͼ��ʾ��������������ȷ����
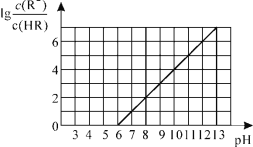
A.0.01mol��L��1HR��Һ��pHԼΪ4
B.���Ű�����ͨ�룬![]() ��С
��С
C.����ҺΪ����ʱ��c��R������c��HR��
D.��ͨ��0.01 mol NH3ʱ����Һ�д��ڣ�c��R������c��NH4+����c��H+����c��OH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ�еĨO��H�O�ܱ�ʾ��ȼ���ȼ���ȵ��ǣ� ��
A.H2��g��+![]() O2��g��=H2O��1����H=-285.8kJ/mol-1
O2��g��=H2O��1����H=-285.8kJ/mol-1
B.H2��g��+C12��g��=2HCl��g����H=-184.6kJ/mol-1
C.2CO��g��+O2��g��=2CO2��g����H= һ566kJ/mol-1
D.CH4��g��+2O2��g��=2H2O��g��+CO2��g����H= һ802.3kJ/mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ұ���ķ���������Ϊԭ����ȡ��ϸ��-���������Ƚ��ͻ�����Ⱦ�ֿ��������Դ�������ʡ���֪���ҵ���Ҫ�ɷ�ΪAl2O3������������SiO2��FeO��Fe2O3�������Ʊ�ʵ���������£�
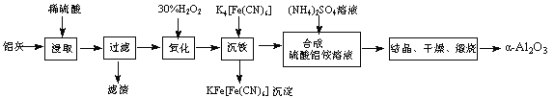
��1�������������������ᷴӦ�Ļ�ѧ����ʽΪ ��
��2��ͼ��������������Ҫ�ɷ�Ϊ (�ѧʽ)��
��3����30%��H2O2��Һ���������ӷ�Ӧ����ʽΪ ��
��4������������茶��壬��������Ҫ��ӦΪ��
4[NH4Al(SO4)2��12H2O]![]() 2Al2O3+ 2NH3��+ N2��+ 5SO3��+ 3SO2��+ 53H2O,������������ͨ����ͼ��ʾ��װ�á�
2Al2O3+ 2NH3��+ N2��+ 5SO3��+ 3SO2��+ 53H2O,������������ͨ����ͼ��ʾ��װ�á�
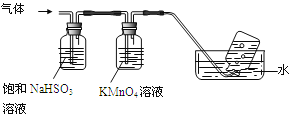
������ƿ���ռ����������� (�ѧʽ)��
����������NaHSO3��Һ���յ����ʳ���H2O��g����� (�ѧʽ)��
��KMnO4��Һ��ɫ��MnO4����ԭΪMn2+�������������ӷ�Ӧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com