
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ?mol-1 | 890.3 | 1299.6 | 285.8 |
| A、C≡C键能为796.0 kJ?mol-1 |
| B、C-H键键长小于H-H键 |
| C、2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ?mol-1 |
| D、2CH4(g)═C2H2(g)+3H2(g)△H=-376.4 kJ?mol-1 |
| 5 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
| A、20mL 0.3mol?L-1 Na2CO3 |
| B、10mL 0.4mol?L-1 Na2CO3 |
| C、25mL 0.4mol?L-1 Na2CO3 |
| D、15mL 0.5mol?L-1 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将水杨酸、乙酸酐和浓硫酸在锥形瓶中混合后,85-90℃水浴加热5-10min,取出锥形瓶,置于冰水浴中,使阿司匹林结晶析出,为了使其结晶完全需要向锥形瓶中继续加适量的水 |
| B、用移液管取液后,将移液管稍倾斜放入锥形瓶中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
| C、相同条件下,10mL 0.1mol/L FeCl2溶液中滴入1mL 0.1mol/L NaNO2溶液,溶液颜色由浅绿色变成黄色,10mL 0.1mol/L KI溶液中滴入1mL 0.1mol/L NaNO2溶液,溶液颜色无变化,说明溶液的pH会影响NO2-的氧化性 |
| D、为了检验火柴头中的硫元素,先用刀片削下几根火柴的火柴头,放入一支中号试管中,先用酒精灯加热该试管底部引燃“火药”,然后塞上橡皮塞待用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
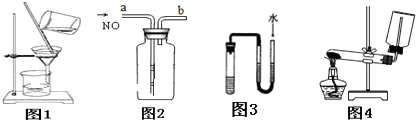
| A、分离乙醇和乙酸乙酯的混合物 |
| B、用图2装置收集一瓶纯净的NO |
| C、用图3装置中U型管两端有液面差且保持不变时证明装置不漏气 |
| D、用图4装置制取并收集氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、普通玻璃、水泥成分中都含有O、Si、Al三种元素 |
| B、从海水中制备Na、Mg、Al三种元素单质的反应都是氧化还原反应 |
| C、电解熔融状态的SiO2、Al2O3可以制得Si、Al,且都有氧气生成 |
| D、加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5受到普遍的关注,因为PM2.5在空气中形成了气溶胶,富含大量的有毒、有害物质,对空气质量影响较大(PM2.5是指大气中直径接近于2.5×10-6m的颗粒物) |
| B、李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法、元素分析仪都是元素定性分析法 |
| C、泡沫灭火器是最常见的灭火器之一,其内筒为塑料桶,盛有碳酸氢钠溶液;外筒为铁桶,外筒和内筒之间装有硫酸铝溶液 |
| D、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、反应过程a有催化剂参与 |
| B、该反应为放热反应,热效应等于△H |
| C、改变催化剂,可改变该反应的活化能 |
| D、在催化剂条件下,反应的活化能等于E1+E2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 操作及现象 | 结论 |
| A | 将0.1mol?L-1氨水稀释成0.01mol?L-1,测得pH由11.1变成10.6 | 稀释后NH3?H2O的电离程度减小 |
| B | 常温下,测得饱和Na2CO3溶液的pH大于饱和NaHCO3溶液 | 常温下水解程度:CO32->HCO3- |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 将固体CaSO4加入Na2CO3饱和溶液中,一段时间后,检验固体成分为CaCO3 | 同温下溶解度:CaSO4<CaCO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 |
 |
 |
 |
| A.检验SO2具有漂白性 | B.配制0.1mol?L-1NaOH溶液时定容 | C.分离出碘水中的碘 | D.配制一定浓度硫酸溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com