
 |
 |
 |
 |
| A.检验SO2具有漂白性 | B.配制0.1mol?L-1NaOH溶液时定容 | C.分离出碘水中的碘 | D.配制一定浓度硫酸溶液 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ?mol-1 | 890.3 | 1299.6 | 285.8 |
| A、C≡C键能为796.0 kJ?mol-1 |
| B、C-H键键长小于H-H键 |
| C、2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ?mol-1 |
| D、2CH4(g)═C2H2(g)+3H2(g)△H=-376.4 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
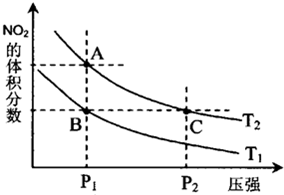 试运用所学知识,解决下列问题:
试运用所学知识,解决下列问题:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
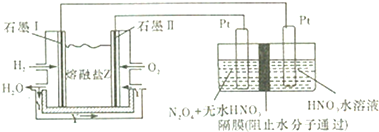
| A、石墨Ⅱ电极上发生反应的电极反应式为:O2+4e-+2CO2═2CO32- |
| B、在电解池中生成N2O5的电极反应式为:N2O4+2NO3--2e-═2N2O5 |
| C、放电时熔融盐中CO32-向石墨I电极方向移动 |
| D、每消耗11.2L氢气,理论上可以制得108g N2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用食醋除去水壶内的水垢:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| C、FeBr2溶液中通入少量Cl2:2Br-+Cl2═Br2+2Cl- |
| D、在NaHCO3溶液中加入少量石灰水:2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、Ag+、NO3- 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| D、NH4+、Al3+、SO42-、CH3COOH 要求:逐滴滴加NaOH溶液立刻有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、30g SiO2含有NA个Si-O共价键 |
| B、1L 0.2mol?L-1 Al2(SO4)3溶液中的离子总数为NA |
| C、标准状况下,22.4L H2O所含原子个数大于3NA |
| D、含4mol HCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有②④ | B、只有④ |
| C、只有②③④ | D、只有①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com