



| 80 |
| 66.1% |
| 41 |
| 12 |
| 80 |
| 66.1% |
| 41 |
| 12 |
| �������� |
| �������� |
| �� |
| �� |
| �� |
| �� |


 ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
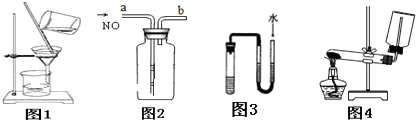
| A�������Ҵ������������Ļ���� |
| B����ͼ2װ���ռ�һƿ������NO |
| C����ͼ3װ����U��������Һ����ұ��ֲ���ʱ֤��װ�ò�©�� |
| D����ͼ4װ����ȡ���ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ���������� | ���� |
| A | ��0.1mol?L-1��ˮϡ�ͳ�0.01mol?L-1�����pH��11.1���10.6 | ϡ�ͺ�NH3?H2O�ĵ���̶ȼ�С |
| B | �����£���ñ���Na2CO3��Һ��pH���ڱ���NaHCO3��Һ | ������ˮ��̶ȣ�CO32-��HCO3- |
| C | ��25mL��ˮ�ͷ�ˮ�зֱ����5��FeCl3������Һ��ǰ��Ϊ��ɫ������Ϊ���ɫ | �¶����ߣ�Fe3+��ˮ��̶����� |
| D | ������CaSO4����Na2CO3������Һ�У�һ��ʱ��������ɷ�ΪCaCO3 | ͬ�����ܽ�ȣ�CaSO4��CaCO3 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �������� | ��ʼ���� | ������ȫ |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 4.7 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
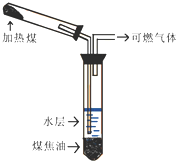 ú�ĸ���ʵ����ͼ��ʾ��
ú�ĸ���ʵ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 |
 |
 |
 |
| A������SO2����Ư���� | B������0.1mol?L-1NaOH��Һʱ���� | C���������ˮ�еĵ� | D������һ��Ũ��������Һ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Ϊ�˱���עˮ���ɫ���ˮ�֣����������������ڼ��뺬��ɳ����������ͼ���Ľ������ʣ������ʶ�����Σ���ܴ��ڸ���������˵������ȷ���ǣ�������
Ϊ�˱���עˮ���ɫ���ˮ�֣����������������ڼ��뺬��ɳ����������ͼ���Ľ������ʣ������ʶ�����Σ���ܴ��ڸ���������˵������ȷ���ǣ�������| A�����������ڷ����廯̨�� |
| B����һ�������¿ɷ���ȡ����Ӧ�ͼӳɷ�Ӧ |
| C��1mol���л����������Ʒ�Ӧ����3NA��H2���� |
| D�����л���ķ���ʽΪC3H21NO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�33.6L HF�к��з�ԭ�ӵ���ĿΪ1.5NA |
| B��1L 0.1mol/L��̼������Һ�е���������������0.1NA |
| C��30g SiO2����0.5NA��[SiO4]������ |
| D��ij�ܱ�������ʢ��0.1mol N2��0.3mol H2����һ�������³�ַ�Ӧ��ת�Ƶ��ӵ���ĿΪ0.6NA |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com