
【题目】室温下,H2R及其钠盐的混合溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH的变化关系如图所示。下列叙述错误的是
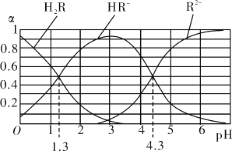
A. 由图可知:H2R的pKa1=1.3(已知:pKa= -lgKa)
B. 在pH=4.3的溶液中:3c(R2-) > c(Na+)
C. 0.2mol/L H2R溶液与0.3mol/L NaOH溶液等体积混合后的溶液中pH=4.3
D. 在pH=3的溶液中存在 ![]() =10-3
=10-3
【答案】C
【解析】
A.先计算Ka1,再计算pKa1;
B.结合溶液中电荷守恒进行分析;
C.结合溶液中离子种类进行分析;;
D.求出Ka1、Ka2,c(R2﹣)·c(H2R)/ c2(HR﹣)= Ka2·1/Ka1,据此分析;
A.Ka1=c(HR﹣)·c(H+)/c(H2R),当pH=1.3时c(HR﹣)=c(H2R),即Ka1=10-1.3,则pKa1=1.3,故A项正确;
B.在pH=4.3的溶液中,c(R2﹣)=c(HR﹣),溶液中电荷守恒为:2c(R2﹣)+c(HR﹣)+c(OH﹣)=c(Na+)+c(H+),所以3c(R2-)=c(Na+)+c(H+)﹣c(OH﹣),溶液呈酸性,即3c(R2-) > c(Na+),故B项正确;
C.0.2mol/L H2R溶液与0.3mol/L NaOH溶液等体积混合后,得到0.15mol/L Na2R和0.05mol/L NaHR混合溶液,此时c(R2﹣)>c(HR﹣),则pH>4.3,故C项错误;
D.根据pH=1.3时离子浓度求出Ka1=c(HR﹣)·c(H+)/c(H2R)=10-1.3,根据pH=4.3时离子浓度求出Ka2=c(R2﹣)·c(H+)/c(HR﹣)=10-4.3,Ka2·1/Ka1= c(R2﹣)·c(H2R)/ c2(HR﹣)=10-3,故D项正确;
综上,本题选C。


科目:高中化学 来源: 题型:
【题目】反应A2+B2![]() 2AB ΔH=QkJ/mol,在不同温度和压强改变的条件下,产物AB的生成情况如图所示:a为500℃、b为300℃的情况,c为反应在300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是
2AB ΔH=QkJ/mol,在不同温度和压强改变的条件下,产物AB的生成情况如图所示:a为500℃、b为300℃的情况,c为反应在300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是

A. A2、B2及AB均为气体,Q>0
B. AB为气体,A2、B2中有一种为非气体,Q>0
C. AB为气体,A2、B2中有一种为非气体,Q<0
D. AB为固体,A2、B2中有一种为非气体,Q>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应,得到如下表中的两组数据:已知2SO2(g)+ O2(g) ![]() 2SO3(g) △H<0
2SO3(g) △H<0
实验 编号 | 温度/℃ | 平衡常数 | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
下列说法中不正确的是
A. x=2.4
B. T1、T2的关系:T1>T2
C. K1、K2的关系:K2>K1
D. 实验1在前6 min的反应速率v(SO2)=0.2 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列叙述正确的是
A. 2.0gH218O与D216O的混合物中所含中子数为NA
B. 0.1molCl2溶于足量水中,转移的电子数为0.1NA
C. 常温常压下50g46%的乙醇溶液中,所含氧原子数目为0.5NA
D. 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2FeSO4![]() Fe2O3+SO2↑+SO3↑,利用下图所示装置检验硫酸亚铁的分解产物(乙、丙、丁中的试剂是足量的)。下列说法中不正确的是
Fe2O3+SO2↑+SO3↑,利用下图所示装置检验硫酸亚铁的分解产物(乙、丙、丁中的试剂是足量的)。下列说法中不正确的是
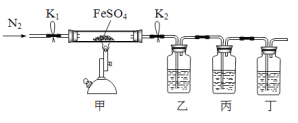
A. 乙、丙、丁中依次盛装的试剂可以是BaCl2溶液、品红溶液、NaOH溶液
B. 实验开始时,先打开K1和K2,缓缓通入N2一段时间,再点燃酒精喷灯加热
C. 若丙中盛装的是酸性KMnO4溶液检验SO2气体时,则SO2表现出还原性
D. 为了检验甲中残留固体中含有Fe3+,取少量固体加入稀硝酸溶解,再滴加KSCN溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种易溶于水的二元中强酸,KHC2O4溶液显酸性。现称取5.0g含H2C2O42H2O、KHC2O4和K2SO4的固体样品,加水溶解,配成250mL溶液。量取两份此溶液各25mL,分别置于两个锥形瓶中。第一份溶液中加入2滴酚酞试液,滴加0.2500mol/LNaOH溶液,滴定终点时消耗NaOH溶液16.00mL。第二份溶液用0.1000mol/L酸性KMnO4溶液滴定,当加入12.00mL酸性KMnO4溶液时恰好反应完全。
(1)K2C2O4溶液呈碱性的原因(用离子方程式表示)_______________________________。
(2)在该实验中不需要用到的实验仪器有___________(填字母编号)。
A.容量瓶 B.酸式滴定管 C.碱式滴定管 D.分液漏斗 E.锥形瓶 F.圆底烧瓶
(3)第一份用NaOH溶液滴定时,滴定终点的判断依据为____________________________________。
(4)原试样中KHC2O4的质量分数为__________%(保留3位有效数字)。
(5)如果用0.2500mol/LNaOH溶液滴定第一份溶液的实验中,在滴定终点时俯视读数。则测得的KHC2O4的质量分数_________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由烃A制备抗结肠炎药物H的一种合成路线如下 (部分反应略去试剂和条件):

回答下列问题:
(1)H的分子式是_____,A的化学名称是______。反应②的类型是_______。
(2)D的结构简式是___________。F中含有的官能团的名称是____________。
(3)E与足量NaOH溶液反应的化学方程式是______________。
(4)设计C→D和E→F两步反应的共同目的是_________。
(5)化合物X是H的同分异构体,X遇FeCl3溶液不发生显色反应,其核磁共振氢谱显示有3种不同化学环境的氢,峰面积比为3∶2∶2,写出1种符合要求的X的结构简式_________________。
(6)已知![]() 易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料制备化合物
易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料制备化合物![]() 的合成路线_______________________________(其他试剂任选)。
的合成路线_______________________________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证铜与稀硝酸反应的还原产物是NO而不是NO2。某同学设计了如图所示的装置,下列叙述错误的是( )

A.应先打开活塞,再从U形管右侧加入稀硝酸
B.加入的稀硝酸应充满U形管左侧
C.反应停止后打开活塞,气体变成红棕色
D.关闭活塞后铜丝会全部溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中,说法正确的是( )
①分子数比11:16②密度比11:16③体积比16:11④原子数比11:16
A.①③B.①④C.②③D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com